La aplicación de tecnologías de software en diversas gestiones de atención médica, incluyendo el diagnóstico o tratamiento de una condición de enfermedad, se está acelerando a un ritmo sin precedentes. Las Autoridades globales de Dispositivos Médicos están renovando sus regulaciones y directrices para abordar estas tecnologías de dispositivos en auge. En Australia, la Administración de Productos Terapéuticos (TGA) es la Autoridad Reglamentaria responsable de la supervisión de los Dispositivos Médicos, incluyendo el software y las aplicaciones móviles. En enero de 2021, la TGA publicó el borrador original sobre las regulaciones de software para Dispositivos Médicos, que fue revisado en febrero de 2021. El 27 de julio de 2021, la TGA publicó un diagrama de flujo detallado que aborda las ambigüedades comunes que los fabricantes de dispositivos y los profesionales reglamentarios pueden tener en relación con la clasificación del software de Dispositivos Médicos.
La TGA identifica el software utilizado en el ámbito de los Dispositivos Médicos como Software como Dispositivo Médico (SaMD), Software integrado en un Dispositivo Médico (SiMD) y Software que controla Dispositivos Médicos. Según la TGA, el término Software como Dispositivo Médico (o SaMD) es cualquier software que puede funcionar en una computadora portátil, teléfono inteligente o tableta cuyo propósito previsto se encuentra dentro de las normas de un Dispositivo Médico. En contraste, SiMD es un software que es una parte integral de un dispositivo y generalmente es importante para el funcionamiento preciso del dispositivo. Algunos softwares controlan los Dispositivos Médicos ya sea físicamente o a través de conexiones inalámbricas como Bluetooth, Wi-Fi, etc. La TGA regula los tres (03) tipos de software.
Algunos software de Dispositivos Médicos están excluidos o exentos de la reglamentación de software como Dispositivo Médico de la TGA basándose en los principios de alinear la reglamentación con la reglamentación internacional y reducir la carga mediante la no reglamentación de los productos, cuando no existe un riesgo importante para la seguridad y ya existen estructuras o marcos adecuados para los controles del producto o del sistema.
| Dispositivos de Software Exentos | Dispositivos de Software Excluidos |
|---|---|
Por ejemplo, algunos sistemas de apoyo a las decisiones clínicas que cumplen tres criterios principales: 1. Si el software no está destinado a analizar o procesar una imagen médica. 2. El software está diseñado para proporcionar únicamente apoyo/recomendación al profesional sanitario. 3. El software no pretende sustituir el juicio clínico del profesional. | Los productos que no entran en la categoría de Dispositivos Médicos y no están sujetos a ningún requisito reglamentario de la TGA se denominan dispositivos de software excluidos. P. ej.,
|
La TGA ha revisado la regulación de los Dispositivos Médicos que comprenden software que controla o interactúa con otros Dispositivos Médicos, ya sea externa o internamente, y el software que funciona como Dispositivo Médico (por derecho propio). Los cambios principales incluyen la introducción de nuevas reglas de clasificación, que aclaran el límite de los productos de software regulados, y se actualizaron los principios esenciales para clarificar los requisitos para los Dispositivos Médicos basados en software.
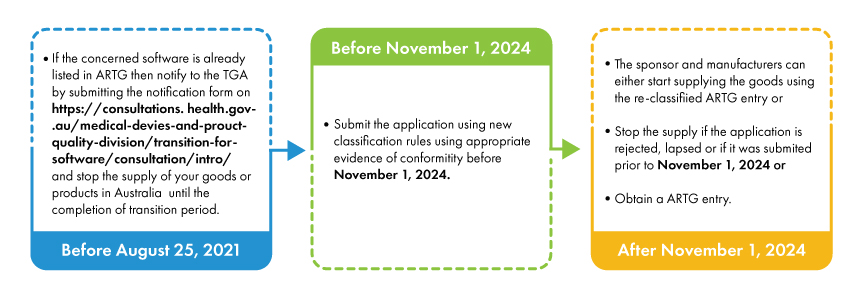
Con la introducción de nuevas reglas de clasificación, algunos Dispositivos Médicos basados en software están siendo reclasificados a clases de riesgo más altas y deben someterse a los procedimientos de evaluación de la conformidad pertinentes. Los patrocinadores y fabricantes de dichos dispositivos reclasificados deben estar registrados en el ARTG (Registro Australiano de Productos Terapéuticos) antes del 25 de febrero de 2021. Los fabricantes y patrocinadores que ya hayan solicitado a la TGA antes del 25 de febrero de 2021, deben presentar un formulario de notificación a la TGA.
Clasificación del software para Dispositivos Médicos en Australia:
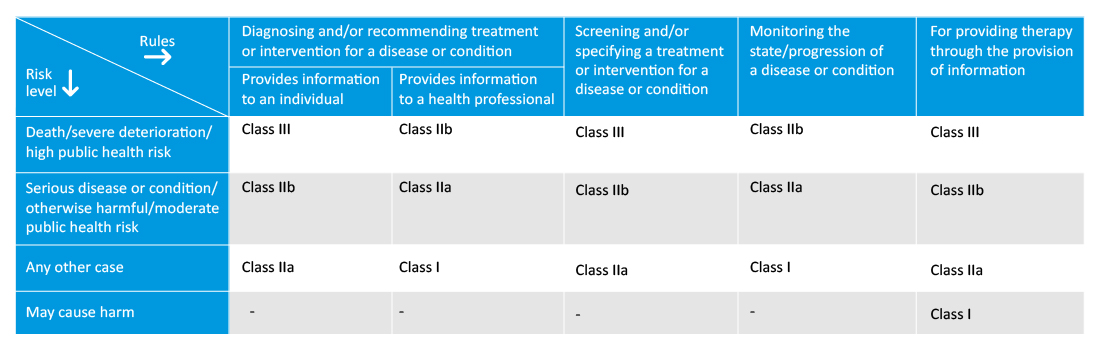
Los fabricantes deben especificar el propósito previsto del SaMD, lo que ayudará en los procedimientos de clasificación y evaluación de la conformidad. La nueva reglamentación también introduce las nuevas reglas de clasificación para Dispositivos Médicos programados y programables o Dispositivos Médicos de software, y la clase del software dependerá de la gravedad de la enfermedad monitoreada/tratada.
![]()
Modificaciones de los principios esenciales:
A continuación se detallan los cambios realizados en los principios esenciales con efecto a partir de 25 de febrero de 2021, al Dispositivo Médico basado en software.
Las enmiendas realizadas en la normativa de software por la TGA pueden aliviar la carga del fabricante para clasificar su software como regulado o no regulado y pueden ayudar en la preparación a tiempo de los documentos necesarios para la evaluación de conformidad de la TGA.
Con todos los escenarios decodificados, ¿su objetivo es que su software se incluya en el Registro Australiano de Productos Terapéuticos (ARTG) con menos carga? Para la inclusión en el ARTG de Dispositivos Médicos, IVD o SaMD, contacte a un experto. Manténgase informado. Manténgase conforme.