
Una 510(k) o una notificación previa a la comercialización es una presentación realizada a la Administración de Alimentos y Medicamentos de los Estados Unidos (FDA de US) para demostrar que el dispositivo a comercializar es seguro y eficaz, es decir, sustancialmente equivalente a un dispositivo comercializado legalmente o a un dispositivo de referencia. Los siguientes son los tres (03) tipos de 510(k) que un fabricante de Dispositivos Médicos puede presentar:
- Tradicional
- Abreviado
- 510(k) especial
En este blog, examinaremos los casos en los que su solicitud calificaría para el segundo tipo, un 510(k) abreviado, según los requisitos de la FDA de US.
Un 510(k) abreviado se utiliza para demostrar equivalencia sustancial con un estándar reconocido, un control especial o una guía mediante una Declaración de Conformidad (DoC). En una presentación abreviada, los fabricantes demuestran equivalencia sustancial con estándares reconocidos basándose en el uso de documentos de orientación o DoCs, en lugar de un dispositivo de referencia, para facilitar la revisión de la US FDA. A continuación se presenta el diagrama de flujo para determinar la equivalencia sustancial para una solicitud de 510(k) abreviado.
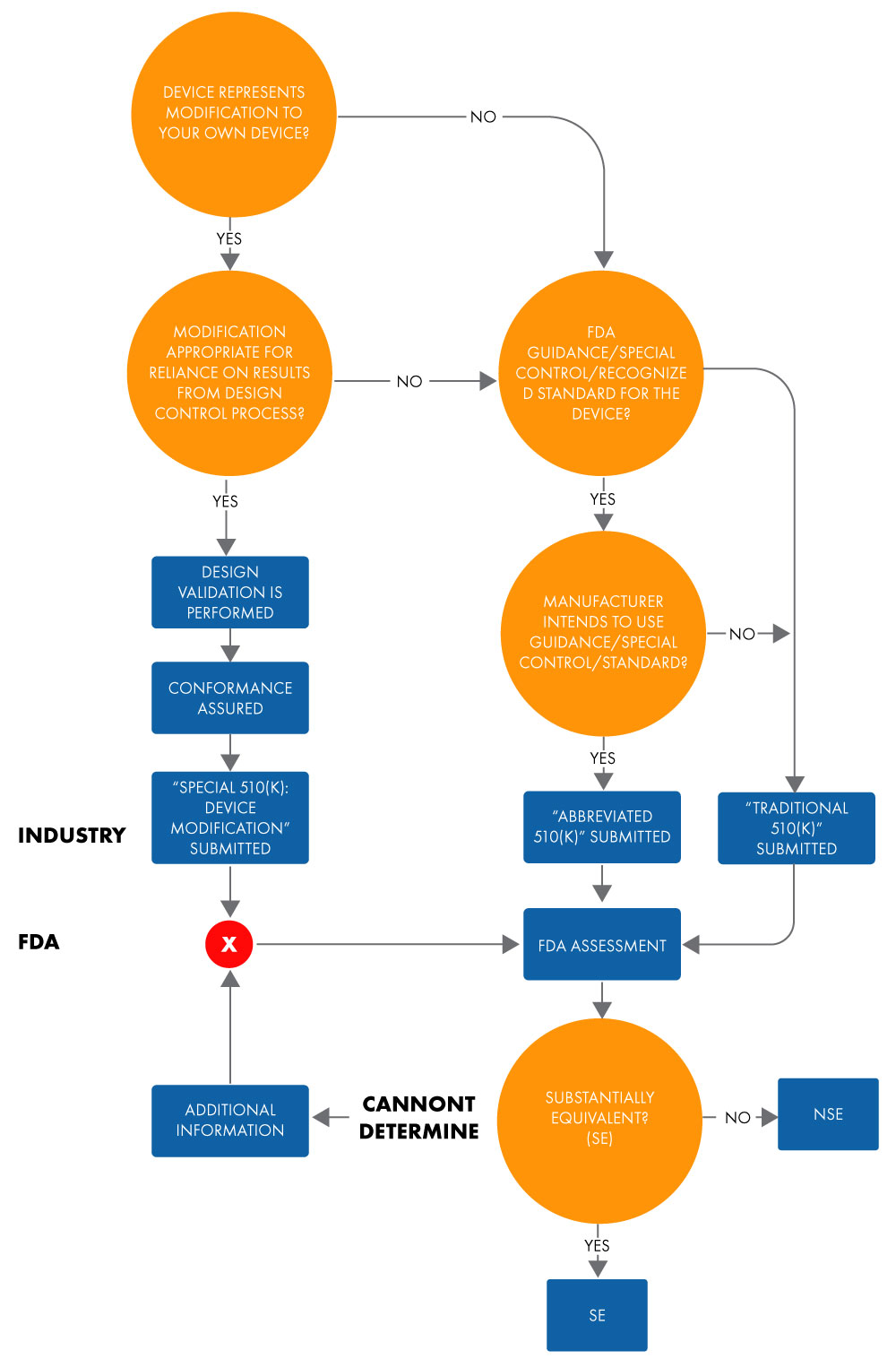
Figura 1: Intención de comercializar el dispositivo mediante 510(k)
El término "abreviado" sugiere que este tipo de proceso de aprobación 510(k) es más corto. Sin embargo, esto no es del todo cierto. Lleva tanto tiempo como una aprobación 510(k) tradicional. Lo mismo ocurre con la documentación y los costos. Además, el formato tanto para el 510(k) tradicional como para el abreviado, en términos de capitulación y estructura, son similares.
Al presentar un 510(k) abreviado, debe basarse en los elementos identificados en 21 CFR 807.87 (presentaciones tradicionales de 510[k]). Puede optar por presentar un 510(k) abreviado cuando la presentación se base en lo siguiente:
- Documentos de Orientación de la FDA: Al presentar un 510(k) abreviado, debe incluir un informe resumido que describa el cumplimiento del documento de orientación pertinente y cómo se utilizó durante el desarrollo y las pruebas del dispositivo.
- Demostración de Cumplimiento con Controles Especiales para el Tipo de Dispositivo: Debe cumplir con controles especiales como estándares de rendimiento, Post-marketing Surveillance (PMS), registros de pacientes, desarrollo y difusión de directrices, recomendaciones, etc., que proporcionan una garantía razonable de la seguridad y eficacia del dispositivo. Una solicitud 510(k) abreviada que se basa en un control(es) especial(es) debe incluir lo siguiente. Un informe resumido que describa la adhesión a los controles especiales y cómo se utilizaron durante el desarrollo y las pruebas del dispositivo.
- Cómo se utilizaron los controles especiales para abordar un riesgo o problema específico.
- Información que describe cualquier desviación de los controles específicos y los intentos del fabricante para cumplirlos.
- Estándar(es) de consenso voluntario: Se le requiere proporcionar una DoC según la norma reconocida para una presentación abreviada 510(k) que se base en ella. Una DoC debe incluir lo siguiente:
- El nombre y la dirección del solicitante/patrocinador responsable de la DoC.
- Detalles de la identificación del producto/dispositivo, incluidos los códigos de producto, el nombre comercial del dispositivo, el número de modelo y cualquier otro dato de identificación de producto único específico de la DoC en cuestión.
- Una declaración de conformidad.
- Una lista de estándares a los que se aplica la DoC, incluyendo la(s) opción(es) seleccionada(s) para cada estándar, si las hubiera.
- El número de reconocimiento de la US FDA para cada estándar.
- La fecha y el lugar de emisión de la DoC.
- La firma, el nombre impreso y la función del patrocinador responsable de la DoC.
- Cualquier limitación(es) sobre la validez de la DoC (por ejemplo, por cuánto tiempo es válida la declaración, qué se probó, las concesiones hechas sobre los resultados de las pruebas, etc.)
En conclusión, un 510(k) abreviado es una forma útil para que los fabricantes de dispositivos demuestren una equivalencia sustancial con estándares reconocidos o controles especiales utilizando una DoC. Para calificar para un 510(k) abreviado, los fabricantes de dispositivos deben proporcionar un informe resumido que explique su adhesión a los documentos de orientación pertinentes, demostrar el cumplimiento de los controles especiales y proporcionar DoCs a los estándares reconocidos. Sin embargo, es importante señalar que el proceso de aprobación, la documentación y el costo de un 510(k) abreviado son similares a los de un 510(k) tradicional.
¿Su dispositivo médico cumple los requisitos para una solicitud 510(k) abreviada? Para cualquier ayuda con la presentación de su solicitud 510(k) abreviada, contacte con nuestro experto reglamentario. ¡Manténgase informado! ¡Mantenga el cumplimiento!









