
Quando uno stabilimento estero è coinvolto nella produzione di un dispositivo medico importato negli Stati Uniti (US), è obbligatorio designare un agente US per tale stabilimento. L'agente US funge da punto di contatto per qualsiasi comunicazione della US Food and Drug Administration (US FDA) relativa alla struttura estera registrata. Poiché questa comunicazione può essere urgente, è fondamentale che l'agente US possieda una conoscenza approfondita delle normative US FDA e sia in grado di consigliare lo stabilimento estero sulla conformità ai requisiti US FDA per i dispositivi medici. Inoltre, avere un agente US indipendente aiuta a prevenire potenziali conflitti di interesse che potrebbero sorgere quando un partner commerciale viene designato come agente US. In questo blog, approfondiremo i dettagli della registrazione di uno stabilimento estero presso la US FDA.
Cos'è la Registrazione dello Stabilimento?
La registrazione annuale presso la US FDA è obbligatoria per i Produttori a Contratto, gli Importatori Iniziali, i Reimballatori/Rietichettatori, gli Sviluppatori di Specifiche, ecc., degli stabilimenti impegnati nella produzione e distribuzione di dispositivi medici destinati al mercato US, una procedura denominata Registrazione dello Stabilimento (Titolo 21 CFR Parte 807).
Chi deve richiedere la registrazione dello stabilimento?
I proprietari di strutture che si occupano della produzione e distribuzione di dispositivi medici destinati all'uso negli US devono completare una registrazione annuale presso la FDA degli US. I tipi di proprietari che possono richiedere la registrazione dello stabilimento sono:
- Proprietari di Stabilimenti Nazionali
- Proprietari di Stabilimenti Esteri
- Produttori a Contratto
- Importatori Iniziali
- Re-imballatori/Ri-etichettatori
- Sviluppatori di Specifiche
Quali sono le Fasi Coinvolte nel Processo di Registrazione dello Stabilimento?
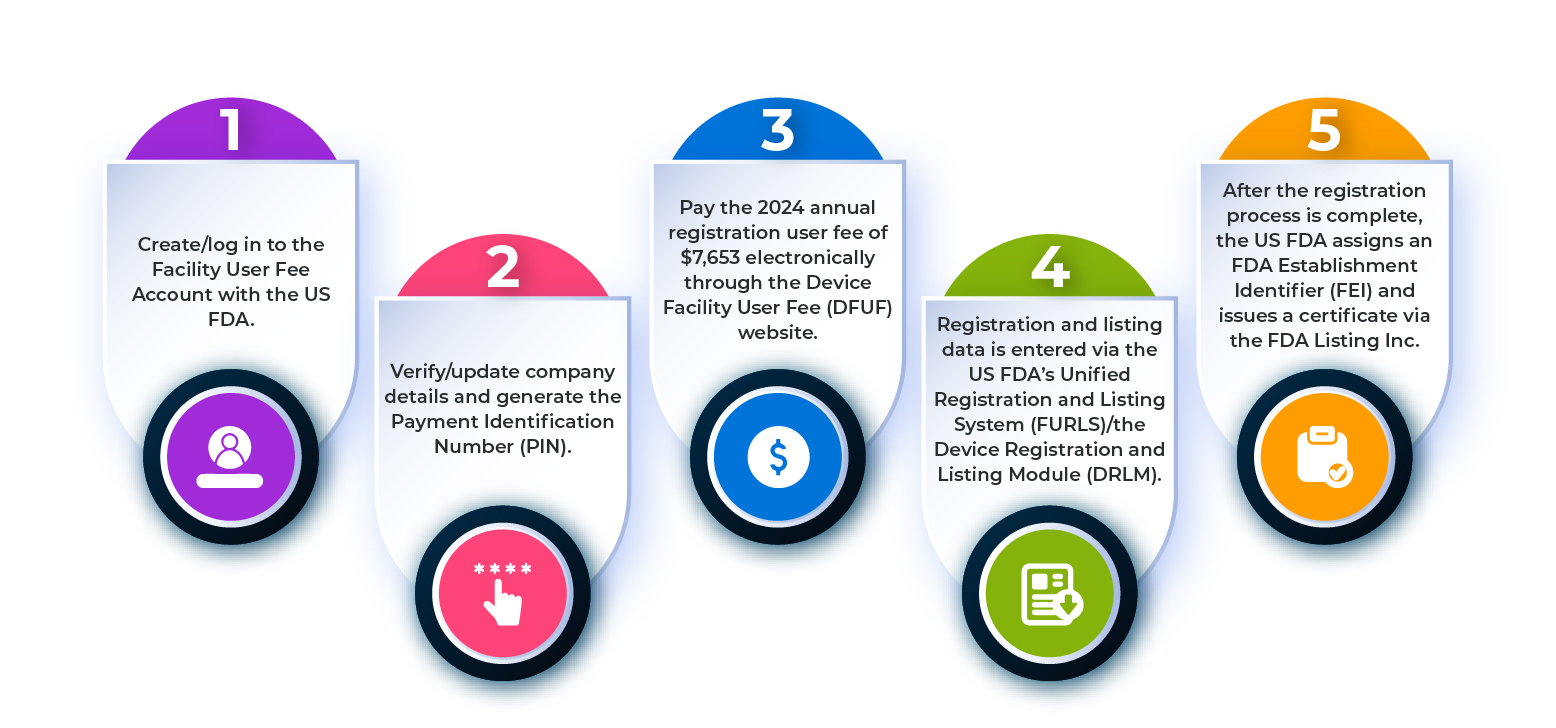
Per registrare uno stabilimento di dispositivi medici presso la US FDA, è necessario seguire i passaggi descritti nel diagramma di flusso sottostante.
Figura 1: Fasi del processo di registrazione dello stabilimento
Quali sono i requisiti di registrazione e di elenco per gli stabilimenti esteri?
Comprendere l'importanza di scegliere un agente US indipendente ed esperto aiuterà un'azienda straniera a dare priorità all'evitare qualsiasi conflitto di interessi, il che è fondamentale per le aziende mentre navigano nel complesso mondo della conformità US FDA. Le aziende straniere devono rafforzare la loro comprensione dei prerequisiti per raggiungere la conformità, promuovere solide partnership con gli agenti US e preparare il terreno per un processo di registrazione agevole. La tabella seguente illustra i requisiti di registrazione e di elenco in base alle attività di un'azienda straniera. Indica anche quali attività comportano una tassa di registrazione dell'azienda.
Tabella 1: Requisiti di registrazione e iscrizione basati sulle attività di uno stabilimento estero
| Attività | Registrati | Elenco | Paga la tariffa | |
| Fabbricante a contratto (inclusi i confezionatori a contratto) | SÌ 807.40 (a) | SÌ 807.40 (a) | SÌ | |
| Sterilizzatore a contratto | SÌ 807.40 (a) | SÌ 807.40 (a) | SÌ | |
| Produttori di dispositivi personalizzati | SÌ 807.20 (a) (2) | SÌ 807.20 (a) (2) | SÌ | |
| Dispositivo oggetto di indagine ai sensi dell'esenzione per dispositivi sperimentali (IDE) | NO 812.1 (a) | NO 812.1(a),807.40 (c) | NO | |
| Esportatore Estero di Dispositivi Situato in un Paese Estero | SÌ 807.40 (a) | SÌ 807.40 (a) | SÌ | |
| produttori esteri (inclusi gli assemblatori di kit) | SÌ 807.40 (a) | SÌ 807.40 (a) | SÌ | |
| Mantiene i registri dei reclami come richiesto ai sensi del 21 CFR 820.198 | SÌ | SÌ | SÌ | |
| Produttore di accessori confezionati o etichettati per la distribuzione commerciale a fini sanitari a un utente finale | SÌ 807.20 (a) (5) | SÌ 807.20 (a) (5) | SÌ | |
| Produttore di componenti distribuiti solo a un fabbricante di dispositivi finiti | NO 807.65 (a) | NO | NO | |
| Rietichettatori o Reimballatori | SÌ 807.20 (a) (3) | SÌ 807.20 (a) (3) | SÌ | |
| Rifabbricante | SÌ | SÌ | SÌ | |
| Rigeneratore di dispositivi monouso | SÌ 807.20 (a) | SÌ 807.20 (a) | SÌ | |
| Sviluppatori di Specifiche | SÌ | SÌ | SÌ | |
La registrazione dello stabilimento presso la FDA degli US è un requisito essenziale per gli stabilimenti esteri coinvolti nella produzione, vendita, riconfezionamento o importazione di dispositivi medici negli US. Questa registrazione garantisce la conformità alle severe normative e standard della FDA degli US. Freyr Solutions fornisce un valido supporto agli stabilimenti che cercano una guida esperta durante il processo di registrazione dello stabilimento. Sfruttando la propria esperienza e la conoscenza delle normative della FDA degli US, Freyr Solutions assiste gli stabilimenti esteri nel soddisfare i requisiti di conformità, portando in ultima analisi a un ingresso più agevole ed efficiente nel mercato dei dispositivi medici degli US. Per saperne di più sul processo di registrazione dello stabilimento presso la FDA degli US, contattateci oggi stesso. Rimanete informati! Rimanete conformi!









