L'applicazione delle tecnologie software nella gestione sanitaria, inclusa la diagnosi o il trattamento di una condizione patologica, sta accelerando a un ritmo senza precedenti. Le autorità globali per i dispositivi medici stanno rivedendo i loro regolamenti e linee guida per affrontare queste tecnologie di dispositivi in rapida crescita. In Australia, la Therapeutic Goods Administration (TGA) è l'Autorità Regolatoria responsabile della supervisione dei dispositivi medici, inclusi software e applicazioni mobili. Nel gennaio 2021, la TGA ha pubblicato la bozza originale sui regolamenti del software per dispositivi medici, che è stata rivista nel mese di febbraio 2021. Il 27 luglio 2021, la TGA ha pubblicato un diagramma di flusso dettagliato che affronta le ambiguità comuni che i produttori di dispositivi e i professionisti normativi possono avere in relazione alla classificazione del software per dispositivi medici.
La TGA identifica il software utilizzato nel settore dei dispositivi medici come Software as a Medical Device (SaMD), Software integrato in un dispositivo medico (SiMD) e Software che controlla i dispositivi medici. Secondo la TGA, il termine Software as a Medical Device (o SaMD) è qualsiasi software che può funzionare su un laptop, uno smartphone o un tablet il cui scopo previsto rientra nelle norme di un dispositivo medico. Al contrario, SiMD è un software che è parte integrante di un dispositivo ed è generalmente importante per il funzionamento accurato del dispositivo. Alcuni software controllano i dispositivi medici fisicamente o tramite connessioni wireless come Bluetooth, Wi-Fi, ecc. La TGA regola tutti e tre i tipi di software.
Pochi software per dispositivi medici sono esclusi o esentati dalla normativa TGA sui software come dispositivi medici, basandosi sui principi di allineamento della normativa con le regolamentazioni internazionali e di riduzione dell'onere attraverso la non regolamentazione dei prodotti, laddove non vi sia un rischio significativo per la sicurezza e siano già presenti strutture o quadri adeguati per i controlli del prodotto o del sistema.
| Dispositivi Software Esenti | Dispositivi Software Esclusi |
|---|---|
Ad esempio, Pochi sistemi di supporto alle decisioni cliniche che soddisfano tre criteri principali: 1. Se il software non è destinato ad analizzare o elaborare un'immagine medica. 2. Il software è destinato a fornire solo supporto/raccomandazione al professionista sanitario. 3. Il software non è destinato a sostituire il giudizio clinico del professionista. | I prodotti che non rientrano nella categoria dei dispositivi medici e non sono soggetti ad alcun requisito normativo della TGA sono definiti dispositivi software esclusi. Ad esempio,
|
La TGA ha rivisto la regolamentazione dei dispositivi medici che includono software che controlla o interagisce con altri dispositivi medici, sia esternamente che internamente, e del software che funziona autonomamente come dispositivo medico. Le principali modifiche includono l'introduzione di nuove regole di classificazione, che chiariscono i confini dei prodotti software regolamentati, e l'aggiornamento dei principi essenziali per specificare i requisiti per i dispositivi medici basati su software.
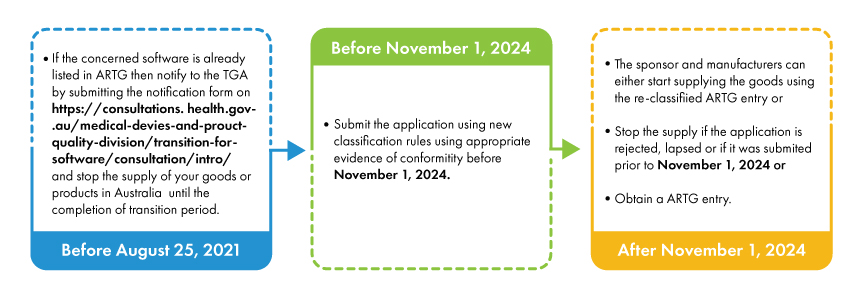
Con l'introduzione di nuove regole di classificazione, alcuni dispositivi medici basati su software vengono riclassificati in classi di rischio più elevate e devono essere sottoposti alle relative procedure di valutazione della conformità. Gli sponsor e i produttori di tali dispositivi riclassificati devono essere elencati nell'ARTG (Registro Australiano dei Prodotti Terapeutici) prima del 25 febbraio 2021. I produttori e gli sponsor che hanno già presentato domanda alla TGA prima del 25 febbraio 2021, devono presentare un modulo di notifica alla TGA.
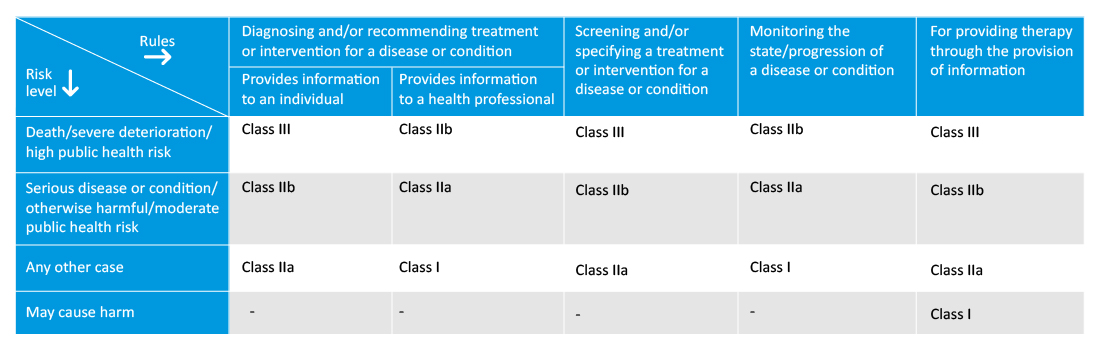
Classificazione del software per dispositivi medici in Australia:
I produttori devono specificare lo scopo previsto del SaMD, il che aiuterà nelle procedure di classificazione e valutazione della conformità successive. Il nuovo regolamento introduce anche le nuove regole di classificazione per i dispositivi medici programmati e programmabili o i dispositivi medici software, e la classe del software dipenderà dalla gravità della malattia monitorata/trattata.
![]()
Modifiche ai principi essenziali:
Di seguito sono riportate le modifiche apportate ai principi essenziali con effetto dal 25 febbraio 2021, al dispositivo medico basato su software.
Le modifiche apportate ai regolamenti sul software dalla TGA possono alleggerire l'onere per il fabbricante di classificare il proprio software come regolamentato o non regolamentato e possono aiutare nella preparazione tempestiva dei documenti richiesti per la valutazione di conformità della TGA.
Con tutti gli scenari decodificati, mirate a far elencare il vostro software nel Registro Australiano dei Beni Terapeutici (ARTG) con meno oneri? Per l'inserimento nell'ARTG di dispositivi medici, IVD o SaMD, contattate un esperto. Rimanete informati. Rimanete conformi.