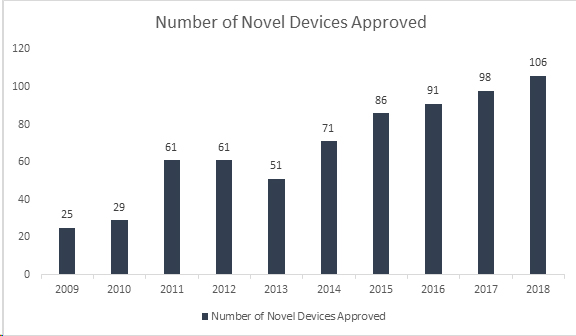
¿Sabía que la FDA ha establecido otro récord al aprobar 106 dispositivos novedosos en 2018, convirtiéndolo en el año más exitoso para los Dispositivos Médicos? Con este logro, la FDA ha superado su récord de 40 años establecido en 2017 de aprobación de 99 dispositivos novedosos, mostrando un crecimiento continuo durante los últimos 8 años. Los dispositivos aprobados incluyen una variedad de productos innovadores como sistemas automatizados de dosificación de insulina para niños, la válvula cardíaca más pequeña del mundo para recién nacidos, la primera aplicación médica móvil para ayudar a gestionar los trastornos por abuso de opioides y sustancias, y tecnologías de inteligencia artificial que diagnostican la retinopatía diabética.
La FDA siempre ha promovido la seguridad y la innovación de los Dispositivos Médicos para garantizar su alta calidad. Para mantenerse al día con este creciente número de aprobaciones de dispositivos novedosos y su seguridad, la FDA planea "modernizar" la vía de autorización de Dispositivos Médicos. Según la agencia, la modernización de la autorización puede requerir una nueva autoridad. En 2018, la FDA y el Centro de Dispositivos y Salud Radiológica (CDRH) publicaron un documento conjunto en el que se indicaba que el 510(k) era uno de los dos tipos de presentación añadidos a la definición de dispositivos novedosos. Junto con esto, las Exenciones para Dispositivos Humanitarios (HDE) también se añadieron a la definición de dispositivo novedoso tras los cambios realizados en el programa de Dispositivos Médicos innovadores del CDRH debido a la Ley del Siglo 21st.
La propuesta de la FDA y el CDRH responde a la necesidad potencial de buscar nuevas autoridades para modernizar el proceso 510(k). El motivo de la propuesta es limitar el uso de dispositivos de referencia, como Sustancialmente Equivalentes (SE), que tienen más de 10 años de antigüedad para promover la innovación. Es un paso adelante con respecto a la guía publicada por la agencia en abril de 2018. El borrador fue publicado por la FDA para proponer la expansión del programa 510(k) Abreviado en el CDRH de la FDA bajo el título – “Vía Basada en la Seguridad y el Rendimiento”. Se introdujo para disminuir la carga de las disposiciones sobre los dispositivos médicos. El enfoque también tiene como objetivo aumentar la eficiencia de la revisión de las presentaciones 510(k), reduciendo así la presión sobre la agencia.
Estos son algunos de los puntos destacados de la guía:
- La nueva vía evalúa la seguridad y eficacia de los dispositivos frente a los estándares establecidos de seguridad y métricas de rendimiento.
- A pesar de las nuevas normas, los dispositivos deberán cumplir con las normas existentes para poder ser comercializados
- La tecnología moderna se probará según los estándares modernos
- Este enfoque impulsará una mayor competencia para el desarrollo de dispositivos más seguros.
El número de dispositivos médicos que solicitan autorización ha aumentado exponencialmente a lo largo de los años. Esto ha dado un amplio margen a la FDA para adoptar e implementar medidas innovadoras para mejorar las vías de autorización. La agencia tiene una fuerte creencia en los méritos de esta propuesta, pero la respuesta de la industria aún está por descifrarse.
Con la FDA publicando continuamente nuevos documentos de orientación para actualizar el registro de Dispositivos Médicos, es necesario que los fabricantes de Dispositivos Médicos los sigan y actúen en consecuencia. Manténgase actualizado. Cumpla con la normativa.