24 de septiembre de 2016; con la fecha límite, a solo un mes, para el cumplimiento del Identificador Único de Dispositivo (UDI) para dispositivos de Clase II, es nuestra suposición, si no una certeza, que todos los fabricantes de Dispositivos Médicos están bien equipados con una hoja de ruta reglamentaria integral. Además de tener un conocimiento sólido de los requisitos previos de gobernanza, se espera que los fabricantes estén preparados para la auditoría de cumplimiento. Desde la validación de los registros del Identificador de Dispositivo (DI) y del Identificador de Producto (PI) hasta las presentaciones exitosas en GUDID, deben tener conocimientos sobre los datos a presentar y los procedimientos a seguir. Ya sea antes o después de la presentación, estar equipado con un mejor conocimiento del saber hacer procedimental podría proteger a los fabricantes de los desafíos correspondientes relacionados con la agregación de datos, la presentación de registros DI y la gestión de informes de dispositivos, el seguimiento de los acuses de recibo de las HA, etc.
Para equipar a los fabricantes con una mejor posición en tales escenarios, aquí proporcionamos una infografía de desafíos y soluciones de cumplimiento UDI fácil de entender, que podría ahorrarle tiempo para decodificar las complejidades del cumplimiento y planificar y estructurar mejor la hoja de ruta.
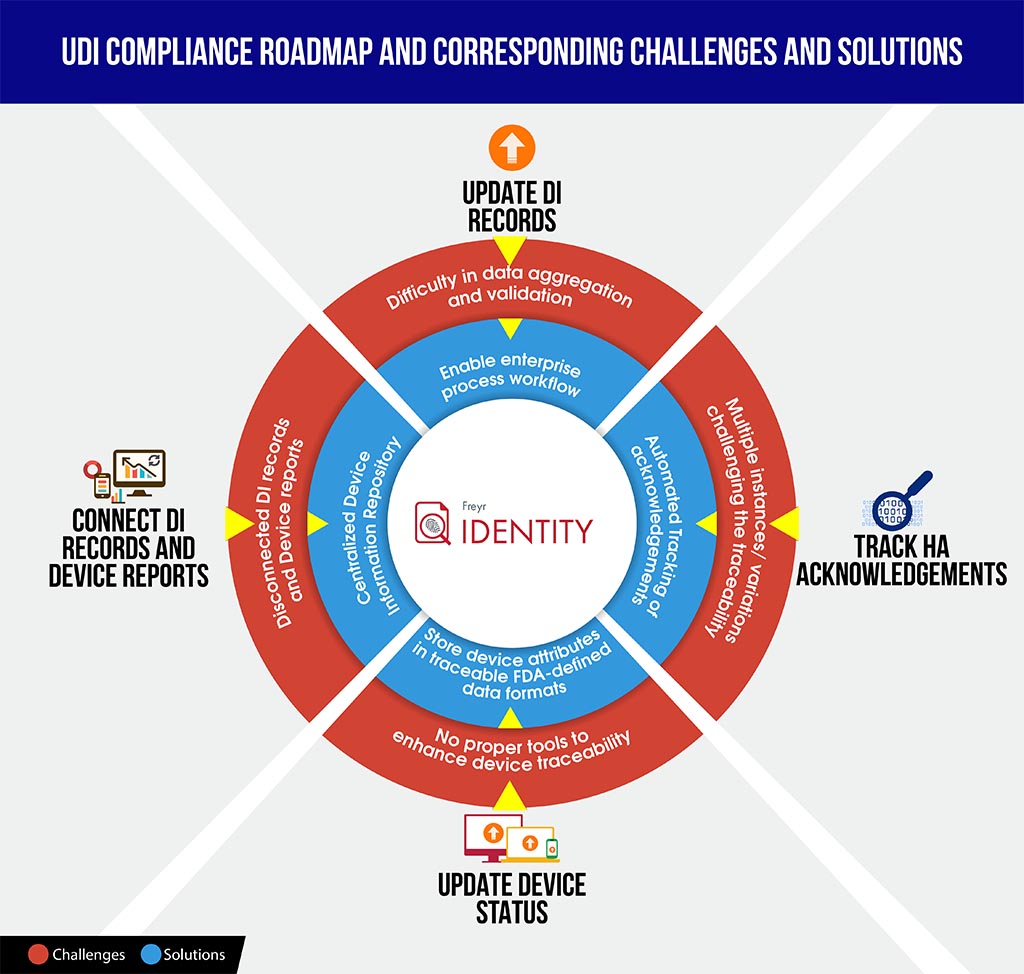
Para guiar a su organización sin problemas a través de este complejo proceso de cumplimiento, Freyr ofrece lo mejor de ambos mundos: una solución de software UDI bajo demanda, totalmente configurable, Freyr IDENTITY, así como un Centro de Excelencia UDI (CoE) que ofrece servicios UDI de primera clase, rentables y personalizables, diseñados en torno a sus requisitos únicos y exigentes.









