
La gestión de riesgos es una actividad crítica en todas las fases del ciclo de vida de los Dispositivos Médicos, ya que afecta directamente a la seguridad y el bienestar de los pacientes. Los riesgos son inevitables; sin embargo, pueden reducirse si las empresas son conscientes de los peligros inminentes y siguen procedimientos eficaces de gestión de riesgos.
El Análisis de Modos y Efectos de Falla (AMEF) es una herramienta de revisión para identificar posibles fallos en el diseño, en un proceso de fabricación o montaje, o en un producto o servicio de un dispositivo. Los «modos de fallo» se refieren a las formas en que un dispositivo podría fallar, lo que podría afectar a los pacientes. El «análisis de efectos» se refiere a examinar las consecuencias de esos fallos. Es un enfoque paso a paso para garantizar la fiabilidad y la calidad de un dispositivo.
Existen dos tipos de FMEA: FMEA de Diseño (DFMEA) y FMEA de Proceso (PFMEA). En el contexto de los Dispositivos Médicos, los fabricantes de dispositivos utilizan el DFMEA para evaluar fallos relacionados con el diseño y las especificaciones del dispositivo, mientras que el PFMEA se utiliza para mejorar el proceso de fabricación.
Aunque el FMEA se relaciona con el aspecto del riesgo, no es un sistema de gestión de riesgos. Los requisitos de la gestión de riesgos están definidos por la ISO 14971:2019, que sirve como marco para que los fabricantes de Dispositivos Médicos predigan la probabilidad de los riesgos y sus consecuencias a lo largo del ciclo de vida del producto. La metodología FMEA de evaluación de riesgos no se alinea con la ISO 14971:2019. El FMEA tiene su propio estándar aceptado internacionalmente, IEC 60812:2018, que explica cómo se planifica, realiza, documenta y mantiene el análisis de modos y efectos de fallos. El FMEA y la ISO 14971 difieren entre sí en ciertos aspectos, que son los siguientes:
Uso normal y condición de fallo
Según la ISO 14971, la gestión de riesgos incluye tanto el uso normal como el incorrecto del dispositivo, mientras que el FMEA incluye riesgos asociados únicamente con el fallo del dispositivo. Un ejemplo sencillo de esto serían los riesgos asociados con la línea intravenosa (IV). La ISO 14971 considera el riesgo potencial de infección a pesar de la administración correcta de una IV. Esto puede deberse a varias razones, como la baja inmunidad del paciente e infecciones presentes en el entorno hospitalario/clínico. Estos riesgos no se tienen en cuenta en una evaluación FMEA. Aunque los fabricantes de Dispositivos Médicos no pueden evitar completamente estos riesgos, pueden concienciar a los usuarios sobre los riesgos residuales asociados con el uso del dispositivo.
Evaluación de la gravedad.
La ISO 14971 considera la gravedad del riesgo basándose en el daño a la vida de las personas, mientras que el FMEA lo considera basándose en fallos en el rendimiento del sistema. La gravedad del riesgo puede considerarse baja en el FMEA si hay una pérdida menor de función, aunque pueda provocar la pérdida de vidas. La gravedad se considerará alta si el dispositivo se avería.
Por ejemplo, la FDA retiró una guía (Clase I) diseñada para encajar dentro de un catéter percutáneo para dirigir el catéter a través de un vaso sanguíneo. La guía en cuestión tiene el potencial de que el recubrimiento se desprenda. El FMEA clasificó esto como una gravedad de bajo riesgo después de la evaluación, pero puede tener implicaciones graves para la salud del paciente.
El procedimiento de evaluación de riesgos / modos de fallo
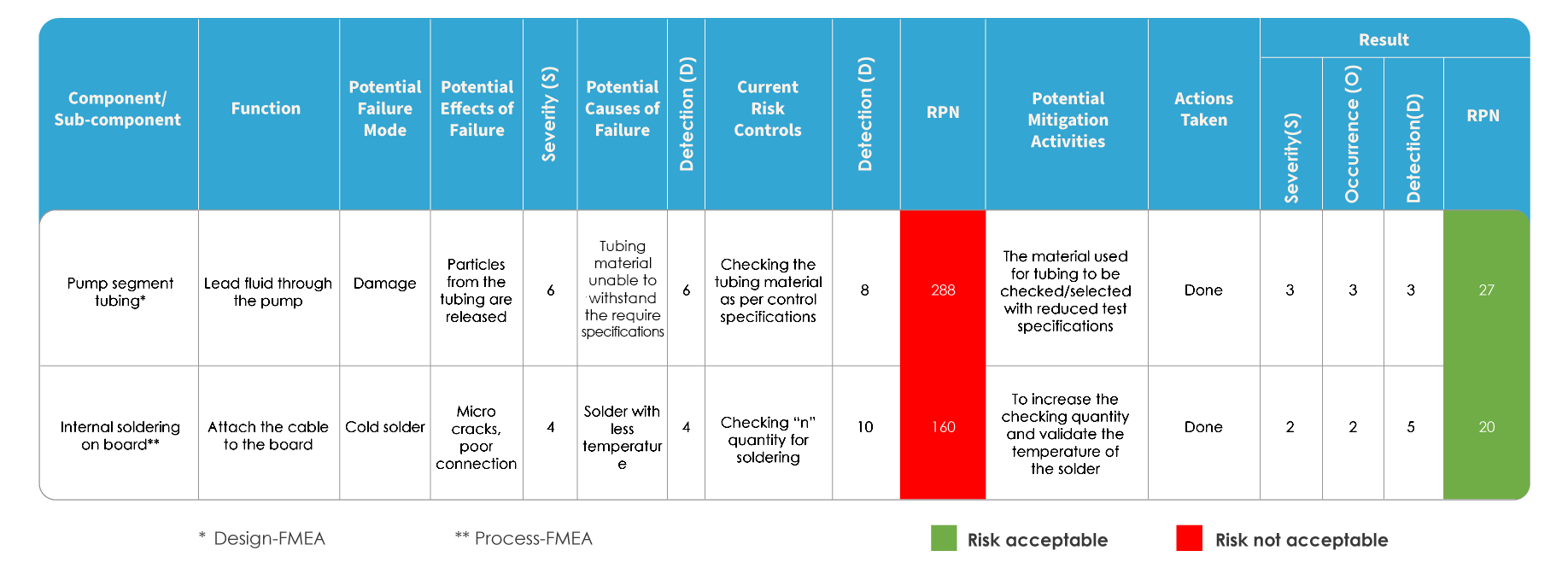
El FMEA y la ISO 14971 difieren en la forma en que se evalúa el riesgo. En el FMEA, el riesgo se evalúa identificando los posibles modos y efectos de fallo, seguido de la clasificación de la gravedad de los fallos. Se identifica cada una de las posibles causas y se determina la probabilidad de ocurrencia. El riesgo se evalúa en función del Número de Prioridad de Riesgo (RPN).
Mapeo de FMEA
En el caso de la gestión de riesgos según la ISO 14971, se utiliza una herramienta de trazabilidad conocida como Matriz de Trazabilidad de Peligros (HTM). Incluye el análisis, la evaluación, el control y la evaluación del riesgo residual.
Matriz de Trazabilidad de Peligros
| Análisis de Riesgos | Riesgo Evaluación | Control de Riesgos | ||||||||||||
| ID | Peligro | Secuencia o combinación de eventos razonablemente previsibles | Peligroso Situación | Daño | Incidencia | Gravedad | ¿Aceptable? | Opciones y Justificación del Control de Riesgos | Control de Riesgos Medidas | Riesgo Control Verificación | Estado | Potencial de Riesgo | Gravedad del riesgo | Riesgo residual |
| 1 | Tensión de línea | El usuario utiliza el dispositivo | El usuario/paciente puede estar expuesto a la tensión de la red eléctrica mientras está en contacto con el dispositivo. | Fallecimiento del usuario / paciente | 5 | 5 | N | La seguridad, mediante un cambio en el diseño y medidas de protección, puede establecerse. | Diseño según IEC 61010. | Las pruebas eléctricas deben realizarse según la norma IEC 61010 | Listo | 2 | 2 | Y |
![]()
Habiendo discutido las diferencias entre ambos, se puede concluir que la ISO 14971 sigue un enfoque integral hacia la gestión de riesgos, mientras que el FMEA es más una herramienta de fiabilidad. Sin embargo, los fabricantes de Dispositivos Médicos tendrían que cumplir con la ISO 14971 para satisfacer las expectativas de las autoridades reglamentarias en cuanto a los estándares de gestión de riesgos.
Para saber más sobre los servicios de consultoría en cumplimiento y gestión de riesgos de ISO 14971:2016, contacte a Freyr hoy mismo!









