Las autoridades sanitarias de todos los países, con la excepción de Canadá, exigen a todos Dispositivos Médicos extranjeros Dispositivos Médicos que designen a un representante local, residente en el país o autorizado. La función de un representante legal es representar al fabricante y al dispositivo en el país de destino, así como actuar de enlace entre las autoridades sanitarias y los fabricantes extranjeros. Existe una terminología específica para cada país en lo que respecta al representante local. En EE. UU., el representante local se denomina US », mientras que en el Reino Unido se le conoce como UKRP persona responsable en el Reino Unido). En Sri Lanka, el representante local se denomina «agente local de Sri Lanka» o «representante autorizado de Sri Lanka», quien también es el titular de la autorización de comercialización (MAH) del producto.
Dispositivos Médicos extranjeros Dispositivos Médicos pueden optar por designar a su distribuidor como agente local, quien, por defecto, también sería el titular de la autorización de comercialización (MAH). Sin embargo, se recomienda designar como MAH a un proveedor de servicios externo que no tenga conflictos de intereses. A continuación MAH enumeran las ventajas de designar a un proveedor de servicios externo independiente como MAH . El MAH :
- Ser competente en los Asuntos Regulatorios del país y los requisitos de vigilancia post-comercialización.
- Alcanzar los objetivos comerciales mediante el nombramiento de múltiples distribuidores para la penetración en el mercado
- Capacidad para centrarse en el cumplimiento reglamentario.
- Técnicamente competente para abordar las consultas planteadas por la Agencia
- Etiquetas comunes para un único MAH el país
- Evitar las complicaciones que supone tener que actualizar las etiquetas en caso de que cambie el distribuidor, que también actuaría como titular de la autorización de comercialización o agente MAH
En algunos países, como por ejemplo en la India, no existe ninguna disposición que permita transferir la autorización de comercialización, por lo que es necesario presentar una nueva solicitud. Por el contrario, en Sri Lanka, la Autoridad Nacional de Regulación de Medicamentos (NMRA) permitela transferencia MAH . El principal reto al que se enfrentan los fabricantes extranjeros de productos sanitarios al cambiar el MAH la obligación de presentar un certificado o carta de no objeción (NoC/NoL) del MAH actual. La NMRA también facilita la MAH MAH , incluso cuando MAH reacio a emitir un NoC.
El cambio de nombre o dirección del titular MAH de Sri Lanka no MAH considera una transferencia de la autorización de comercialización si el titular sigue siendo la misma persona o entidad, y dicho cambio deberá notificarse mediante una solicitud de modificación posterior a la autorización. El fabricante deberá ponerse en contacto directamente con la NMRA en caso de que tenga la intención de modificar los datos MAH en la solicitud que aún se encuentre en fase de tramitación por parte de la NMRA.
La necesidad de transferir un MAH MAH MAH en aquellos casos en que el fabricante decide desprenderse de la autorización de comercialización vigente o cuando otra entidad jurídica se hace cargo de dicha autorización. El MAH transferir se denomina «cedente», mientras que la empresa, la sociedad, la persona física o la entidad jurídica a la que se va a conceder la transferencia se denomina «cesionario».
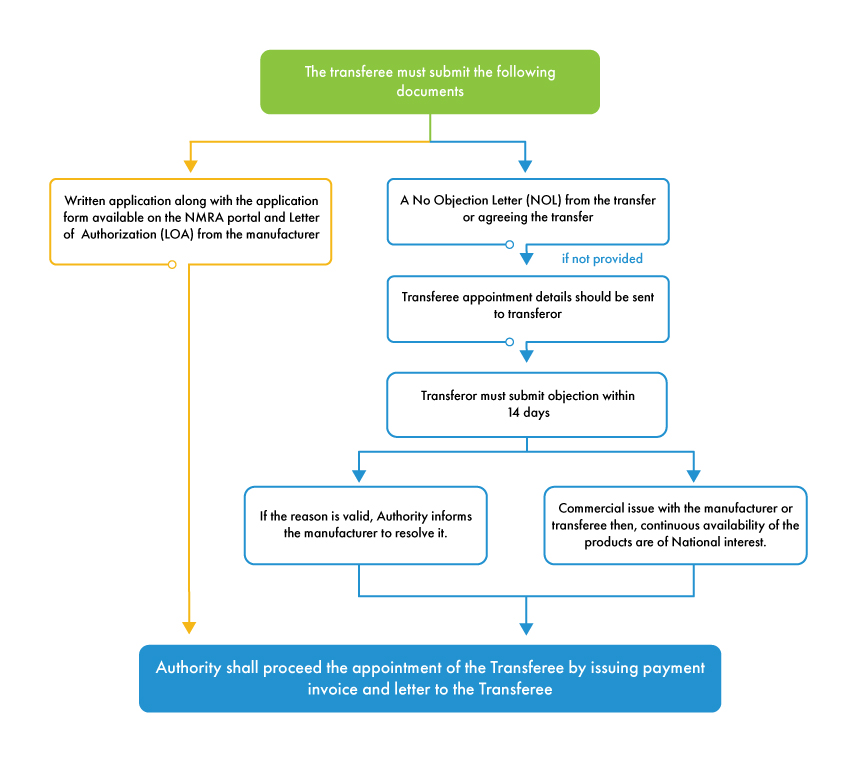
Para que se inicie el proceso MAH , el cedente debe emitir una carta de no objeción (NOL) en la que se manifieste su conformidad con la transferencia. Si el cedente se niega a emitir la NOL, la autoridad concede un plazo de 14 días para presentar la objeción contra el nombramiento del cesionario (nuevo MAH). Si el motivo de la objeción es válido y se refiere al fabricante, la autoridad informa al fabricante para que resuelva la objeción y procede con el proceso de transferencia. Si el cedente tiene algún conflicto comercial con el cesionario o el fabricante, la NMRA seguirá adelante con el proceso de transferencia, ya que a la autoridad le preocupa la disponibilidad del producto en el mercado de Sri Lanka más que las obligaciones comerciales entre las distintas partes interesadas.
A diferencia de otros países, la normativa de la NMRA es favorable para los fabricantes extranjeros en lo que respecta a MAH . La NMRA permite MAH con toda la documentación requerida, a menos que la objeción planteada por el cedente sea sustancial y genuina. Resulta beneficioso para todos los fabricantes extranjeros designar a un MAH independiente MAH evitar cualquier complicación en el proceso de autorización de comercialización de sus productos en Sri Lanka. El apoyo del agente Dispositivos Médicos en Sri Lanka sirve de plataforma para que todos los fabricantes extranjeros designen y cambien al MAH y con la documentación adecuada.
Si necesitaMAH de agente local o de titular de la autorización de comercialización (MAH , o servicios MAH en Sri Lanka, reach con un experto regional en materia de normativa. Manténgase informado. Cumpla con la normativa.









