A lo largo de los años, con los avances del software y la digitalización, ha habido un cambio radical en la forma en que se administran y entregan los Dispositivos Médicos. La integración del software con los Dispositivos Médicos ha aumentado rápidamente, impulsando avances increíbles en la entrega de soluciones sanitarias en diversos ámbitos como el diagnóstico, la prevención de enfermedades y el tratamiento de lesiones o enfermedades.
Sin embargo, el efecto del software en la seguridad y el rendimiento de los Dispositivos Médicos ha sido dudoso, particularmente cuando el propio dispositivo es un producto de solo software. Por lo tanto, las regulaciones de software para Dispositivos Médicos se revisan constantemente para determinar la consideración del software como Dispositivo Médico (SaMD). Recientemente, el consejo asesor de la Comisión Europea - Grupo de Coordinación de Dispositivos Médicos (MDCG) se ha centrado en mejorar las regulaciones del software para Dispositivos Médicos y ha publicado una guía que describe el enfoque a aplicar al determinar si un software es un Dispositivo Médico o no. ¿Qué describe la guía? Descubrámoslo.
El Alcance de la Guía
La guía del MDCG cubre tanto el software de Dispositivos Médicos como el software de Dispositivos Médicos de diagnóstico in vitro (IVD). Según el documento, un Software de Dispositivos Médicos (MDSW) se define como un software destinado a ser utilizado solo o en combinación, para un propósito especificado en la definición de "Dispositivo Médico" en el Reglamento de Dispositivos Médicos 2017/745 (MDR) o el Reglamento de Dispositivos Médicos de Diagnóstico In Vitro 2017/746 (IVDR). Describe los criterios a aplicar para determinar si un software sujeto a revisión es un Dispositivo Médico o no, y tiene como objetivo proporcionar aclaraciones y recomendaciones adicionales sobre MDSW para los fabricantes de Dispositivos Médicos y otras partes.
En primer lugar, la guía establece los términos más importantes utilizados en el contexto de MDSW, que incluyen:
Uso previsto: El uso para el que está destinado un dispositivo según los datos proporcionados por el fabricante en la etiqueta, en las instrucciones de uso, o en materiales o declaraciones promocionales o de venta y según lo especificado por el fabricante en la evaluación clínica.
Accesorio: Un artículo que, sin ser en sí mismo un dispositivo médico, está destinado por su fabricante a ser utilizado junto con uno o varios dispositivos médicos para permitir específicamente que los dispositivos médicos se utilicen de acuerdo con su(s) propósito(s) previsto(s) o para ayudar a la funcionalidad del dispositivo médico de los dispositivos médicos de forma específica y directa en términos de su(s) propósito(s) previsto(s). Además, el MDCG menciona que el accesorio de software puede impulsar o influir en el uso de un dispositivo médico y las instrucciones de uso y otra documentación proporcionada por el fabricante deben contener detalles sobre la forma en que se deben seleccionar el software y los accesorios adecuados.
Software: Se refiere a un conjunto de instrucciones que procesa datos de entrada y crea datos de salida.
Determinación del Software para Dispositivos Médicos
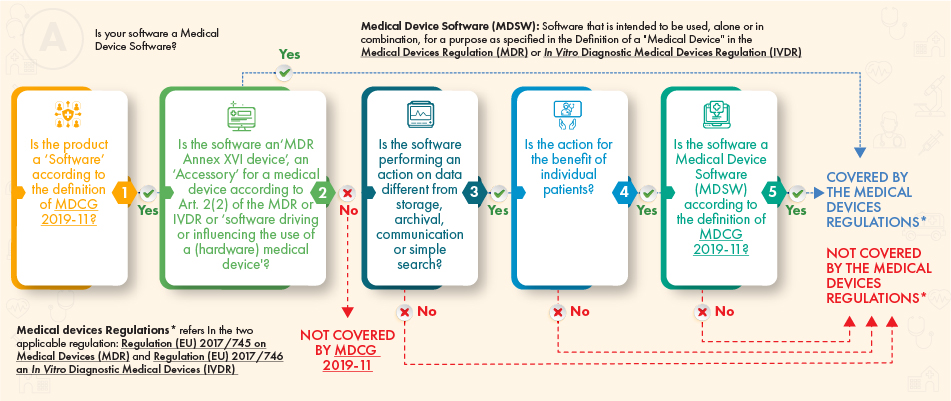
Según el diagrama de flujo de orientación anterior, el software en cuestión debería estar sujeto a regulación si cumple los siguientes criterios:
- La definición de un Dispositivo Médico, un accesorio del mismo, o que impulsa las operaciones del Dispositivo Médico, o
- Realiza un procesamiento adicional de datos (no solo almacenamiento o comunicación) y su acción crea beneficios para los pacientes y cumple con la definición de software para dispositivos médicos de acuerdo con la guía MDCG.
Determinación del software para Dispositivos Médicos de Diagnóstico In Vitro
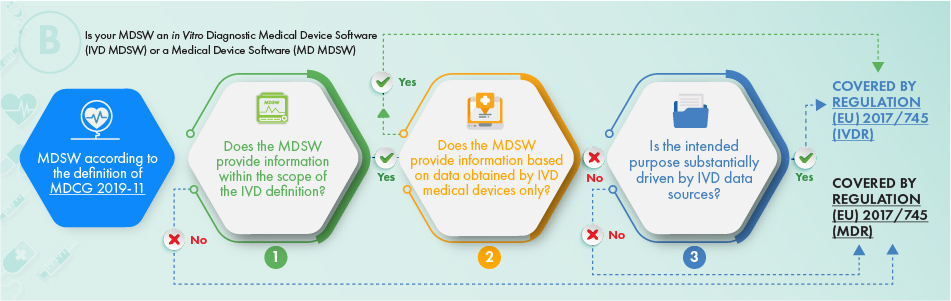
El diagrama de flujo anterior describe el enfoque que debe aplicarse con respecto a los productos destinados a fines de diagnóstico in vitro. Para determinar si el software en cuestión debe estar sujeto a regulación, deben abordarse los siguientes criterios:
- La definición de un Dispositivo Médico, un accesorio del mismo, o que impulsa las operaciones del Dispositivo Médico, o
- Proporciona la información que normalmente ofrecen los dispositivos médicos de diagnóstico in vitro y solo la información recopilada de un dispositivo médico de diagnóstico in vitro, o
- La finalidad prevista del software está relacionada con asuntos del IVDR
Según la guía del MDCG, el tipo de interconexión entre el software de Dispositivos Médicos y el dispositivo no afecta la calificación del software como dispositivo bajo el MDR y el IVDR. Un software de Dispositivos Médicos podría existir como producto independiente o incorporarse en un dispositivo de hardware, y aclara los siguientes requisitos reglamentarios:
- Considerando su cualificación y clasificación, un producto de software de dispositivo médico independiente debe someterse a todo el alcance de los procedimientos reglamentarios de acuerdo con la legislación aplicable.
- Un software de dispositivo médico que es un componente integral o parte de un dispositivo médico de hardware podría comercializarse bajo el procedimiento simplificado. Estaría sujeto a revisión no por separado, sino durante la evaluación general del propio dispositivo médico de hardware.
En resumen, la guía MDCG cubre los aspectos vitales relacionados con la clasificación del software de Dispositivos Médicos y la determinación de los requisitos reglamentarios a aplicar. Los fabricantes de Dispositivos Médicos, los desarrolladores de software y otras partes deben seguir e implementar las recomendaciones de la MDCG para garantizar el cumplimiento. Para obtener más información sobre cómo determinar su software como Dispositivo Médico, consulte a un experto reglamentario. Manténgase informado. Manténgase conforme.









