
El Reglamento de Dispositivos Médicos (MDR) de la Unión Europea (UE) ha sido noticia desde hace un tiempo. El MDR ha reemplazado la Directiva de Dispositivos Médicos (MDD) y la Directiva de Dispositivos Implantables Activos (AIMDD). Inicialmente, se estableció que toda la transición estaría en pleno efecto para mayo de 2020; sin embargo, debido a la aparición de la pandemia de COVID-19, la implementación se pospuso hasta el 26 de mayo de 2021. En este cronograma, para el 26 de mayo de 2024, todos los certificados de la MDD quedarán sin efecto, y los fabricantes de dispositivos deberán cumplir con el EU MDR. Además, los dispositivos de la MDD legalmente comercializados conforme a las Directivas 90/385/CEE y 93/42/CEE antes del 26 de mayo de 2020, y los dispositivos comercializados a partir del 26 de mayo de 2020, en virtud de un certificado, seguirán estando disponibles en el mercado hasta el 27 de mayo de 2025. Los plazos se muestran a continuación –
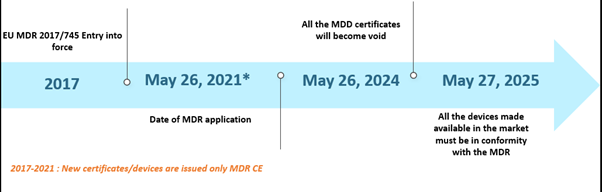
Los plazos de escenarios pasados del EU MDR
Sin embargo, la limitada capacidad de los Organismos Notificados (ON) y la falta de preparación de los fabricantes plantearon algunos desafíos en la implementación del EU MDR según el cronograma establecido. A octubre de 2022, en total, hay treinta y ocho (38) Organismos Notificados (ON), y estos ON recibieron alrededor de 8120 solicitudes para la certificación EU MDR, de las cuales se han emitido 1990 certificados. Según sus estimaciones con el cronograma inicial, solo se pudieron procesar 7000 certificados, y esto llevó a la extensión del plazo. Además, una de las otras razones probables de la extensión fue garantizar la disponibilidad continua de Dispositivos Médicos seguros cuyos certificados ya han caducado o están a punto de caducar antes del 26 de mayo de 2024. El escenario actual para el cronograma extendido se representa a continuación:
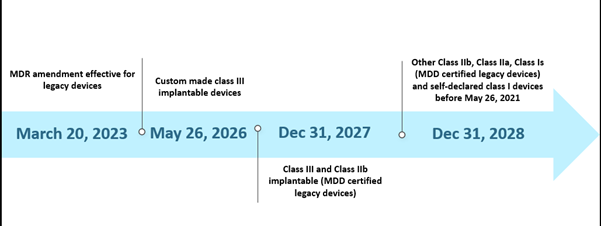
Los plazos de escenarios pasados del EU MDR
La nueva prórroga es aplicable a los dispositivos heredados que cumplen el artículo 120 (3e) con una certificación CE MDD válida o una derogación a fecha del 20 de marzo de 2023, y permanecerán en el mercado junto con los dispositivos con marcado CE MDR. Para el 26 de mayo de 2024, los fabricantes de dispositivos heredados deben tener un Sistema de Gestión de Calidad (SGC) implementado y haber presentado una solicitud a un Organismo Notificado (ON) designado por el MDR para la evaluación de la conformidad. Para el 26 de septiembre de 2024, los fabricantes de dispositivos heredados deben tener un acuerdo con un Organismo Notificado (ON) designado por el MDR.
Ahora veamos el impacto que los fabricantes podrían tener con esta prórroga.
Oportunidades que tienen los fabricantes con esta extensión:
- Acceso ampliado al mercado para los fabricantes de dispositivos certificados por MDD/AIMDD que ya han tomado las iniciativas de cumplimiento del MDR.
- Los fabricantes con certificación MDR cuyos certificados CE MDD/AIMDD no han sido revocados tienen permitido introducir dispositivos heredados en el mercado hasta el final del período de transición, además de sus dispositivos conformes con el MDR.
- Los fabricantes que tienen una derogación nacional a partir del 20 de marzo de 2023 pueden beneficiarse del período de transición.
- El período de extensión da más tiempo para una mejor comprensión de las normas y reglamentos, lo que ayuda a agilizar el proceso y lograr el cumplimiento del MDR.
Desafíos que podrían surgir para los fabricantes con esta extensión:
- No hay beneficio de mercado para los fabricantes de dispositivos heredados que no quisieron cumplir con el MDR.
- La extensión del MDR puede provocar que los procesos de certificación se prolonguen y retrasen los lanzamientos de productos, lo cual es un resultado directo del retraso en las revisiones por parte de los organismos notificados (NB).
¿Qué medidas deberían tomar los fabricantes?
- Es imperativo que los fabricantes determinen la clase de riesgo MDR de su dispositivo médico para identificar rápidamente el cronograma de transición adecuado según las regulaciones MDR modificadas.
- Para asegurar el cumplimiento con las regulaciones de MDR, es crucial identificar e iniciar comunicación con los Organismos Notificados (ON) designados por MDR que poseen la competencia específica requerida para la clasificación de su Dispositivo Médico.
- Es fundamental realizar una evaluación exhaustiva de las deficiencias de su dispositivo médico certificado bajo la MDD/AIMDD, identificar y abordar cualquier no conformidad con las regulaciones MDR y asegurar el cumplimiento a tiempo.
Es esencial que los fabricantes tomen medidas inmediatas para asegurar el cumplimiento con el MDR. El plazo ampliado ofrece algunas oportunidades para que los fabricantes logren el cumplimiento del MDR, pero también presenta desafíos, como procesos de certificación retrasados y el costo del cumplimiento. Para superar estos desafíos y aprovechar las oportunidades, permita que nuestro equipo de profesionales le asista a través del proceso de cumplimiento del MDR y asegure su éxito en este desafiante entorno reglamentario. Reserve una cita con nosotros hoy mismo para saber más sobre cómo podemos ayudarle a lograr el cumplimiento del MDR y a mantenerse a la vanguardia. Manténgase informado. Mantenga el cumplimiento.









