
Un protocolo de validación se define como un plan documentado para probar un Dispositivos Médicos para confirmar que el proceso de producción utilizado para fabricar el producto cumple con los requisitos específicos del usuario, técnicos y reglamentarios. Esto incluye una revisión de las variables del proceso y las limitaciones operativas, y el análisis de los resultados de las pruebas en condiciones de uso reales.
El proceso de validación implica varias acciones tangibles. Los pasos se explican a continuación:
- Primero, se forma el equipo de validación y a cada miembro se le asignan roles y responsabilidades específicas. El propósito de la validación del proceso es proporcionar una declaración clara de los objetivos de validación y definir el alcance de las actividades de validación, especificando los aspectos del Dispositivo Médico que se están validando. Luego, el equipo comprende los principios subyacentes del proceso para identificar parámetros específicos y resultados deseados.
- En segundo lugar, se establecen los criterios de evaluación y aceptación, junto con la selección de métodos de prueba, herramientas y técnicas de análisis estadístico adecuados. A continuación, se redactan los protocolos de validación de procesos y se implementan la Calificación de Instalación (IQ), la Calificación Operacional (OQ) y la Calificación de Desempeño (PQ).
- Finalmente, se determinan controles de proceso continuos y medidas de monitoreo para asegurar la validación continuada del proceso. Siempre que sea necesario, se realiza una revalidación para mantener la precisión y eficacia del proceso de validación.
La Figura 1 a continuación proporciona una representación paso a paso del proceso de validación.
Figura 1: Las etapas del proceso de validación
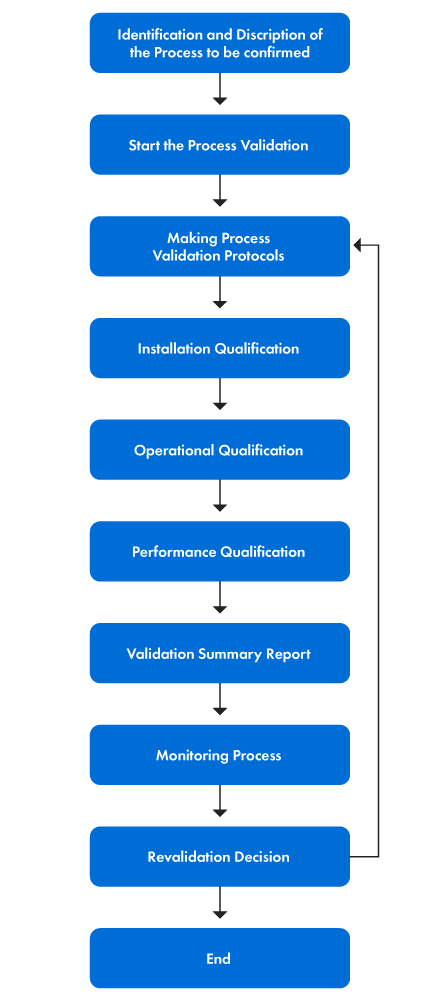
PVP
Debido a la amplia gama de volúmenes de producción y complejidades de fabricación, existen numerosos enfoques para llevar a cabo la validación de procesos. Sin embargo, las regulaciones de la Administración de Alimentos y Medicamentos de los Estados Unidos (USFDA) e ISO 13485 ofrecen sugerencias limitadas sobre métodos específicos. No obstante, una fuente ampliamente reconocida y autorizada para la validación de procesos de Dispositivos Médicos es un documento de orientación del Grupo de Trabajo de Armonización Global (GHTF), ahora llamado Foro Internacional de Reguladores de Dispositivos Médicos (IMDRF), publicado en 2004. Sigue siendo la referencia principal incluso en el sitio web oficial de la USFDA.
Según el documento de orientación, se forma un equipo de validación para crear un Plan Detallado de Validación de Procesos (PVP). Los protocolos de validación de procesos incluyen un esquema detallado sobre cómo implementar la CI, la CO, la CP y la revalidación. El PVP debe contener los siguientes elementos:
- Definición del dispositivo y determinación del enfoque de validación.
- Identificar los elementos que requieren validación.
- Realización de actividades en el sitio designado.
- Describir el alcance de la documentación.
- Creación de un cronograma para las actividades de validación.
- Desarrollar un cronograma maestro general.
- Mantener una lista exhaustiva y referencias tanto a las validaciones internas como externas que se han realizado.
El protocolo de validación se redacta antes de llevar a cabo las actividades de validación. Debe ser preparado por el equipo de validación y aprobado por el departamento correspondiente. El propósito de un protocolo de validación es definir los guiones de prueba que deben seguirse para garantizar que los procesos y equipos estén listos para fabricar productos de Dispositivos Médicos seguros y eficaces.
Un informe analítico que contiene información junto con los análisis, explicaciones y recomendaciones necesarios, forma parte del protocolo de validación. Estos registros se revisan posteriormente para asegurar que se cumplen los dos (02) criterios siguientes:
- Cumplimiento de los estándares reglamentarios.
- Todos los registros y datos generados se revisan para verificar los resultados, la idoneidad y la exhaustividad.
La Figura 2 a continuación representa el PVP y los diversos procesos que implica.
Figura 2: El PVP y sus Requisitos
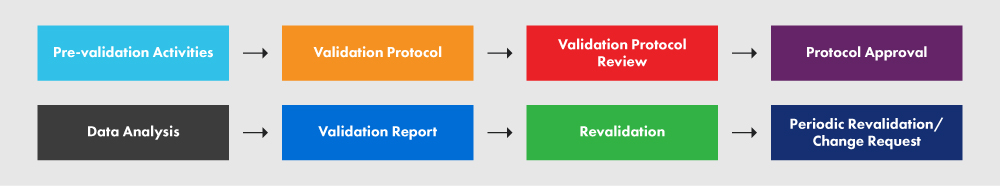
Un protocolo redactado adecuadamente proporciona directrices, políticas y procedimientos claros que deben seguirse durante la validación del proceso. Abarca aspectos como las instalaciones, los equipos, los métodos y la formación. El protocolo especifica los insumos y límites del proceso, así como los pasos esenciales para la ejecución exitosa del proyecto de validación del proceso. Si bien el siguiente esquema no abarca todos y cada uno de los elementos requeridos en su protocolo, le ofrece una visión general del nivel de detalle necesario. Recomendamos encarecidamente seguir el documento de orientación para una mejor comprensión del proceso.
- Página de título
- Productos a cubrir
- Equipo/Proceso a validar
- General
- Objetivos
- Documentos de referencia
- Plan de validación
- IQ
- OQ
- PQ
- Equipos de medición y ensayo y calibración
- Mantenimiento de Equipos
- Revalidación
- Aprobación del equipo de validación/Página de firma
La gestión de operaciones desempeña un papel crucial en el mantenimiento de un rendimiento óptimo mediante el seguimiento de las medidas clave, la revisión de los métodos y procedimientos de trabajo y la toma de medidas rápidas cuando surgen problemas. En los casos en que surjan problemas, es posible que deba revalidar un proceso parcial o incluso totalmente. Según la Sección 820.75(c) del Reglamento del Sistema de Calidad (QSR) de la USFDA, la revalidación del proceso debe considerarse en estas circunstancias: “Cuando se produzcan cambios o desviaciones del proceso, el fabricante debe revisar, evaluar y realizar la revalidación según corresponda. Estas actividades deben documentarse.”
Los posibles desencadenantes para la revalidación de procesos incluyen modificaciones en las especificaciones, métodos, procedimientos, software, diseños, componentes clave, escalado de lotes, cambios de ubicación, cambios de equipo y similares. Además, la implementación de Acciones Correctivas y Preventivas (CAPA) también puede servir como desencadenante para la revalidación del proceso. Las razones principales para la revalidación son las siguientes:
- Cambios realizados en el proceso.
- Tendencia negativa en la calidad, deterioro repentino de la calidad o un aumento drástico de las quejas de los clientes.
- Gran expansión de la capacidad de la línea.
- Cambios en el diseño.
- Cambios en el embalaje del producto.
- Transferencia de un proceso a otra instalación.
- Cambios en el proceso de solicitud.
Para saber más sobre los protocolos de validación y su importancia en el campo de la fabricación de Dispositivos Médicos, consúltenos. ¡Manténgase informado! ¡Manténgase en cumplimiento!









