24 settembre 2016; con la scadenza, a solo un mese di distanza, per la conformità all'Identificatore Unico del Dispositivo (UDI) per i dispositivi di Classe II, è nostra supposizione, se non certezza, che tutti i produttori di dispositivi medici siano ben attrezzati con una roadmap normativa completa. Oltre ad avere una solida padronanza dei prerequisiti di governance, i produttori devono essere pronti per l'audit di conformità. Dalla convalida dei record dell'Identificatore del Dispositivo (DI) e dell'Identificatore del Prodotto (PI) fino alle presentazioni GUDID di successo, devono essere a conoscenza dei dati da presentare e delle procedure da seguire. Sia in fase di pre-presentazione che di post-presentazione, una migliore conoscenza del know-how procedurale potrebbe proteggere i produttori dalle sfide corrispondenti relative all'aggregazione dei dati, alla presentazione dei record DI e alla gestione dei rapporti sui dispositivi, al tracciamento delle conferme HA, ecc.
Per fornire ai produttori una posizione migliore in tali scenari, qui forniamo un'infografica di facile comprensione sulle sfide e soluzioni per la conformità UDI, che potrebbe farvi risparmiare tempo nel decodificare le complessità della conformità e pianificare meglio e strutturare la tabella di marcia.
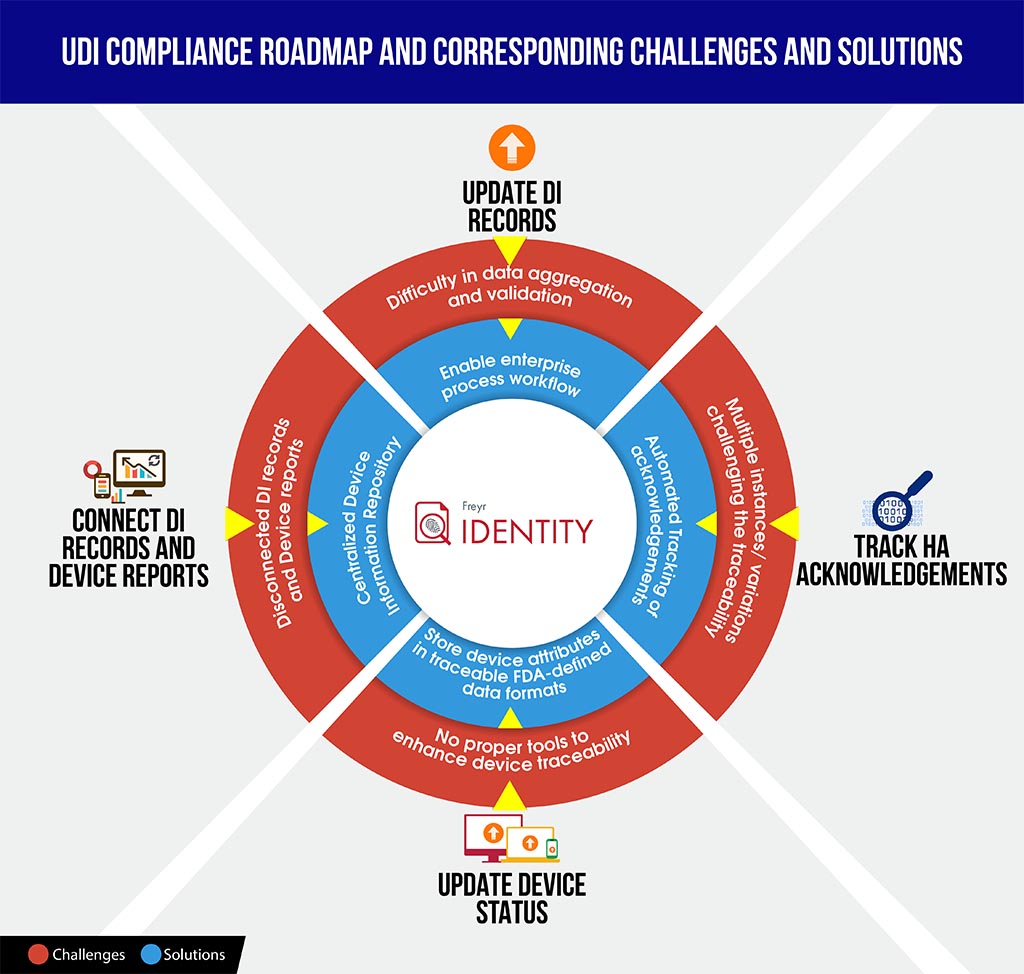
Per guidare agevolmente la vostra organizzazione attraverso questo complesso processo di conformità, Freyr offre il meglio di entrambi i mondi: una soluzione software UDI on-demand, completamente configurabile, Freyr IDENTITY, nonché un Centro di Eccellenza UDI (CoE) che offre servizi UDI di prim'ordine, convenienti e personalizzabili, costruiti attorno alle vostre esigenze uniche e complesse.









