Nel corso degli anni, con i progressi del software e della digitalizzazione, si è verificato un cambiamento epocale nel modo in cui i dispositivi medici vengono gestiti e forniti. L'integrazione del software con i dispositivi medici è aumentata rapidamente, portando a incredibili progressi nella fornitura di soluzioni sanitarie in vari ambiti come la diagnosi, la prevenzione delle malattie e il trattamento di lesioni o malattie.
Tuttavia, l'effetto del software sulla sicurezza e le prestazioni dei dispositivi medici è stato dubbio, in particolare quando il dispositivo stesso è un prodotto esclusivamente software. Pertanto, le normative sul software per dispositivi medici vengono costantemente riviste per determinare la considerazione del software come dispositivo medico (SaMD). Recentemente, il comitato consultivo della Commissione Europea - il Medical Device Coordination Group (MDCG) - si è concentrato sul miglioramento delle normative sul software per dispositivi medici e ha pubblicato una guida che descrive l'approccio da applicare per determinare se un software sia o meno un dispositivo medico. Cosa delinea la guida? Scopriamolo.
L'ambito della guida
La guida MDCG copre sia il software per dispositivi medici che il software per dispositivi medici diagnostici in vitro (IVD). Secondo il documento, un Software per Dispositivi Medici (MDSW) è definito come un software destinato ad essere utilizzato da solo o in combinazione, per uno scopo specificato nella definizione di “dispositivo medico” nel Regolamento sui Dispositivi Medici 2017/745 (MDR) o nel Regolamento sui Dispositivi Medici Diagnostici In Vitro 2017/746 (IVDR). Delinea i criteri da applicare per determinare se un software soggetto a revisione sia o meno un dispositivo medico e intende fornire ulteriori chiarimenti e raccomandazioni sull'MDSW per i produttori di dispositivi medici e altre parti.
In primo luogo, la guida illustra i termini più importanti utilizzati nel contesto dei MDSW, che includono:
Destinazione d'uso: L'uso per il quale un dispositivo è destinato secondo i dati forniti dal fabbricante sull'etichetta, nelle istruzioni per l'uso, o nei materiali o dichiarazioni promozionali o di vendita e come specificato dal fabbricante nella valutazione clinica.
Accessorio: Un articolo che, pur non essendo esso stesso un dispositivo medico, è destinato dal suo fabbricante ad essere utilizzato insieme a uno o più dispositivi medici per consentire specificamente l'uso del/dei dispositivo/i medico/i in conformità con il/i suo/i scopo/i previsto/i o per assistere la funzionalità del/dei dispositivo/i medico/i in modo specifico e diretto in relazione al/ai suo/i scopo/i previsto/i. Inoltre, l'MDCG menziona che l'accessorio software può guidare o influenzare l'uso di un dispositivo medico e le istruzioni per l'uso e altra documentazione fornita dal fabbricante dovrebbero contenere dettagli sul modo in cui il software e gli accessori appropriati dovrebbero essere selezionati.
Software: Si riferisce a un insieme di istruzioni che elabora i dati di input e crea i dati di output.
Determinazione del Software per Dispositivi Medici
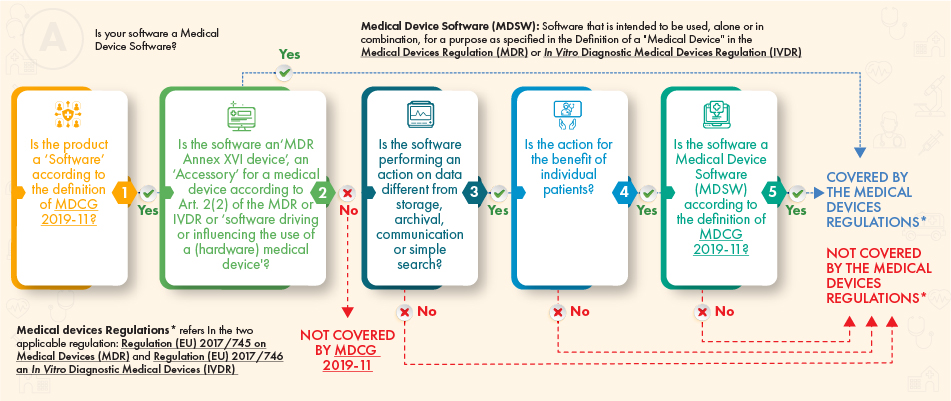
Secondo il diagramma di flusso delle linee guida sopra riportato, il software in questione dovrebbe essere soggetto a regolamentazione, se soddisfa i seguenti criteri:
- La definizione di un dispositivo medico, un suo accessorio, o che ne determina il funzionamento, o
- Esegue un'ulteriore elaborazione dei dati (non solo archiviazione o comunicazione) e la sua azione crea benefici per i pazienti e soddisfa la definizione di software per dispositivi medici in conformità con la guida MDCG.
Determinazione del Software per Dispositivi Medici Diagnostici In Vitro
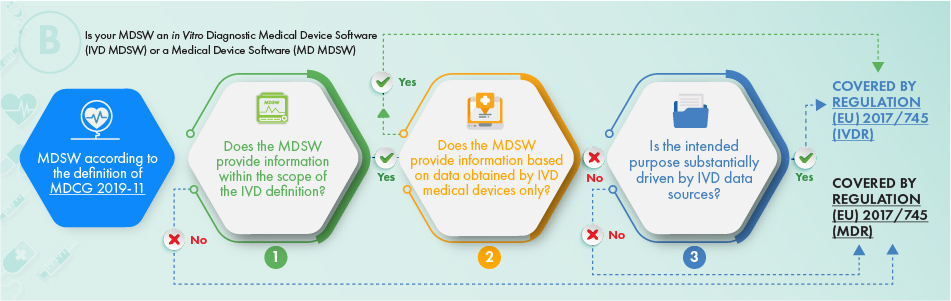
Il diagramma di flusso sopra riportato descrive l'approccio da applicare per quanto riguarda i prodotti destinati a scopi diagnostici in vitro. Per accertare se il software in questione debba essere soggetto a regolamentazione, è necessario considerare i seguenti criteri:
- La definizione di un dispositivo medico, un suo accessorio, o che ne determina il funzionamento, o
- Fornisce le informazioni solitamente fornite dai dispositivi medici diagnostici in vitro e solo le informazioni raccolte da un dispositivo medico diagnostico in vitro, oppure
- Lo scopo previsto del software è correlato alle questioni IVDR.
Secondo le linee guida MDCG, il tipo di interconnessione tra il software del dispositivo medico e il dispositivo non influisce sulla qualificazione del software come dispositivo ai sensi del MDR e dell'IVDR. Un software per dispositivi medici potrebbe esistere come prodotto autonomo o essere incorporato in un dispositivo hardware e chiarisce i seguenti requisiti normativi:
- Considerando la sua qualificazione e classificazione, un prodotto software per dispositivi medici autonomo deve essere soggetto all'intera gamma di procedure normative in conformità con la legislazione applicabile.
- Un software per dispositivi medici che è un componente integrale o parte di un dispositivo medico hardware potrebbe essere immesso sul mercato con la procedura semplificata. Sarebbe soggetto a revisione non separatamente, ma durante la valutazione generale del dispositivo medico hardware stesso.
In sintesi, la guida MDCG copre gli aspetti vitali relativi alla classificazione del software per dispositivi medici e alla determinazione dei requisiti normativi da applicare. I produttori di dispositivi medici, gli sviluppatori di software e altre parti devono seguire e implementare le raccomandazioni MDCG per garantire la conformità. Per ottenere ulteriori approfondimenti sulla determinazione del vostro software come dispositivo medico, consultate un esperto normativo. Rimanete informati. Rimanete conformi.









