
Una 510(k) o una notifica pre-commercializzazione è una richiesta presentata alla United States Food and Drug Administration (US FDA) per dimostrare che il dispositivo da commercializzare è sicuro ed efficace, ovvero sostanzialmente equivalente a un dispositivo legalmente commercializzato o a un dispositivo di riferimento. Di seguito sono riportati i tre tipi di 510(k) che un produttore di dispositivi medici può presentare:
- Tradizionale
- Abbreviato
- 510(k) Speciale
In questo blog, esamineremo i casi in cui la vostra domanda si qualificherebbe per il secondo tipo, un 510(k) abbreviato, secondo i requisiti della US FDA.
Un 510(k) abbreviato viene utilizzato per dimostrare l'equivalenza sostanziale a uno standard riconosciuto, un controllo speciale o una guida, utilizzando una Dichiarazione di Conformità (DoC). In una presentazione abbreviata, i produttori dimostrano l'equivalenza sostanziale a standard riconosciuti basandosi sull'uso di documenti di orientamento o DoC, anziché su un dispositivo precedente, per facilitare la revisione della US FDA. Di seguito è riportato il diagramma di flusso per determinare l'equivalenza sostanziale per una domanda di 510(k) abbreviato.
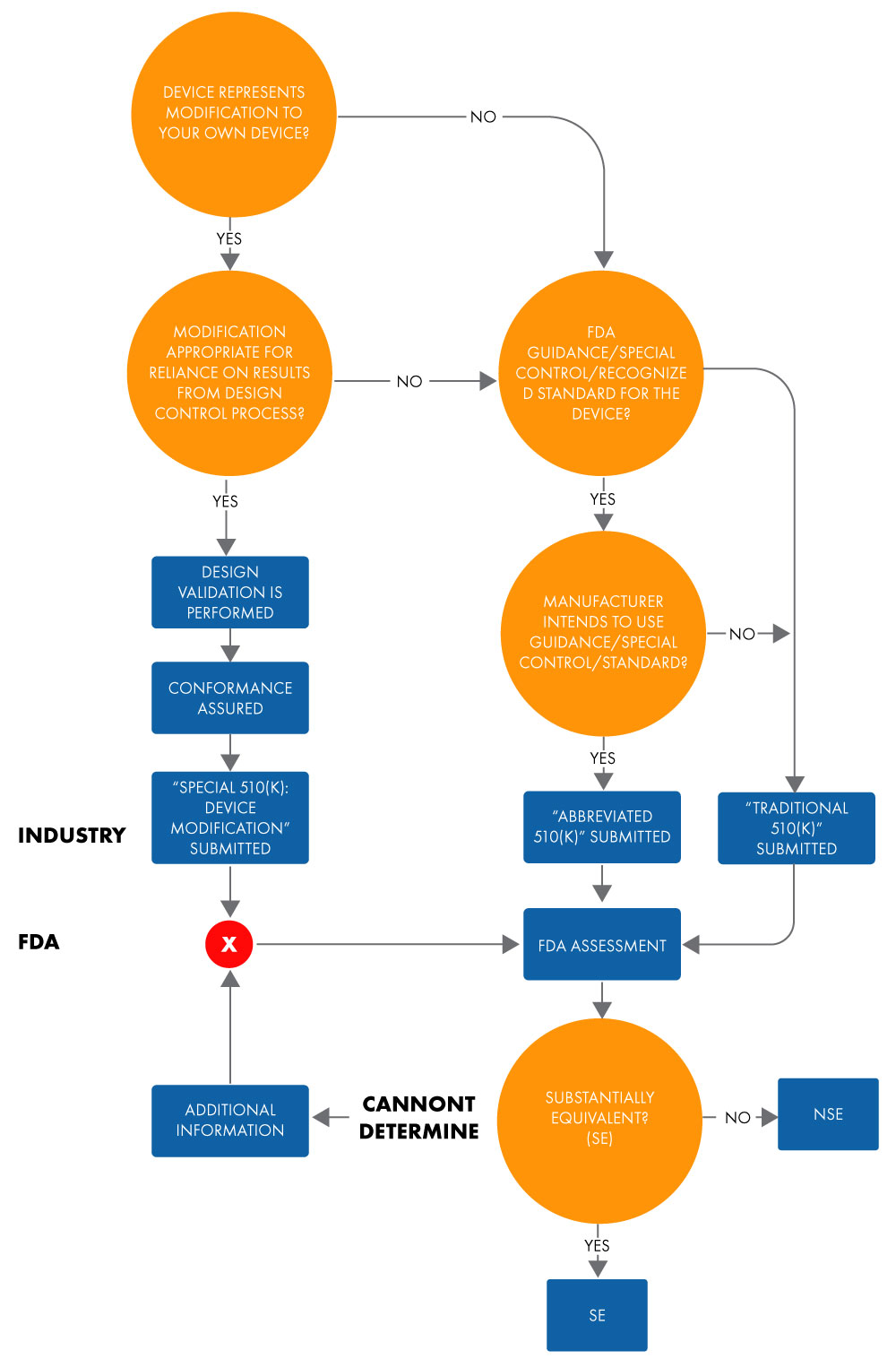
Figura 1: Intenzione di commercializzare il dispositivo tramite 510(k)
Il termine "abbreviato" suggerisce che questo tipo di processo di approvazione 510(k) sia più breve. Tuttavia, questo non è del tutto vero. Richiede lo stesso tempo di un'approvazione 510(k) tradizionale. Lo stesso vale per la documentazione e i costi. Inoltre, il formato sia per il 510(k) tradizionale che per quello abbreviato, in termini di suddivisione in capitoli e struttura, è simile.
Quando si presenta un 510(k) abbreviato, è necessario fare affidamento sugli elementi identificati nel 21 CFR 807.87 (presentazioni tradizionali 510[k]). Si può scegliere di presentare un 510(k) abbreviato quando la presentazione si basa su quanto segue:
- Documento/i di orientamento della FDA: Durante la presentazione di un 510(k) abbreviato, si dovrebbe includere un rapporto riassuntivo che illustri l'aderenza al documento di orientamento pertinente e come è stato utilizzato durante lo sviluppo e i test del dispositivo.
- Dimostrazione di conformità con controlli speciali per il tipo di dispositivo: È necessario conformarsi a controlli speciali come standard di prestazione, sorveglianza post-commercializzazione (PMS), registri dei pazienti, sviluppo e diffusione di linee guida, raccomandazioni, ecc., che forniscono una ragionevole garanzia della sicurezza e dell'efficacia del dispositivo. Una presentazione 510(k) abbreviata che si basa su uno o più controlli speciali dovrebbe includere quanto segue. Un rapporto riassuntivo che descrive l'adesione ai controlli speciali e come sono stati utilizzati durante lo sviluppo e i test del dispositivo.
- Come sono stati utilizzati i controlli speciali per affrontare un rischio o un problema specifico.
- Informazioni che descrivono eventuali deviazioni dai controlli specifici e i tentativi del produttore di conformarsi ad essi.
- Standard(s) di Consenso Volontario: È necessario fornire una DoC allo standard riconosciuto per una presentazione 510(k) abbreviata che si basa su di essa. Una DoC dovrebbe includere quanto segue:
- Il nome e l'indirizzo del richiedente/sponsor responsabile della DoC.
- Dettagli sull'identificazione del prodotto/dispositivo, inclusi i codici prodotto, il nome commerciale del dispositivo, il numero di modello e qualsiasi altro dato di identificazione unico del prodotto specifico per la DoC in questione.
- Una dichiarazione di conformità.
- Un elenco di standard per i quali la DoC è applicabile, incluse le opzioni selezionate per ciascuno standard, se presenti.
- Il numero di riconoscimento della FDA degli US per ogni standard.
- La data e il luogo di emissione della DoC.
- La firma, il nome stampato e la funzione dello sponsor responsabile della DoC.
- Eventuali limitazioni sulla validità della DoC (ad esempio, per quanto tempo la dichiarazione è valida, cosa è stato testato, le concessioni fatte sui risultati dei test, ecc.)
In conclusione, un 510(k) abbreviato è un modo utile per i produttori di dispositivi per dimostrare l'equivalenza sostanziale a standard riconosciuti o controlli speciali utilizzando una DoC. Per qualificarsi per un 510(k) abbreviato, i produttori di dispositivi devono fornire un rapporto riassuntivo che spieghi la loro aderenza ai documenti guida pertinenti, dimostrare la conformità ai controlli speciali e fornire DoC a standard riconosciuti. È, tuttavia, importante notare che il processo di approvazione, la documentazione e il costo di un 510(k) abbreviato sono simili a quelli di un 510(k) tradizionale.
Il vostro dispositivo medico è idoneo per una domanda 510(k) abbreviata? Per qualsiasi assistenza nella presentazione della vostra domanda 510(k) abbreviata, rivolgetevi al nostro esperto normativo. Rimanete informati! Rimanete conformi!









