
Zarządzanie ryzykiem jest kluczową czynnością na wszystkich etapach cyklu życia wyrobu medycznego, ponieważ bezpośrednio wpływa na bezpieczeństwo i dobro pacjentów. Ryzyka są nieuniknione; jednakże można je ograniczyć, jeśli firmy są świadome nadchodzących zagrożeń i przestrzegają skutecznych procedur zarządzania ryzykiem.
Analiza rodzajów i skutków wad (FMEA) jest narzędziem przeglądowym służącym do identyfikacji możliwych wad w projekcie, procesie produkcyjnym lub montażowym, a także w produkcie lub usłudze w ramach wyrobu. „Rodzaje wad” odnoszą się do sposobów, w jakie wyrób może ulec awarii, co może potencjalnie wpłynąć na pacjentów. „Analiza skutków” odnosi się do badania konsekwencji tych wad. Jest to podejście krok po kroku, mające na celu zapewnienie niezawodności i jakości wyrobu.
Istnieją dwa rodzaje analiz FMEA: FMEA Projektu (DFMEA) i FMEA Procesu (PFMEA). W kontekście wyrobów medycznych, producenci wyrobów wykorzystują DFMEA do oceny awarii dotyczących projektu i specyfikacji wyrobu, natomiast PFMEA służy do usprawniania procesu produkcyjnego.
Chociaż FMEA dotyczy aspektu ryzyka, nie jest to system zarządzania ryzykiem. Wymagania dotyczące zarządzania ryzykiem są określone w normie ISO 14971:2019, która służy producentom wyrobów medycznych jako ramy do przewidywania prawdopodobieństwa ryzyka i jego konsekwencji w całym cyklu życia produktu. Metodologia oceny ryzyka FMEA nie jest zgodna z normą ISO 14971:2019. FMEA ma własną, międzynarodowo uznaną normę, IEC 60812:2018, która wyjaśnia, w jaki sposób planuje się, wykonuje, dokumentuje i utrzymuje analizę rodzajów i skutków awarii. FMEA i ISO 14971 różnią się od siebie w pewnych aspektach, które przedstawiono poniżej:
Normalne użycie i stan awarii
Zgodnie z normą ISO 14971, zarządzanie ryzykiem obejmuje zarówno prawidłowe, jak i nieprawidłowe użycie wyrobu, natomiast FMEA obejmuje ryzyka związane wyłącznie z awarią wyrobu. Prostym przykładem są ryzyka związane z linią dożylną (IV). ISO 14971 uwzględnia potencjalne ryzyko infekcji pomimo prawidłowego podania dożylnego. Może to wynikać z różnych przyczyn, takich jak niska odporność pacjenta i infekcje obecne w środowisku szpitalnym/klinicznym. Ryzyka te nie są uwzględniane w ocenie FMEA. Chociaż producenci wyrobów medycznych nie mogą całkowicie uniknąć tych ryzyk, mogą informować użytkowników o ryzykach resztkowych związanych z użyciem wyrobu.
Ocena stopnia ciężkości
ISO 14971 uwzględnia dotkliwość ryzyka w oparciu o szkodę dla życia ludzi, natomiast FMEA uwzględnia to samo w oparciu o usterki w działaniu systemu. Dotkliwość ryzyka może być uznana za niską w FMEA, jeśli występuje niewielka utrata funkcji, nawet jeśli może to prowadzić do utraty życia. Dotkliwość zostanie uznana za wysoką, jeśli urządzenie ulegnie awarii.
Na przykład, FDA wycofała prowadnicę (Klasa I) przeznaczoną do umieszczenia w cewniku przezskórnym w celu skierowania cewnika przez naczynie krwionośne. Wspomniana prowadnica miała potencjał do łuszczenia się powłoki. FMEA potencjalnie sklasyfikowała to jako niskie ryzyko po ocenie, ale może to mieć poważne konsekwencje dla zdrowia pacjenta.
Procedura oceny ryzyka / trybów awarii
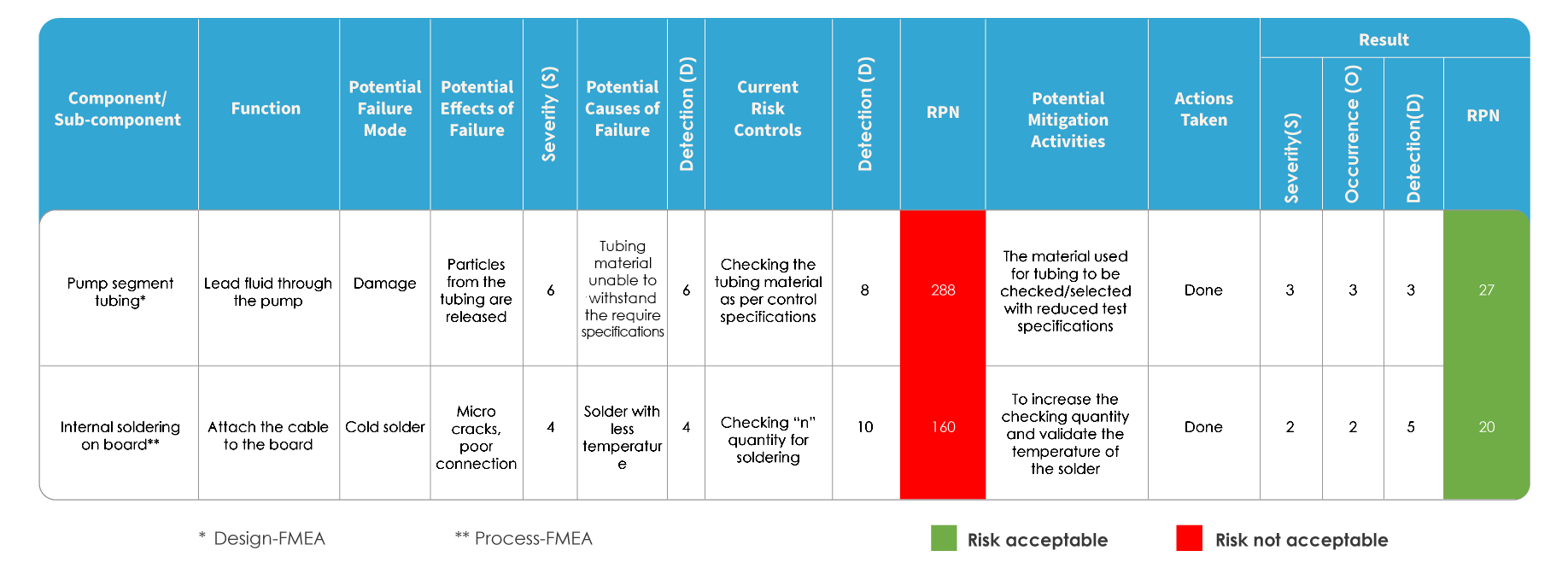
FMEA i ISO 14971 różnią się sposobem oceny ryzyka. W FMEA ryzyko ocenia się poprzez identyfikację potencjalnych trybów i skutków awarii, a następnie poprzez uszeregowanie dotliwości awarii. Identyfikuje się każdą z potencjalnych przyczyn i określa prawdopodobieństwo jej wystąpienia. Ryzyko jest oceniane na podstawie wskaźnika priorytetu ryzyka (RPN).
Mapowanie FMEA
W przypadku mapowania zarządzania ryzykiem zgodnie z normą ISO 14971, stosuje się narzędzie do śledzenia, znane jako Macierz Identyfikowalności Zagrożeń (HTM). Obejmuje ono analizę ryzyka, ocenę, kontrolę i ocenę ryzyka resztkowego.
Matryca identyfikowalności zagrożeń
| Analiza ryzyka | Ryzyko Ocena. | Kontrola Ryzyka | ||||||||||||
| ID | Zagrożenie | Rozsądnie przewidywalna sekwencja lub kombinacja zdarzeń | Niebezpieczny Sytuacja | Szkoda | Wystąpienie | Nasilenie | Akceptowalne? | Opcje Kontroli Ryzyka i Uzasadnienie | Kontrola Ryzyka Pomiary | Ryzyko Kontrola Weryfikacja | Status | Potencjał Ryzyka | Poważność Ryzyka | Ryzyko rezydualne |
| 1 | Napięcie sieciowe | Użytkownik używa urządzenia | Użytkownik/Pacjent może być narażony na napięcie sieciowe podczas kontaktu z urządzeniem | Zgon użytkownika / pacjenta | 5 | 5 | N | Bezpieczeństwo można zapewnić poprzez zmiany w projekcie i środki ochronne. | Projekt zgodny z IEC 61010. | Badania elektryczne należy przeprowadzić zgodnie z normą IEC 61010 | Gotowe | 2 | 2 | Y |
![]()
Po omówieniu różnic między tymi dwoma, można stwierdzić, że ISO 14971 stosuje kompleksowe podejście do zarządzania ryzykiem, natomiast FMEA jest bardziej narzędziem do oceny niezawodności. Jednakże producenci wyrobów medycznych musieliby przestrzegać normy ISO 14971, aby spełnić oczekiwania organów regulacyjnych dotyczące standardów zarządzania ryzykiem.
Aby dowiedzieć się więcej o zgodności z ISO 14971:2016 i usługach doradczych w zakresie zarządzania ryzykiem, skontaktuj się z Freyr już dziś!









