
Zgłoszenie 510(k) lub powiadomienie przed wprowadzeniem na rynek to zgłoszenie składane do Amerykańskiej Agencji ds. Żywności i Leków (US FDA) w celu wykazania, że wyrób, który ma być wprowadzony na rynek, jest bezpieczny i skuteczny, to znaczy, że jest zasadniczo równoważny z wyrobem legalnie wprowadzonym na rynek lub wyrobem referencyjnym. Poniżej przedstawiono trzy (03) typy zgłoszeń 510(k), które może złożyć producent wyrobów medycznych:
- Tradycyjny
- Skrócony
- Specjalne 510(k).
W tym blogu przeanalizujemy przypadki, w których Twój wniosek kwalifikowałby się do drugiego typu, skróconego 510(k), zgodnie z wymogami US FDA.
Skrócone zgłoszenie 510(k) służy do wykazania istotnej równoważności z uznanym standardem, specjalną kontrolą lub wytycznymi, przy użyciu Deklaracji Zgodności (DoC). W skróconym zgłoszeniu producenci wykazują istotną równoważność z uznanymi standardami na podstawie wykorzystania dokumentów wytycznych lub DoC, zamiast urządzenia referencyjnego, aby ułatwić przegląd US FDA. Poniżej przedstawiono schemat blokowy do określania istotnej równoważności dla skróconego wniosku 510(k).
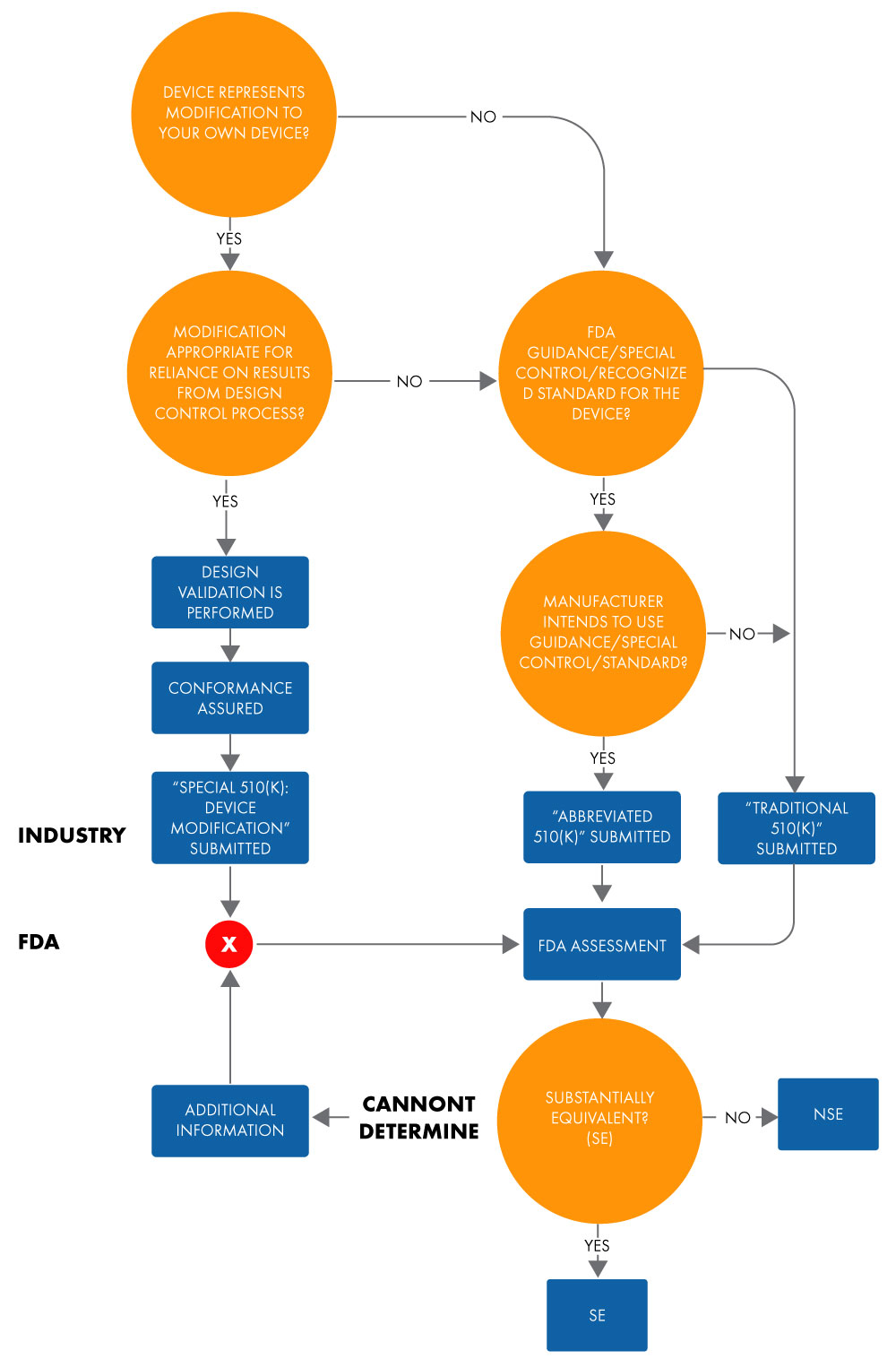
Rysunek 1: Zamiar wprowadzenia wyrobu na rynek za pośrednictwem 510(k)
Termin „skrócony” sugeruje, że ten typ procesu zatwierdzania 510(k) jest krótszy. Jednak nie jest to do końca prawda. Zajmuje tyle samo czasu co zatwierdzenie tradycyjnego 510(k). To samo dotyczy dokumentacji i kosztów. Ponadto format zarówno tradycyjnego, jak i skróconego 510(k), pod względem podziału na rozdziały i struktury, jest podobny.
Składając skrócone zgłoszenie 510(k), należy opierać się na elementach określonych w 21 CFR 807.87 (tradycyjne zgłoszenia 510[k]). Można zdecydować się na złożenie skróconego zgłoszenia 510(k), gdy zgłoszenie opiera się na następujących elementach:
- Dokument(y) wytycznych FDA: Składając skrócony wniosek 510(k), należy dołączyć raport podsumowujący, który przedstawia zgodność z odpowiednim dokumentem wytycznych i sposób jego wykorzystania podczas opracowywania i testowania urządzenia.
- Wykazanie zgodności ze specjalnymi kontrolami dla danego typu wyrobu: Należy przestrzegać specjalnych kontroli, takich jak normy wydajności, Nadzór po wprowadzeniu do obrotu (PMS), rejestry pacjentów, opracowywanie i rozpowszechnianie wytycznych, zaleceń itp., które zapewniają uzasadnione gwarancje bezpieczeństwa i skuteczności wyrobu. Skrócone zgłoszenie 510(k), które opiera się na specjalnych kontrolach, powinno zawierać następujące elementy. Raport podsumowujący, który opisuje przestrzeganie specjalnych kontroli i sposób ich wykorzystania podczas opracowywania i testowania wyrobu.
- Jak specjalne środki kontroli zostały wykorzystane do rozwiązania określonego ryzyka lub problemu.
- Informacje opisujące wszelkie odstępstwa od określonych kontroli oraz próby producenta w celu ich przestrzegania.
- Dobrowolna Norma(y) Konsensusu: Wymagane jest dostarczenie deklaracji zgodności (DoC) z uznaną normą dla skróconego zgłoszenia 510(k), które na niej polega. DoC powinno zawierać następujące elementy:
- Nazwa i adres wnioskodawcy/sponsora odpowiedzialnego za DoC.
- Szczegóły identyfikacji produktu/wyrobu, w tym kody produktów, nazwa marketingowa wyrobu, numer modelu oraz wszelkie inne unikalne dane identyfikacyjne produktu specyficzne dla danego DoC.
- Oświadczenie o zgodności.
- Lista norm, dla których ma zastosowanie DoC, w tym wybrane opcje dla każdej normy, jeśli takie istnieją.
- Numer uznania US FDA dla każdej normy.
- Data i miejsce wydania DoC.
- Podpis, imię i nazwisko (drukowane) oraz funkcja sponsora odpowiedzialnego za DoC.
- Wszelkie ograniczenia dotyczące ważności DoC (na przykład, jak długo deklaracja jest ważna, co było testowane, ustępstwa dotyczące wyników testów itp.).
Podsumowując, skrócone zgłoszenie 510(k) jest użytecznym sposobem dla producentów wyrobów na wykazanie istotnej równoważności z uznanymi normami lub specjalnymi kontrolami za pomocą DoC. Aby zakwalifikować się do skróconego zgłoszenia 510(k), producenci wyrobów muszą przedstawić raport podsumowujący, wyjaśniający ich zgodność z odpowiednimi dokumentami wytycznymi, wykazać zgodność ze specjalnymi kontrolami i dostarczyć DoC do uznanych norm. Należy jednak zauważyć, że proces zatwierdzania, dokumentacja i koszt skróconego zgłoszenia 510(k) są podobne do tych w przypadku tradycyjnego zgłoszenia 510(k).
Czy Twój wyrób medyczny kwalifikuje się do skróconego wniosku 510(k)? W celu uzyskania pomocy w złożeniu skróconego wniosku 510(k) skontaktuj się z naszym ekspertem ds. regulacji. Bądź na bieżąco! Zachowaj zgodność!









