
La gestione del rischio è un'attività critica in tutte le fasi del ciclo di vita dei dispositivi medici, poiché influisce direttamente sulla sicurezza e sul benessere dei pazienti. I rischi sono inevitabili; tuttavia, possono essere ridotti se le aziende sono consapevoli dei pericoli imminenti e seguono procedure efficaci di gestione del rischio.
L'analisi dei modi e degli effetti dei guasti (FMEA) è uno strumento di revisione per identificare possibili guasti in un progetto, un processo di produzione o assemblaggio, o un prodotto o servizio in un dispositivo. I “modi di guasto” si riferiscono ai modi in cui un dispositivo potrebbe guastarsi, il che potrebbe potenzialmente influenzare i pazienti. L'“analisi degli effetti” si riferisce all'esame delle conseguenze di tali guasti. È un approccio passo-passo per garantire l'affidabilità e la qualità di un dispositivo.
Esistono due tipi di FMEA: FMEA di Progettazione (DFMEA) e FMEA di Processo (PFMEA). Nel contesto dei dispositivi medici, i produttori di dispositivi utilizzano la DFMEA per valutare i guasti relativi alla progettazione e alle specifiche del dispositivo, mentre la PFMEA è utilizzata per migliorare il processo di produzione.
Sebbene l'FMEA coinvolga l'aspetto del rischio, non è un sistema di gestione del rischio. I requisiti della gestione del rischio sono definiti dalla ISO 14971:2019, che funge da quadro di riferimento per i produttori di dispositivi medici per prevedere la probabilità dei rischi e le loro conseguenze durante l'intero ciclo di vita del prodotto. La metodologia FMEA di valutazione del rischio non è allineata con la ISO 14971:2019. L'FMEA ha un proprio standard accettato a livello internazionale, IEC 60812:2018, che spiega come l'analisi dei modi e degli effetti dei guasti viene pianificata, eseguita, documentata e mantenuta. L'FMEA e la ISO 14971 differiscono tra loro in alcuni aspetti, che sono i seguenti:
Uso Normale e Condizione di Guasto
Secondo la ISO 14971, la gestione del rischio include sia l'uso normale che quello scorretto del dispositivo, mentre l'FMEA include i rischi associati solo al guasto del dispositivo. Un semplice esempio di ciò sarebbero i rischi associati alla linea endovenosa (IV). La ISO 14971 considera il potenziale rischio di infezione nonostante la corretta somministrazione di un IV. Ciò può essere dovuto a varie ragioni, come la bassa immunità del paziente e le infezioni presenti nell'ambiente ospedaliero/clinico. Questi rischi non sono considerati in una valutazione FMEA. Sebbene i produttori di dispositivi medici non possano evitare completamente questi rischi, possono rendere gli utenti consapevoli dei rischi residui associati all'uso del dispositivo.
Valutazione della gravità.
La norma ISO 14971 considera la gravità del rischio basandosi sul danno alla vita delle persone, mentre la FMEA la considera basandosi su malfunzionamenti nelle prestazioni del sistema. La gravità del rischio può essere considerata bassa nella FMEA in caso di una perdita minore di funzionalità, anche se ciò potrebbe portare alla perdita di vite umane. La gravità sarà considerata alta se il dispositivo si guasta.
Ad esempio, la FDA ha richiamato un filo guida (Classe I) destinato a essere inserito in un catetere percutaneo per dirigere il catetere attraverso un vaso sanguigno. Il filo guida in questione ha il potenziale che il rivestimento si sfaldi. La FMEA ha potenzialmente classificato questo come una gravità a basso rischio dopo la valutazione, ma può avere gravi implicazioni sulla salute del paziente.
La procedura di valutazione del rischio / delle modalità di guasto
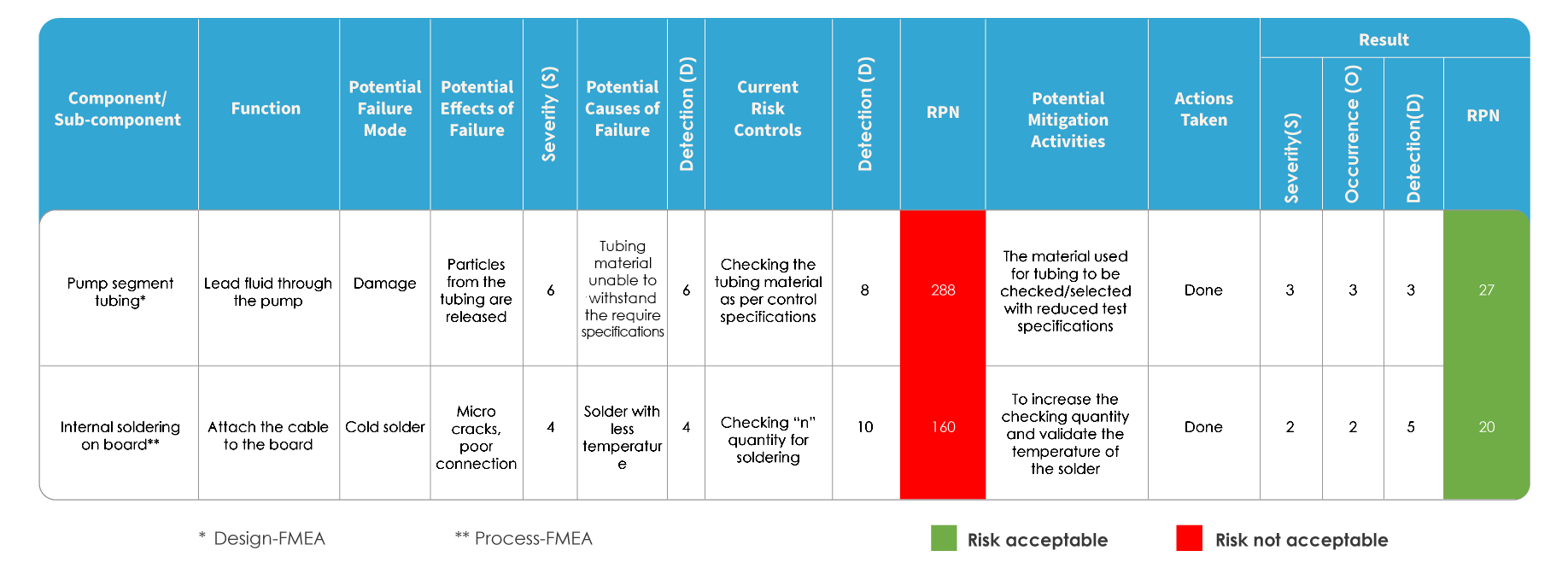
FMEA e ISO 14971 differiscono nel modo in cui il rischio viene valutato. Nella FMEA, il rischio viene valutato identificando le potenziali modalità ed effetti di guasto, seguiti dalla classificazione della gravità dei guasti. Ciascuna delle potenziali cause viene identificata e viene determinata la probabilità di occorrenza. Il rischio viene valutato in base al Numero di Priorità del Rischio (RPN).
Mappatura FMEA
Nel caso della mappatura della gestione del rischio secondo la norma ISO 14971, viene utilizzato uno strumento di tracciabilità noto come Matrice di Tracciabilità dei Pericoli (HTM). Esso include l'analisi, la valutazione, il controllo e la valutazione del rischio residuo.
Matrice di tracciabilità dei pericoli
| Analisi del rischio | Rischio Valutazione. | Controllo del Rischio | ||||||||||||
| ID | Pericolo | Sequenza o Combinazione di Eventi Ragionevolmente Prevedibile | Pericoloso Situazione | Danno | Occorrenza | Gravità | Accettabile? | Opzioni e motivazioni del controllo del rischio | Controllo del Rischio Misure | Rischio Controllo Verifica | Stato | Potenziale di Rischio | Gravità del rischio | Rischio Residuo |
| 1 | Tensione di linea | L'utente utilizza il dispositivo. | L'utente/paziente potrebbe essere esposto alla tensione di rete mentre è a contatto con il dispositivo. | Decesso dell'utente / paziente | 5 | 5 | N | La sicurezza, attraverso una modifica del design e delle misure protettive, può essere messa in atto. | Progettazione secondo IEC 61010. | I test elettrici devono essere eseguiti secondo la norma IEC 61010 | Completato | 2 | 2 | Y |
![]()
Avendo discusso le differenze tra i due, si può concludere che ISO 14971 segue un approccio completo alla gestione del rischio, mentre FMEA è più uno strumento di affidabilità. Tuttavia, i produttori di dispositivi medici dovrebbero conformarsi a ISO 14971 per soddisfare le aspettative delle autorità normative sugli standard di gestione del rischio.
Per saperne di più sui servizi di consulenza per la conformità ISO 14971:2016 e la gestione del rischio, contattate Freyr oggi stesso!









