
Qual è il ruolo della cybersecurity nei dispositivi medici?
Il processo di autorizzazione 510(k) è un percorso normativo utilizzato dalla US FDA per valutare e fornire l'autorizzazione alla distribuzione commerciale dei dispositivi medici. Il processo mira a garantire che i dispositivi medici siano sicuri ed efficaci per l'uso da parte dei pazienti. La US FDA definisce la sicurezza informatica come “[i]l processo di prevenzione dell'accesso non autorizzato, della modifica, dell'uso improprio o della negazione dell'uso, o dell'uso non autorizzato di informazioni che sono memorizzate, accessibili o trasferite da un dispositivo medico a un destinatario esterno.”
I dispositivi medici sono sempre più connessi alle reti e, di conseguenza, sono vulnerabili a minacce informatiche come attacchi hacker, violazioni di dati e attacchi malware. Affrontare la sicurezza informatica in fase di progettazione e sviluppo è fondamentale per garantire che i dispositivi medici dispongano di controlli di sicurezza adeguati. Le minacce e le vulnerabilità non possono essere eliminate, e ridurre i rischi di sicurezza informatica è particolarmente difficile. Se la sicurezza informatica non viene mantenuta correttamente, ciò potrebbe compromettere la funzionalità dei dispositivi, causare la perdita di dati personali o medici e la possibilità che le minacce alla sicurezza si diffondano ad altre reti o dispositivi interconnessi.
Incidenti causati da una cybersecurity compromessa
Gli incidenti di cybersecurity hanno reso inoperativi dispositivi medici e reti ospedaliere, causando l'interruzione dell'erogazione dell'assistenza ai pazienti nelle strutture sanitarie negli US. Tali cyberattacchi e exploit possono anche causare danni ai pazienti a causa di rischi clinici, ad esempio, un ritardo nella diagnosi e/o nel trattamento dei pazienti.
Di seguito sono elencati gli incidenti chiave nel settore sanitario che sottolineano l'importanza della cybersecurity per la sicurezza dei pazienti.
- Nel 2017, l'attacco ransomware WannaCry ha colpito i sistemi ospedalieri e i dispositivi medici a livello globale.
- Nel 2020, un attacco ransomware a un ospedale tedesco ha evidenziato i potenziali ottantatré impatti del ritardo nell'assistenza ai pazienti, poiché l'attacco ha costretto i pazienti a essere dirottati verso un altro ospedale.
Le principali considerazioni sulla sicurezza informatica per l'autorizzazione 510(k)
I seguenti sono i principi generali di cybersecurity per i produttori di dispositivi medici, secondo la guida sulla cybersecurity della FDA US specifica per le presentazioni pre-commercializzazione.
- Regolamento del Sistema Qualità (QSR).: I produttori dovrebbero affrontare le questioni di cybersecurity nella fase di progettazione e sviluppo del dispositivo medico, poiché ciò può portare a una mitigazione più robusta ed efficiente dei rischi per i pazienti. I produttori dovrebbero stabilire input di progettazione relativi alla cybersecurity per il loro dispositivo e un approccio alla vulnerabilità e gestione della cybersecurity come parte della validazione del software e dell'analisi dei rischi richiesta dal 21 CFR 820.30(g).
- Sicurezza della progettazione: I produttori di dispositivi devono assicurarsi che i loro prodotti siano progettati tenendo conto della sicurezza del dispositivo. La US FDA valuterà l'adeguatezza della sicurezza, basandosi sulla capacità del dispositivo di fornire e implementare obiettivi di sicurezza come autenticità, autorizzazione, disponibilità, riservatezza e sicurezza, e aggiornabilità tempestiva in tutta l'architettura del sistema.
- Trasparenza: La mancanza di informazioni sulla sicurezza informatica del dispositivo, come le informazioni necessarie per integrare il dispositivo nell'ambiente di utilizzo, nonché le informazioni necessarie agli utenti per mantenere la sicurezza informatica durante il ciclo di vita del dispositivo, può influire sulla sua sicurezza ed efficacia. Per affrontare queste preoccupazioni, è importante che gli utenti del dispositivo abbiano accesso alle informazioni relative ai controlli di sicurezza informatica, ai potenziali rischi e ad altre informazioni pertinenti.
- Documentazione per la presentazione: La progettazione e la documentazione della cybersecurity del dispositivo dovrebbero essere proporzionate al rischio di cybersecurity del dispositivo. I produttori dovrebbero considerare il sistema più ampio in cui un dispositivo può essere utilizzato.
Figura 1: Sfide e soluzioni comuni di cibersecurity 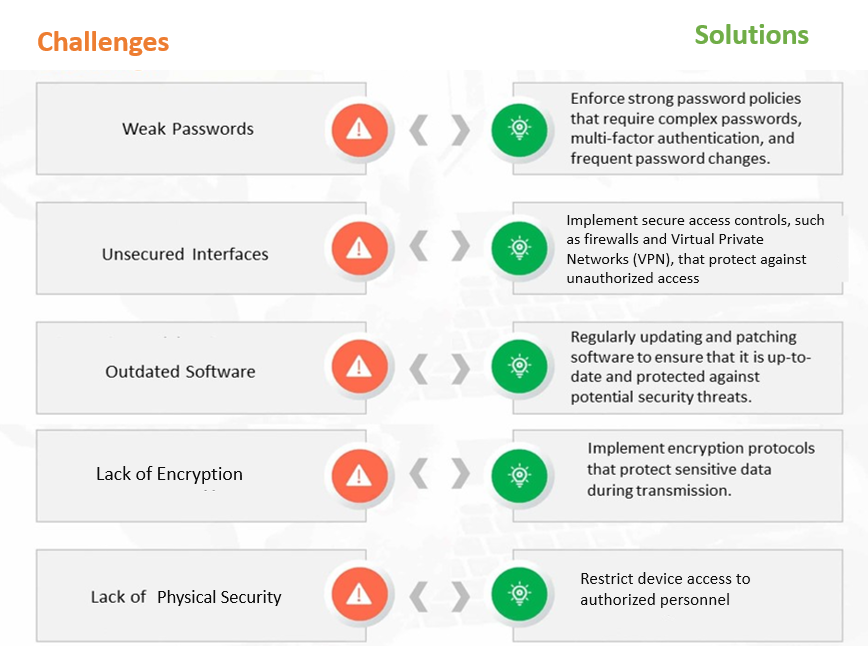
Conclusione
In sintesi, la cybersecurity nei dispositivi medici è cruciale per garantire la sicurezza dei pazienti e prevenire incidenti che potrebbero interrompere l'erogazione dell'assistenza sanitaria. I regolamenti sulla cybersecurity della US FDA sottolineano la necessità per i produttori di affrontare le questioni di cybersecurity durante la progettazione e lo sviluppo dei dispositivi medici e di fornire informazioni trasparenti sui controlli di cybersecurity. Il QSR, la sicurezza della progettazione, la trasparenza e la documentazione di presentazione sono considerazioni chiave per l'autorizzazione 510(k). È anche importante affrontare le comuni sfide di cybersecurity come le vulnerabilità nei componenti di terze parti e gli attacchi ransomware e implementare soluzioni come una solida analisi dei rischi e aggiornamenti software regolari.
Per un processo di autorizzazione 510(k) senza problemi e conforme, contattate i nostri esperti normativi. Rimanete informati! Rimanete conformi!









