
Il Sistema di Gestione della Qualità (SGQ) è una componente essenziale dell'industria dei dispositivi medici, garantendo la sicurezza, l'efficacia e la conformità normativa dei dispositivi medici durante tutto il loro ciclo di vita. Il SGQ è implementato in tutte le fasi del ciclo di vita del dispositivo medico, inclusa la fase di progettazione e sviluppo, per garantire che il dispositivo soddisfi i requisiti normativi e dell'utente e che tutti i potenziali rischi siano identificati e affrontati.
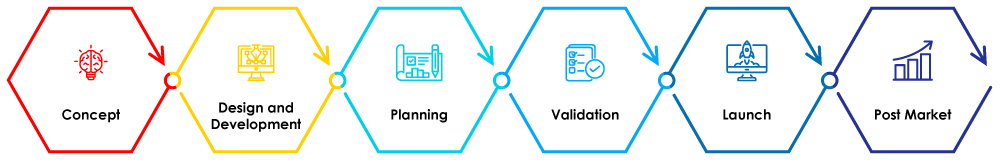
Figura 1 – Fasi del ciclo di vita dei dispositivi medici
In questo blog, discuteremo l'importanza del QMS nella fase di progettazione e sviluppo del ciclo di vita dei dispositivi medici.
Fase di Progettazione e Sviluppo nel Ciclo di Vita del Dispositivo Medico
La fase di progettazione e sviluppo è una delle fasi più critiche nel ciclo di vita di un dispositivo medico. Durante questa fase, viene sviluppato il design del dispositivo e vengono creati i prototipi, seguiti da test di verifica e convalida come parte del ciclo di vita del dispositivo medico.
Per garantire che il dispositivo medico soddisfi i requisiti normativi, la sicurezza, l'efficacia e le aspettative dell'utente, l'implementazione di un Sistema di Gestione della Qualità (QMS) è essenziale nella fase di progettazione e sviluppo del ciclo di vita di un dispositivo medico.
La documentazione è fondamentale durante la fase di progettazione e sviluppo dei dispositivi medici. Il SGQ garantisce che tutta la documentazione relativa alla progettazione e allo sviluppo sia controllata, gestita e documentata.
Il Fascicolo della Storia del Progetto (DHF) è un file/registro importante, contenente tutta la documentazione relativa alla progettazione e allo sviluppo del dispositivo. Il DHF fornisce la prova che la progettazione del dispositivo soddisfa i requisiti normativi.
Il DHF dovrebbe contenere la documentazione relativa agli input di progettazione, agli output di progettazione, alle revisioni di progettazione, alla verifica della progettazione, alla convalida, alle modifiche alla progettazione e alla gestione del rischio. Scopri di più sul DHF qui.
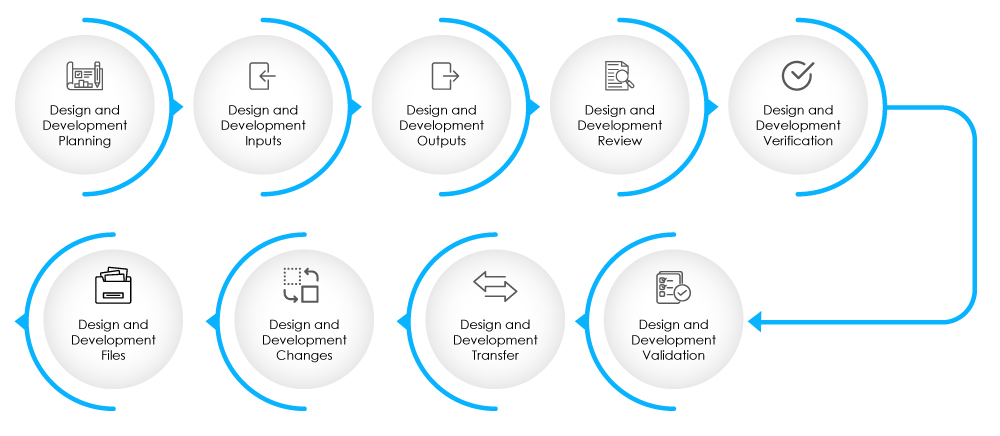
Fig. 2 – Fasi della progettazione e dello sviluppo
Migliori pratiche per la fase di progettazione e sviluppo
- Stabilire un approccio strutturato: Sviluppare un approccio strutturato allo sviluppo e alla gestione del DHF che sia adattato alle esigenze specifiche della vostra organizzazione. Questo approccio dovrebbe includere linee guida chiare, procedure e flussi di lavoro per lo sviluppo e la gestione del DHF.
- Definire e Documentare gli Input di Progettazione: Definire e documentare chiaramente gli input di progettazione, inclusi i requisiti e le specifiche per il dispositivo. Questo può aiutare a garantire che il DHF sia completo ed esaustivo.
- Gestire le Modifiche di Progettazione: Implementare un solido processo di gestione delle modifiche che includa procedure per documentare, valutare e approvare le modifiche di progettazione. Ciò può aiutare a garantire che le modifiche siano adeguatamente documentate e valutate per il loro impatto sulla sicurezza e sull'efficacia del dispositivo.
- Garantire la tracciabilità: Sviluppare una matrice di tracciabilità che colleghi gli input di progettazione agli output di progettazione e assicurarsi che tutte le attività di progettazione e sviluppo siano adeguatamente documentate e registrate. Ciò può contribuire a garantire che il DHF sia tracciabile e che il processo decisionale sia ben documentato.
- Bilanciare Innovazione e Conformità: Sviluppare una cultura dell'innovazione garantendo il rispetto dei requisiti di conformità relativi al DHF, come i controlli di progettazione e la gestione del rischio. Ciò può essere raggiunto sviluppando procedure e flussi di lavoro che facilitino l'innovazione, assicurando al contempo il rispetto dei requisiti normativi.
- Implementare il Controllo dei Documenti: Implementare procedure di controllo dei documenti che garantiscano che i documenti DHF siano adeguatamente controllati, con controllo di versione e accessibili al personale autorizzato. Ciò può contribuire a garantire che i documenti DHF siano sicuri e che le modifiche siano correttamente documentate e approvate.
- Formare il team: Assicurarsi che il team responsabile dello sviluppo e della gestione del DHF sia adeguatamente formato sui requisiti del DHF e abbia le competenze tecniche per sviluppare il prodotto. Ciò può essere raggiunto attraverso sessioni di formazione regolari, mentoring e l'assunzione di professionisti esperti con le competenze e l'esperienza necessarie.
Seguendo queste migliori pratiche, l'industria dei dispositivi medici può garantire la conformità ai requisiti normativi, promuovere la sicurezza e l'efficacia dei propri prodotti e mantenere il proprio vantaggio competitivo sul mercato.
In conclusione, l'implementazione di un QMS fin dalla fase di progettazione e sviluppo è fondamentale per il successo nel settore dei dispositivi medici altamente regolamentato. Mantenendo registrazioni sistematiche e soddisfacendo i requisiti normativi, il settore dei dispositivi medici può garantire la fornitura di prodotti di alta qualità e il mantenimento della soddisfazione del cliente.
In Freyr, offriamo servizi QMS per aiutare l'industria dei dispositivi medici a soddisfare i requisiti normativi in tutte le fasi del ciclo di vita del dispositivo medico. Contatta i nostri esperti QMS e normativi per saperne di più.









