
¿Cuál es el papel de la ciberseguridad en los Dispositivos Médicos?
El proceso de autorización 510(k) es una vía reglamentaria utilizada por la Administración de Alimentos y Medicamentos de los US (US FDA) para evaluar y otorgar la autorización para la distribución comercial de Dispositivos Médicos. El proceso tiene como objetivo garantizar que los Dispositivos Médicos sean seguros y eficaces para el uso de los pacientes. La US FDA define la ciberseguridad como «[e]l proceso de prevenir el acceso no autorizado, la modificación, el uso indebido o la denegación de uso, o el uso no autorizado de la información que se almacena, accede o transfiere desde un Dispositivo Médico a un destinatario externo».
Los Dispositivos Médicos están cada vez más conectados a redes y, por lo tanto, son vulnerables a amenazas de ciberseguridad como el hackeo, las filtraciones de datos y los ataques de malware. Abordar la ciberseguridad en la etapa de diseño y desarrollo es fundamental para garantizar que los Dispositivos Médicos cuenten con los controles de seguridad adecuados. Las amenazas y vulnerabilidades no pueden eliminarse, y reducir los riesgos de ciberseguridad es especialmente desafiante. Si la ciberseguridad no se mantiene adecuadamente, podría llevar a una funcionalidad comprometida de los dispositivos, la pérdida de datos personales o médicos, y la posibilidad de que las amenazas de seguridad se propaguen a otras redes o dispositivos interconectados.
Incidentes causados por ciberseguridad comprometida
Los incidentes de ciberseguridad han provocado que los dispositivos médicos y las redes hospitalarias queden inoperativos, interrumpiendo la prestación de atención al paciente en los centros de salud de US. Estos ciberataques y exploits también pueden causar daño a los pacientes debido a riesgos clínicos, como un retraso en el diagnóstico y/o tratamiento de los pacientes.
A continuación se enumeran los incidentes clave en el sector sanitario que resaltan la importancia de la ciberseguridad para la seguridad del paciente.
- En 2017, el ataque de ransomware WannaCry afectó a los sistemas hospitalarios y a los Dispositivos Médicos en todo el mundo.
- En 2020, un ataque de ransomware a un hospital alemán puso de manifiesto los posibles ochenta y tres (83) impactos de la atención al paciente retrasada, ya que el ataque obligó a desviar a los pacientes a otro hospital.
Las consideraciones clave de ciberseguridad para la autorización 510(k)
A continuación, se presentan los principios generales de ciberseguridad para los fabricantes de Dispositivos Médicos, según la guía de ciberseguridad de la US FDA específica para las presentaciones previas a la comercialización.
- Reglamento del Sistema de Calidad (QSR).: Los fabricantes deben abordar los problemas de ciberseguridad en la etapa de diseño y desarrollo del dispositivo médico, ya que esto puede resultar en una mitigación más robusta y eficiente de los riesgos para el paciente. Los fabricantes deben establecer entradas de diseño relacionadas con la ciberseguridad para su dispositivo y un enfoque de gestión y vulnerabilidad de la ciberseguridad como parte de la validación de software y el análisis de riesgos que requiere 21 CFR 820.30(g).
- Seguridad del diseño: Los fabricantes de dispositivos deben asegurarse de que sus productos estén diseñados teniendo en cuenta la seguridad del dispositivo. La FDA de US evaluará la idoneidad de la seguridad, basándose en la capacidad del dispositivo para proporcionar e implementar objetivos de seguridad como autenticidad, autorización, disponibilidad, confidencialidad y seguridad, y capacidad de actualización oportuna en toda la arquitectura del sistema.
- Transparencia: La falta de información sobre ciberseguridad en el dispositivo, como la necesaria para integrarlo en el entorno de uso, así como la información que los usuarios necesitan para mantener la ciberseguridad durante todo el ciclo de vida del dispositivo, puede afectar su seguridad y eficacia. Para abordar estas preocupaciones, es importante que los usuarios del dispositivo tengan acceso a la información relativa a los controles de ciberseguridad, los riesgos potenciales y otra información relevante.
- Documentación de Presentación: Se espera que el diseño y la documentación de ciberseguridad de los dispositivos se adapten al riesgo de ciberseguridad de un dispositivo. Los fabricantes deben considerar el sistema más amplio en el que se puede utilizar un dispositivo.
Figura 1: Desafíos y soluciones comunes de ciberseguridad 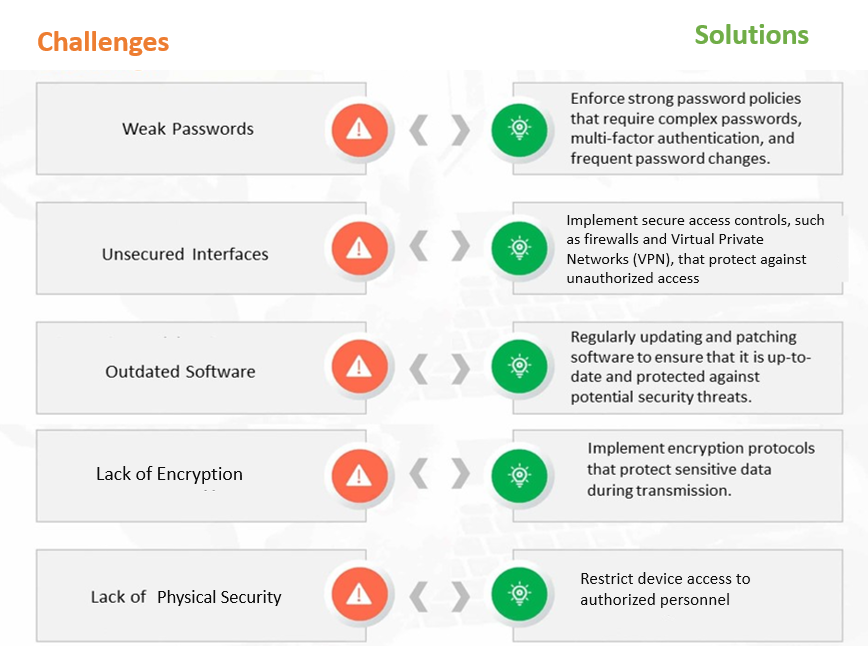
Conclusión
En resumen, la ciberseguridad en Dispositivos Médicos es crucial para garantizar la seguridad del paciente y prevenir incidentes que puedan interrumpir la prestación de atención médica. Las regulaciones de ciberseguridad de la US FDA enfatizan la necesidad de que los fabricantes aborden los problemas de ciberseguridad durante el diseño y desarrollo de Dispositivos Médicos y proporcionen información transparente sobre los controles de ciberseguridad. El QSR, la seguridad del diseño, la transparencia y la documentación de presentación son consideraciones clave para la autorización 510(k). También es importante abordar los desafíos comunes de ciberseguridad, como las vulnerabilidades en componentes de terceros y los ataques de ransomware, e implementar soluciones como un análisis de riesgos robusto y actualizaciones regulares de software.
Para experimentar un proceso de autorización 510(k) sin complicaciones y conforme a la normativa, póngase en contacto con nuestros expertos reglamentarios. ¡Manténgase informado! ¡Manténgase conforme!









