Quando a pandemia de COVID-19 foi reconhecida pela primeira vez como uma crise de saúde global em 2020, as Autoridades de Saúde (HAs) globais tomaram medidas inovadoras para lidar com ela da melhor forma possível. Da mesma forma, as empresas farmacêuticas desenvolveram várias vacinas/medicamentos em benefício do público. No entanto, o registo dos produtos revelou-se bastante desafiador. Para simplificar o registo, mantendo a sua segurança, qualidade e eficácia, as HAs concederam Autorizações de Uso de Emergência (EUAs) a algumas vacinas e produtos relevantes.
A questão pode surgir sobre como as Autoridades de Saúde conseguiram garantir que os benefícios dos referidos produtos superavam os riscos. A resposta é a adoção das melhores práticas de farmacovigilância (FV).
O que é Farmacovigilância?
A PV é definida como um conjunto de atividades científicas relacionadas com a deteção, avaliação, compreensão e prevenção de efeitos adversos e quaisquer outros problemas relacionados com medicamentos. A seguir, apresentamos uma explicação figurativa de como a PV funciona e do processo envolvido.
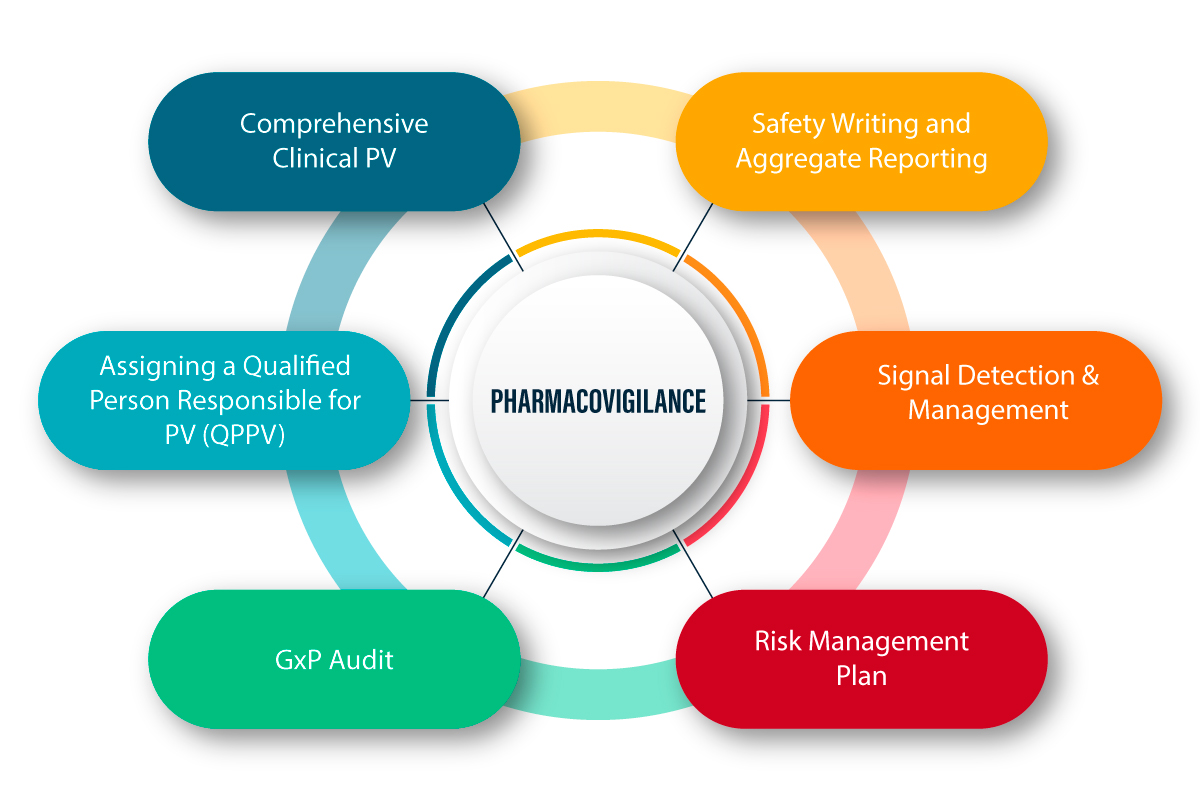
PV na Pandemia de COVID-19
Quando a pandemia de COVID-19 começou a espalhar-se pelo mundo, vacinas e medicamentos relevantes tiveram de ser introduzidos no mercado num período limitado, mantendo os padrões de qualidade exigidos. Nesses cenários, existiam menos indivíduos disponíveis para ensaios clínicos durante a fase de desenvolvimento de medicamentos/vacinas, e o processo teve de ser concluído mais rapidamente do que o normal. Isso poderia levar ao surgimento de certos efeitos adversos na fase pós-aprovação.
Assim, o equilíbrio benefício-risco das vacinas/Medicamentos foi considerado primordial. Com a comunicação atempada de reações adversas e efeitos secundários prejudiciais, a eficácia dos produtos foi mantida em tempo real.
Algumas das principais atividades de farmacovigilância que ajudaram a manter a segurança, qualidade e eficácia dos referidos produtos durante a pandemia são as seguintes:
- Adoção de um bom Plano de Gestão de Risco
- Avaliação de risco com a ajuda de Relatórios Periódicos de Segurança (PSURs)
- Compilação dos dados de exposição
- Estudos de Segurança Pós-Autorização (PASS)
- Notificação espontânea de reações adversas suspeitas
- Gestão eficaz de sinais
Farmacovigilância (PV) em Assuntos Regulamentares (RA)
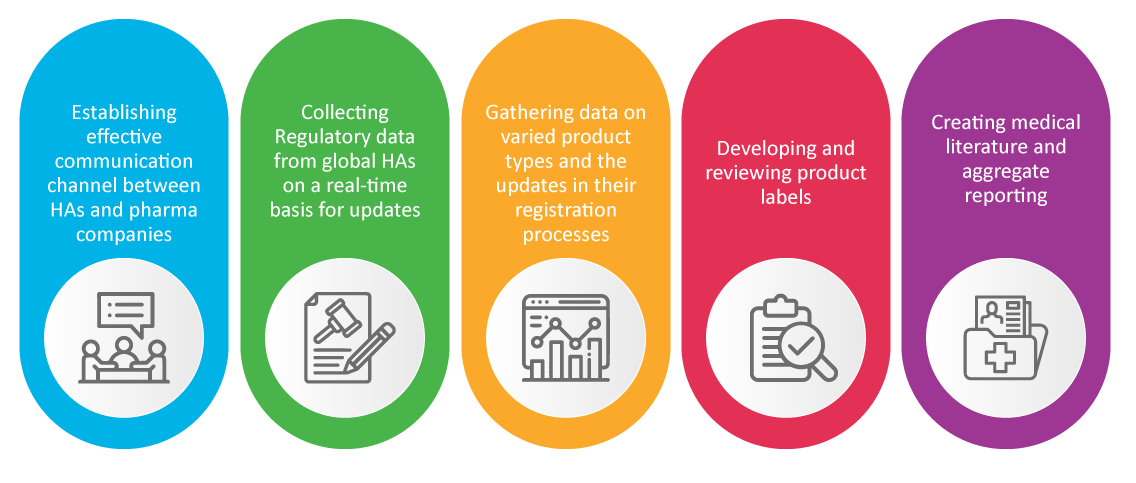
É bem conhecido que a equipa de Assuntos Regulamentares de uma empresa farmacêutica é responsável pela segurança e aprovação de novos produtos. Os especialistas em RA tratam das atividades de farmacovigilância que se revelaram cruciais durante a pandemia, tais como:
Conclusão
Para concluir, a Farmacovigilância ajuda a monitorizar e a reportar a segurança de um medicamento. Com Relatórios de Casos Individuais de Segurança (ICSR) personalizados, torna-se mais fácil para os fabricantes/patrocinadores cumprirem os respetivos regulamentos das Autoridades de Saúde globais. Procura apoio regulamentar para a preparação de ICSR? Consulte um especialista regulamentar comprovado para conformidade. Contacte a Freyr.










