O SmPC ou Resumo das Características do Medicamento é um documento legal que faz parte da Autorização de Introdução no Mercado de cada medicamento. O documento serve como base de informação sobre o uso de medicamentos para profissionais de saúde. A informação incluída no SmPC é atualizada regularmente de acordo com o surgimento das informações mais recentes. O SmPC contém mais informações do que um Folheto Informativo. As informações do SmPC podem ser encontradas através das seguintes fontes:
- Websites das Autoridades de Saúde; como a Agência Europeia de Medicamentos (EMA)
- Dicionários de medicamentos
O que consiste um SmPC?
- Informação relacionada com a utilização do medicamento
- Informação qualitativa e quantitativa sobre os benefícios e riscos dos medicamentos
- Informação sobre a dosagem
- Método de administração
- Informação farmacológica
- Informação de cuidados individuais
Estrutura de um SmPC
A estrutura do SmPC é definida pela legislação farmacêutica europeia. A informação incluída no SmPC deve ser específica do produto e pode ser referenciada de forma cruzada para evitar qualquer redundância. Deve ser documentada numa linguagem clara e não deve levar a qualquer ambiguidade. O SmPC está dividido em 6 secções principais:
- Nome do produto
- Composição
- Forma farmacêutica
- Dados clínicos – Inclui indicações terapêuticas, recomendações de dosagem e informações de segurança
- Propriedades farmacológicas – Têm em consideração as indicações terapêuticas dos elementos clínicos e as suas potenciais reações adversas a medicamentos
- Dados farmacêuticos – Inclui informações de regulamentação relacionadas com o medicamento
De acordo com a estrutura da EMA, um SmPC pode ser representado da seguinte forma:
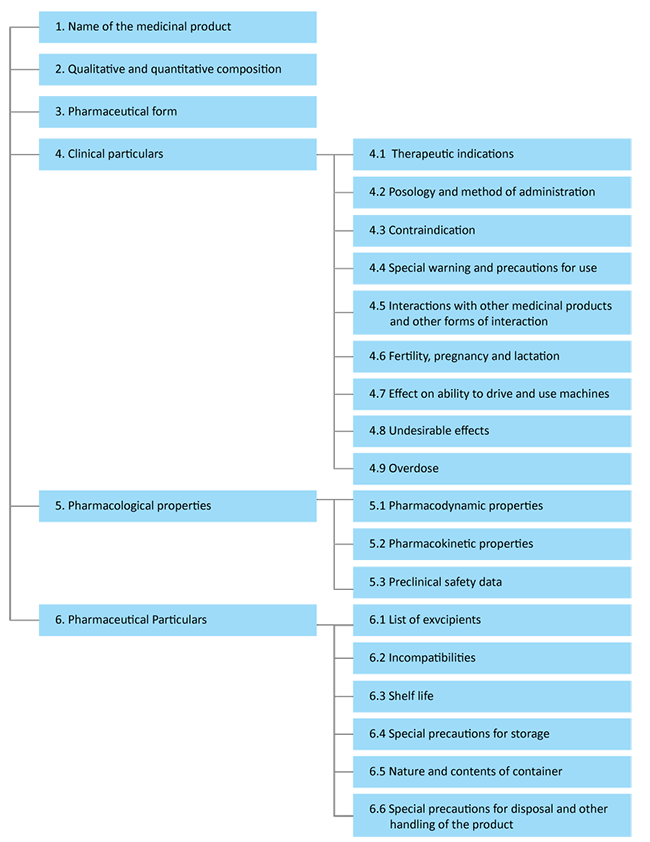
Referência: EMA
Que Informação é Excluída de um SmPC?
- Informação disponível nos relatórios públicos de avaliação (detalhes de desenvolvimento científico)
- Informação sobre indicações não aprovadas
- Questões com falta de dados
- Aconselhamento geral sobre condições farmacológicas
Manter um SmPC é importante para o ciclo de vida de qualquer medicamento, uma vez que faz parte da sua autorização de introdução no mercado. Portanto, a elaboração de um SmPC em conformidade é altamente recomendada. Procura assistência regulamentar especializada para desenvolver um SmPC? Contacte a Freyr @ sales@freyrsolutions.com.