
A rotulagem de produtos farmacêuticos é um dos aspetos mais rigorosamente fiscalizados no âmbito da conformidade regulamentar. Um pequeno erro pode ter consequências significativas tanto para a segurança dos doentes como para a reputação da empresa. Considere estas conclusões:
- 20 % das empresas farmacêuticas e de dispositivos médicos comunicam mensalmente problemas de controlo de qualidade relacionados com a rotulagem.
- Estudos revelaram que 40 % dos rótulos de medicamentos em determinados mercados não cumprem os requisitos regulamentares, apresentando frequentemente lacunas em informações essenciais de segurança.
- A nível mundial, 35 a 40 % dos recalls de produtos devem-se a erros de embalagem e rotulagem, de acordo com os resumosFDA US .
- Nas auditorias regulamentares, mais de 50 % das constatações dizem respeito à documentação de rotulagem, desde as informações de prescrição até artwork às traduções.
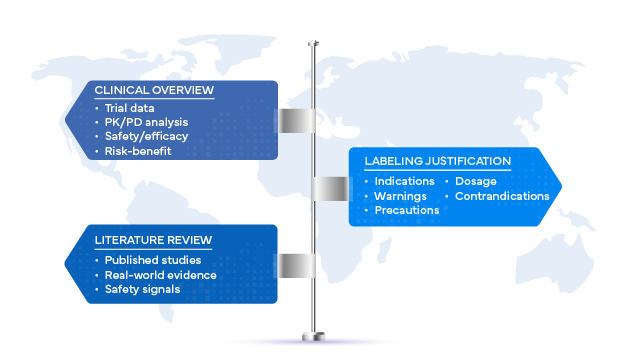
Estas estatísticas sublinham uma realidade: as decisões relativas à classificação devem ser precisas, baseadas em dados concretos e plenamente justificadas. A base dessa justificação reside na análise clínica e nas revisões sistemáticas da literatura.
O papel da visão geral clínica
A síntese clínica, tal como definida pela ICH (R2), é mais do que uma formalidade regulamentar. Trata-se de uma análise estruturada e crítica de todos os dados clínicos disponíveis que sustentam o desenvolvimento de um produto. Quando associada à rotulagem, desempenha um papel decisivo para garantir que a segurança, a eficácia e o perfil risco-benefício sejam claramente representados nas informações de prescrição.
As principais contribuições da síntese clínica para a rotulagem incluem:
- Estabelecer uma ligação direta entre os resultados dos ensaios clínicos e as alegações do produto
- Justificar a inclusão de advertências, precauções e contraindicações
- Garantir a coerência entre as conclusões em matéria de segurança e as decisões relativas à rotulagem
- Apresentar às entidades reguladoras uma análise transparente e baseada em dados concretos dos benefícios e riscos
Por exemplo, se os dados do ensaio revelarem um evento adverso estatisticamente significativo num subgrupo, a análise clínica justifica a inclusão de advertências específicas para esse subgrupo na bula.
Por que as revisões da literatura são essenciais
Embora os dados dos ensaios clínicos constituam a base para a justificação da rotulagem, as revisões sistemáticas da literatura ampliam a base de evidências ao incorporar resultados que vão além dos estudos realizados pelos patrocinadores. Estas revisões sintetizam publicações submetidas a revisão por pares, evidências do mundo real e dados de segurança pós-comercialização, a fim de proporcionar às entidades reguladoras uma perspetiva mais ampla e imparcial.
Uma revisão bibliográfica sólida ajuda as empresas a:
- Validar as alegações de segurança através de fontes independentes
- Detectar sinais de alerta precoce ou reações adversas que não se manifestaram nos ensaios clínicos
- Resultados comparativos com produtos da concorrência ou efeitos a nível de toda a categoria
- Harmonizar as fichas técnicas de referência (CCDS) com os documentos de produtos locais (LPD) específicos de cada região
Por exemplo, estudos publicados ou meta-análises podem revelar efeitos adversos raros, mas graves, reforçando a justificação para incluir ou atualizar uma precaução no rótulo.
Expectativas regulamentares relativas à justificação da rotulagem
As autoridades sanitárias mundiais, incluindo aFDA US , EMA, MHRA e PMDA, esperam que as justificações dos rótulos reflitam rigor científico, transparência e coerência. Os revisores regulamentares avaliam frequentemente:
- Hierarquia de evidências: dar prioridade aos dados de ensaios clínicos aleatórios controlados, mas tendo em conta estudos observacionais ou de situação real relevantes
- Coerência entre documentos: Garantir que a visão geral clínica, o Resumo de Segurança Clínica (SCS) e o rótulo proposto estejam em consonância
- Fundamentação clara: explicar por que razão cada indicação, recomendação de dosagem ou advertência é incluída (ou excluída)
A falta de uma base de evidências clara para a rotulagem pode resultar em consultas por parte das autoridades reguladoras, prazos de análise prolongados ou mesmo na rejeição.
Melhores práticas para justificar decisões relativas à rotulagem
As empresas farmacêuticas podem reforçar os seus pedidos de rotulagem adotando estas boas práticas:
- Colaboração interdepartamental: Envolver as equipas clínicas, de segurança e regulamentares para uma interpretação holística
- Aproveite a tecnologia: utilize ferramentas baseadas em IA para revisões da literatura, a fim de acelerar a triagem e a extração
- Manter registos documentais: Registar os fundamentos para a inclusão/exclusão nos estudos, de modo a cumprir os requisitos das auditorias regulamentares
- Comparar com os padrões globais: alinhar-se com os produtos da concorrência e com as diretrizes em constante evolução para colmatar as lacunas de conformidade
- Atualizar continuamente: Incorporar a literatura mais recente e os dados de farmacovigilância nas estratégias de rotulagem em curso
Conclusão
Com o escrutínio regulatório a atingir níveis sem precedentes e os custos da não conformidade a aumentar, as empresas não podem dar-se ao luxo de basear-se em suposições ao elaborar os rótulos dos produtos. Uma análise clínica sólida, combinada com revisões exaustivas da literatura, garante que todas as alegações sejam apoiadas por evidências científicas transparentes.
Na Freyr Solutions, ajudamos as empresas farmacêuticas globais a lidar com esta complexidade. end-to-end nossa end-to-end em rotulagem regulamentar, documentação clínica e estratégias de conformidade garante que as suas decisões em matéria de rotulagem sejam cientificamente fundamentadas, estejam em conformidade com os requisitos regulamentares e sejam harmonizadas a nível global.
Estabeleça hoje mesmo uma parceria com a Freyr para reforçar a sua estratégia de rotulagem com justificações baseadas em dados científicos, nas quais as entidades reguladoras confiam e dos quais os doentes dependem.










