
Os ensaios cegos são a pedra angular da integridade dos ensaios clínicos, eliminando o enviesamento e garantindo uma avaliação objetiva dos produtos em investigação. No entanto, por trás do rigor científico reside uma componente criativa fundamental: os rótulos das embalagens para ensaios clínicos. Para artwork regulatório, conceber rótulos para ensaios cegos é um exercício de equilíbrio entre conformidade, confidencialidade e clareza.
Na Freyr Solutions, somos especializados em artwork em conformidade com os regulamentos e pronto para auditoria, artwork ensaios clínicos globais. Neste blogue, exploramos como artwork das embalagens para ensaios clínicos artwork ser adaptado para satisfazer as exigências específicas dos estudos cegos.
Por que razão Artwork nos estudos cegos
A conceção de rótulos de embalagem para estudos cegos (normalmente em ensaios clínicos) envolve processos específicos para manter o cegamento e garantir o cumprimento dos requisitos regulamentares e específicos do ensaio.
Ao contrário dos produtos comerciais, o artwork estudos cegos deve ocultar a identidade do produto, mas fornecer informações claras e aprovadas pelas autoridades reguladoras aos utilizadores finais, tais como investigadores, farmacêuticos e doentes. Qualquer discrepância — seja na cor, na forma, na tipografia ou no conteúdo da rotulagem — pode, involuntariamente, quebrar o cegamento do estudo.
Artwork estudos cegos devem, por conseguinte, ter objetivos-chave:
- Garantir a integridade cega: O rótulo não deve revelar qualquer informação que possa identificar o tratamento. Deve ser mantida a consistência visual em todos os braços do estudo.
- Usabilidade: Garantir uma utilização segura e correta (por exemplo, submissão adequada submissão do pessoal do local). Evitar a diferenciação do produto através de elementos de design.
- Gerir dados variáveis: Os principais elementos de dados variáveis — tais como códigos de aleatorização, datas de validade, números de kit, identificações de doentes e informações específicas de cada consulta — devem estar disponíveis.
- Conformidade regulamentar: Cumprir os regulamentos globais/regionais relativos aos ensaios clínicos
- Rastreabilidade: Assegurar uma ligação clara ao ensaio clínico e ao doente, sem revelar o tipo de produto. Deve estar sujeita a controlo de versões e permitir a auditoria.
Processo de criação de rótulos de embalagem para ensaios clínicos cegos
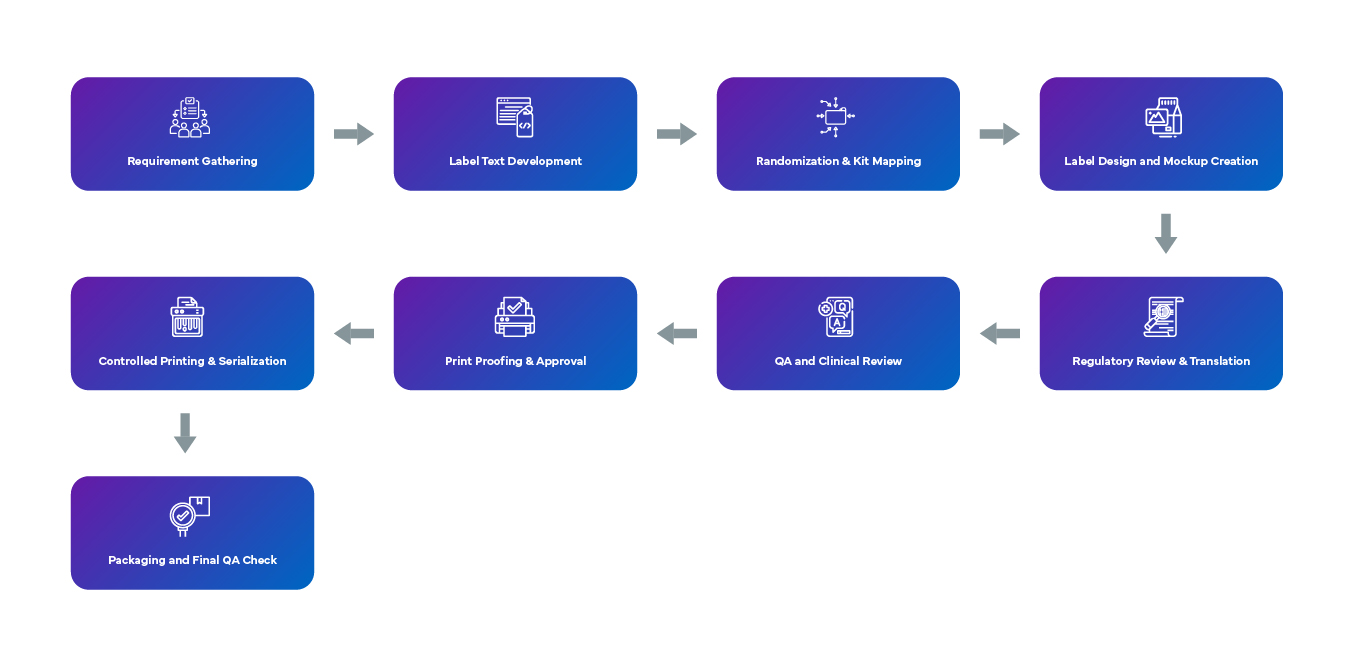
O processo de conceção de rotulagem cega começa com a recolha de requisitos através da análise do protocolo e do contributo das partes interessadas, garantindo a conformidade com os regulamentos específicos de cada país. O texto neutro do rótulo é elaborado utilizando termos como «Medicamento do estudo» e inclui informações essenciais, tais como números do ensaio, datas de validade e advertências, evitando simultaneamente identificadores que possam revelar o tratamento. A randomização e o mapeamento dos kits são tratados de forma segura, com rótulos concebidos para manter o cegamento, recorrendo frequentemente a códigos de barras. São criadas maquetes de design tendo em conta o tamanho do recipiente, as necessidades multilingues e os requisitos de sobreposição. As revisões regulamentares e de tradução garantem a conformidade global. As equipas QA Clínicas verificam o alinhamento com o protocolo, enquanto as provas de rótulo são submetidas a verificações eletrónicas e aprovações formais. submissão de rótulos — seja primária, secundária ou sobre-rotulagem — tem em conta as restrições ambientais. A impressão controlada, frequentemente just-in-time, garante a rastreabilidade serializada e a embalagem final é concluída sob QA para confirmar a precisão do rótulo, a adesão e a integridade do cegamento.
Artwork essenciais sobre Artwork para rótulos de estudos cegos
| Artwork | Requisitos de desenho em estudos cegos | Artwork de Freyr |
| Esquema de cores | Evita a diferenciação por cores que poderia indicar os grupos de tratamento | Paletas de cores uniformes em todas as secções; de preferência em tons de cinza ou neutros |
| Tipos de letra e tipografia | Estilo e tamanho de letra uniformes em todas as variantes, para evitar pistas visíveis | As diretrizes tipográficas predefinidas são aplicadas de forma uniforme em todos os designs das etiquetas |
| Disposição e hierarquia das etiquetas | Posicionamento de texto e imagens de acordo com as diretrizes técnicas | Layouts de design baseados em modelos para garantir a uniformidade |
| Rotulagem de placebo vs. rotulagem ativa | Não deve apresentar quaisquer diferenças visuais | Utilize modelos de etiquetas idênticos; apenas os campos variáveis diferem através dos dados codificados. |
| Códigos de aleatorização/rastreamento | Deve estar presente, mas não deve ser interpretável pelo utilizador final | Capacidade de gerar qualquer tipo de código de barras. |
| Gestão linguística | O conteúdo multilingue não deve introduzir distorções no layout | Os blocos de texto foram concebidos com um layout simétrico. |
| Campos de dados dinâmicos | Dados como o lote, a data de validade e o ID do componente variam de embalagem para embalagem | Campos reservados ou conforme acordado pela equipa de design para a disposição |
| Material e formato da etiqueta | Deve permitir o cegamento e o descegamento, conforme as necessidades do estudo | Utilização de etiquetas em livreto, etiquetas autocolantes ou sobreetiquetas, conforme necessário |
| Controlo de versões e aprovação | Os rótulos são atualizados frequentemente devido a alterações nos protocolos | artwork centralizada artwork com controlo de versões das etiquetas e gestão de aprovações |
Referências de organismos reguladores para a rotulagem de ensaios clínicos
Região | Organismo Regulador | Referência à diretriz |
| UE | EMA | Anexo VI do Regulamento (UE) n.º 536/2014 |
| US | FDA | 21 CFR Parte 312.6 |
| REINO UNIDO | MHRA | Guia de Boas Práticas Clínicas |
| Canadá | Health Canada | Documento de orientação para patrocinadores de ensaios clínicos |
Erros comuns na Artwork de estudos cegos Artwork e como evitá-los)
✗ Utilização de etiquetas com dimensões diferentes para o grupo ativo e o grupo placebo
✓ Padronizar o tamanho e a forma em todos os grupos
✗ A disposição dos idiomas varia de país para país
✓ Utilize blocos de idiomas espelhados com formatação consistente
✗ IDs de lote/produto visíveis na artwork do produto
✓ Utilizar dados codificados e códigos de barras para ocultar identificadores visíveis
Por que razão deve colaborar com a Freyr na Artwork para estudos cegos?
- Experiência em conceção de rótulos cegos para ensaios clínicos globais
- Disponibilidade de informações regulatórias nas regiões dos US, da UE, do Reino Unido, do Canadá e da Ásia-Pacífico
- Utilização da ferramenta Artwork , se necessário. A ferramenta pode ser personalizada para cumprir os requisitos dos ensaios clínicos.
- Ficheiros com controlo de versões, em conformidade e prontos para auditoria
- Capacidade multilingue e revisão técnica de rótulos para qualquer país ou região










