
A partir de 31 de janeiro de 2022, o novo regulamento farmacêutico da União Europeia (UE) para o Regulamento de Ensaios Clínicos (CTR) tornou-se obrigatório, revogando a Diretiva de Ensaios Clínicos 2001/20/CE. O regulamento harmoniza os protocolos para a avaliação e supervisão de ensaios clínicos em toda a UE. As diretrizes foram revistas para promover uma abordagem uniforme à investigação clínica, enfatizando a segurança dos participantes nos ensaios clínicos e o aumento da divulgação pública.
O regulamento estabelece um novo sistema de avaliação em duas partes para todos os ensaios clínicos da UE. A Parte I consiste numa avaliação científica da documentação essencial do ensaio clínico, e a Parte II consiste numa avaliação ética da documentação a nível nacional. Após esta avaliação em duas partes, cada Estado-Membro tomará uma decisão unificada sobre o ensaio e notificará o promotor através do Sistema de Informação sobre Ensaios Clínicos.
Prazos de Transição para Novos Candidatos
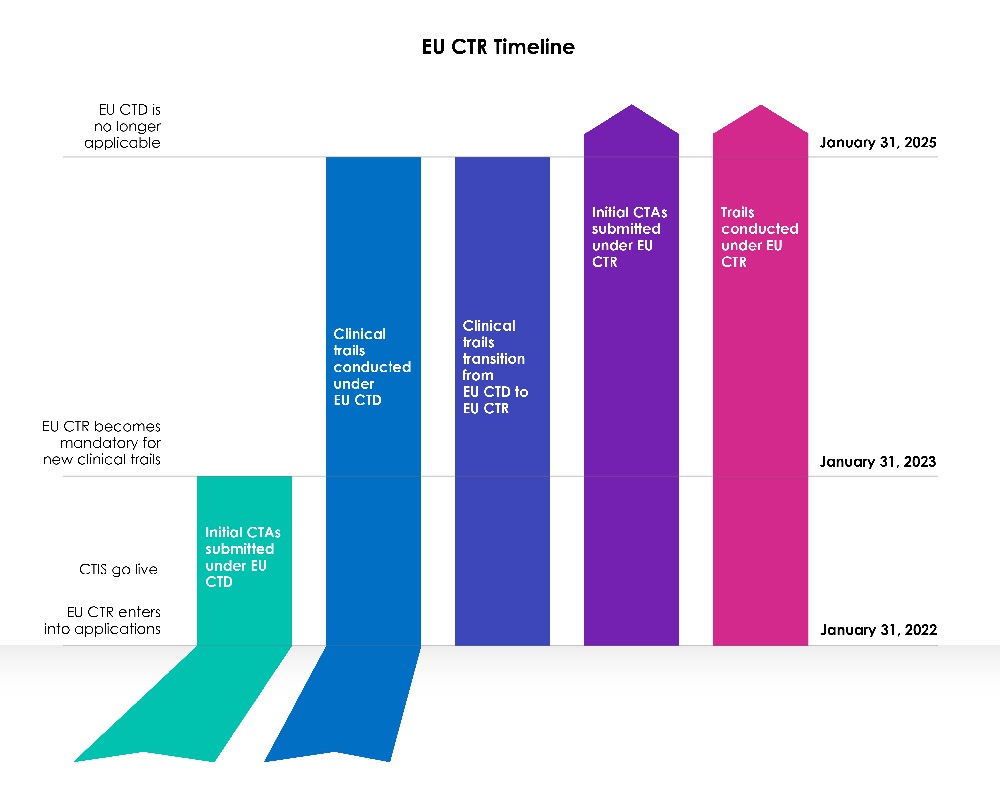
Uma fase de transição de três (03) anos começou com a data de entrada em funcionamento do CTIS da UE.
Ano 1 (31 de janeiro de 2022 a 30 de janeiro de 2023):
A Diretiva de Ensaios Clínicos da União Europeia (UE) 2001/20/CE (EU-CTD) regeu os ensaios clínicos na UE desde 2004. Esforçou-se por padronizar as regras e melhorou significativamente a segurança dos pacientes nos ensaios clínicos. No entanto, na prática, criou consequências não intencionais. Durante o primeiro ano, após a implementação do CTIS, os promotores puderam escolher se apresentavam uma nova submissão de Ensaio Clínico (CTA) sob o Sistema de Informação de Ensaios Clínicos (CTIS) ao abrigo da Diretiva de Ensaios Clínicos (CTD: Diretiva 2001/20/CE), ou se utilizavam o CTIS de acordo com a legislação atual, o Regulamento de Ensaios Clínicos (UE) N.º 536/2014.
Ambas as ideias eram viáveis, e os patrocinadores tiveram a oportunidade de escolher qual legislação seguir.
Os membros estavam prontos para utilizar o Clinical Trial Information System (CTIS) e aceitaram submissões ao abrigo da nova legislação, o Regulamento de Ensaios Clínicos (EU CTR), no primeiro dia de funcionamento do CTIS.
Anos 2 e 3 (31 de janeiro de 2023 a 31 de janeiro de 2025):
A partir de 31 de janeiro de 2023, todas as novas submissões de ensaios clínicos (CT) devem ser submetidas através do CTIS ao abrigo da nova legislação (CTR).
Novas submissões de ensaios clínicos (CT) não são permitidas no EudraCT sob a Diretiva de Ensaios Clínicos (CTD). A Diretiva de Ensaios Clínicos da UE já não permite a admissão de novos Member States após 31 de janeiro de 2023. Os ensaios realizados sob a CTD devem primeiro ser transicionados, após o que uma submissão adicional relativa a um Member State pode ser apresentada via CTIS da UE.
Para Requerentes Existentes
As submissões de ensaios clínicos apresentadas antes de 30 de janeiro de 2023, ao abrigo da legislação antiga (CTD) utilizando o EudraCT, serão permitidas até à sua conclusão ao abrigo dessa Diretiva ((CTD: Diretiva 2001/20/EC), até 30 de janeiro de 2025. Os procedimentos permanecerão inalterados, e os promotores poderão apresentar modificações significativas e avisos de fim de ensaio, conforme exigido pelo regulamento. O EudraCT permanecerá ativo durante o período de transição para permitir que estes ensaios continuem.
É, no entanto, importante notar que as submissões de transição podem ser submetidas a qualquer momento durante o período de transição de três (03) anos, e os promotores são encorajados a concluir o processo suficientemente cedo no período de transição para garantir a continuidade dos ensaios clínicos na UE para além de 30 de janeiro de 2025, considerando os feriados legais e a paragem de duas (02) semanas no inverno.
Ensaios Não Transferíveis
- Os ensaios que já foram concluídos ou que serão concluídos pouco antes do fim do período de transição da UE/EEA não devem ser objeto de transição.
- Se uma notificação de fim de ensaio tiver sido concluída em todos os países membros da UE/EEA, mas o fim global do ensaio ainda não tiver sido notificado, o estudo não deve ser transicionado. Ao abrigo da Diretiva, o fim global do ensaio e os resultados resumidos do ensaio devem ser publicados via EudraCT.
- Os ensaios que começaram antes da implementação da Diretiva 2001/20/CE não beneficiam de tal procedimento de transição. Se forem intervencionais e tiverem de continuar a operar após o fim da fase de transição do CTR, uma nova submissão de CT deve ser emitida ao abrigo do CTR.
- Ensaios pediátricos realizados fora da UE/EEA, mas para os quais foi atribuído um número EudraCT, também não devem ser convertidos.
- Os ensaios que estão suspensos após o fim do período de transição não podem ser objeto de transição. Reiniciar o ensaio nestas circunstâncias necessitaria da submissão de uma nova submissão de CT ao abrigo do CTR.
CTIS da UE CTIS EMA atualizações técnicas da EMA para melhorar as suas características e funcionalidades. Quando são introduzidas alterações significativas no CTIS, a EMA notas de lançamento que descrevem o que mudou no sistema. As atualizações podem incluir melhorias nas características e funcionalidades existentes, a adição de novas funcionalidades e aperfeiçoamentos funcionais e técnicos. Um parceiro experiente em assuntos regulamentares pode abordar potenciais desafios e ajudar os patrocinadores na transição de ensaios clínicos existentes e futuros, no âmbito das estratégias de desenvolvimento clínico. Clique aqui para saber mais sobre o CTIS a experiência da Freyr nesta área: https://www.freyrsolutions.com/medical-devices/regulatory-affairs.










