
A US Food and Drug Administration (US FDA) publicou uma orientação em dezembro de 2022, uma revisão da orientação intitulada ‘Failure to Response to an ANDA Complete Response Letter (CRL) Within the Regulatory Timeframe Guidance for Industry,’ de julho de 2022. Destina-se a orientar os requerentes de Abbreviated New Drug Applications (ANDAs) submetidas ao abrigo da secção 505(j) do Federal Food, Drug, and Cosmetic Act (FD&C Act) (21 U.S.C. 355(j)). Uma resposta completa e relevante a uma CRL é crucial para a aprovação do medicamento genérico. O documento de orientação oferece recomendações sobre as repercussões de receber uma CRL e as ações que a FDA pode tomar se a CRL não for respondida dentro do prazo especificado.
A FDA deve garantir que os medicamentos genéricos aprovados cumprem os padrões de segurança, qualidade, eficácia e acessibilidade. Se a ANDA não cumprir os requisitos regulamentares da FDA, uma CRL é enviada ao requerente e inclui as deficiências identificadas durante a sua avaliação.
Segue-se uma descrição figurativa do que um requerente pode fazer no prazo de um ano após receber a CRL:
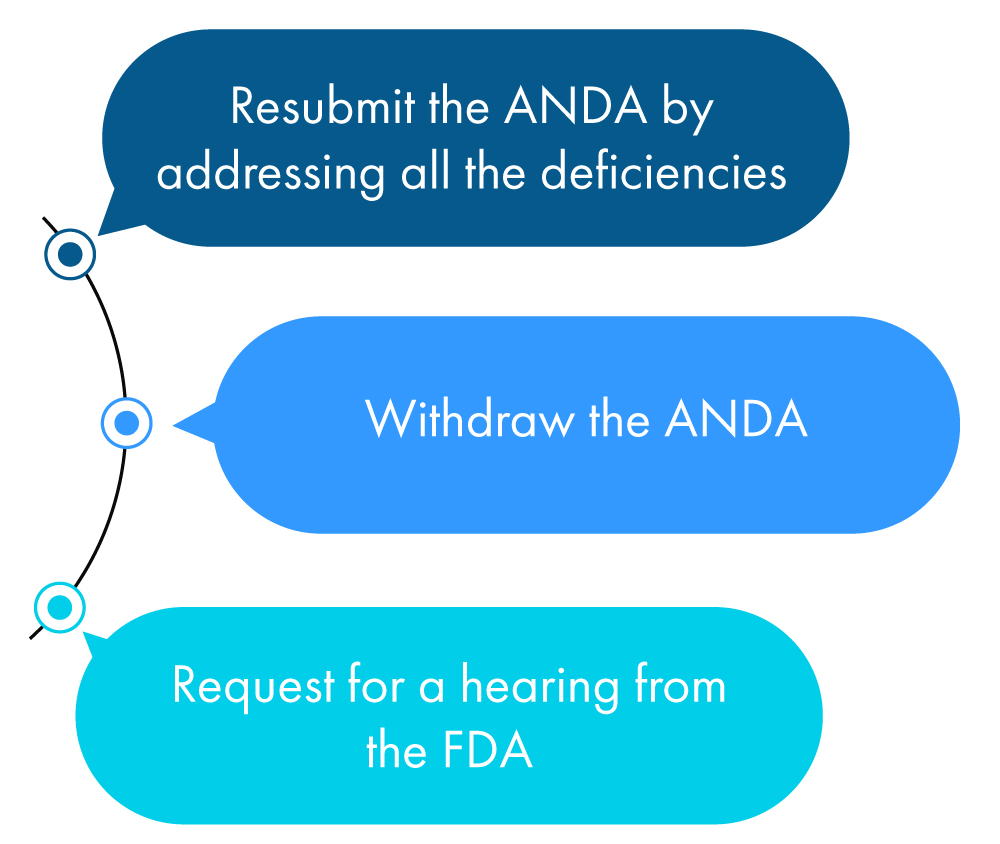
Se nenhuma das ações acima for tomada pelo requerente, a FDA considera isso um pedido de retirada da ANDA, a menos que o requerente tenha solicitado uma extensão de prazo para verificar todas as discrepâncias mencionadas na CRL.
O que acontece após um (01) ano da emissão do CRL?
A FDA envia uma notificação escrita de que o requerente tem trinta (30) dias a partir da notificação para o seguinte:
- Apresente as razões pelas quais a ANDA não deve ser retirada
- Pedido de extensão do prazo para resolver todas as deficiências mencionadas no CRL
Assim que a FDA recebe um pedido de extensão do requerente, considera vários fatores, conforme mencionado abaixo, e subsequentemente decide sobre o pedido:
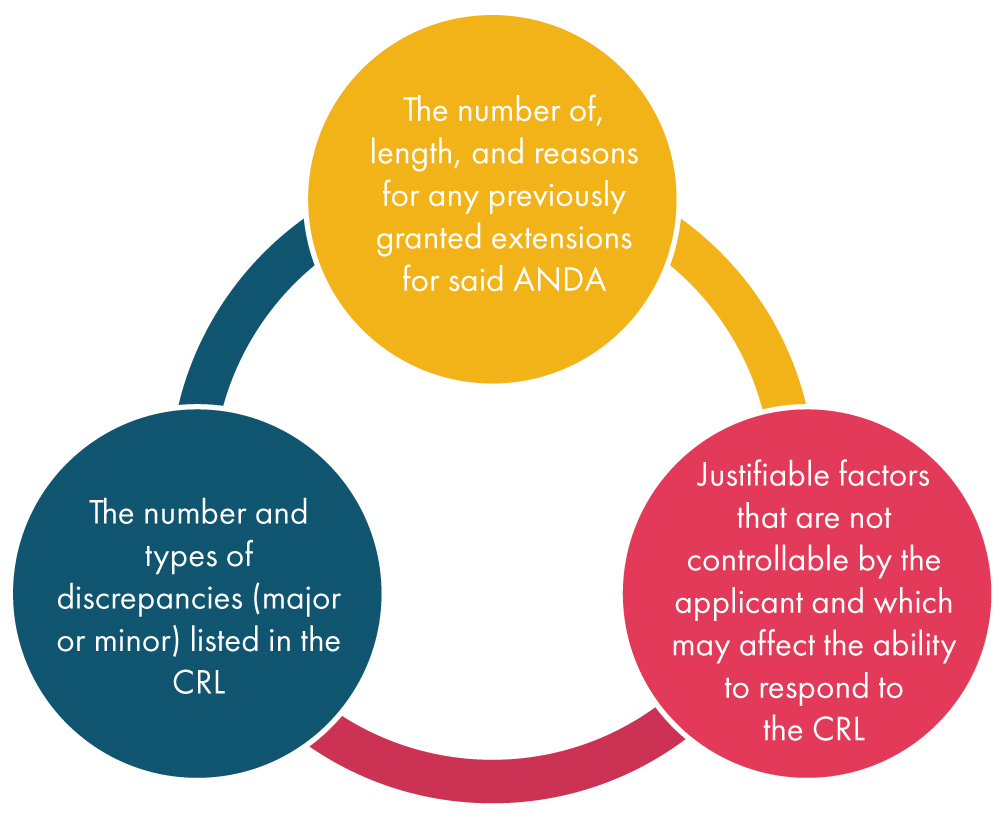
O que é uma Alteração?
O requerente precisa de submeter um pedido de prorrogação para responder a um CRL através de uma alteração. A FDA classifica uma alteração como maior ou menor com base no efeito que tem no processo de aprovação.
Recomendações Vitais da FDA que os Candidatos Devem Conhecer:
- A FDA reclassificará uma alteração menor como uma alteração maior se a alteração for submetida após um ano do CRL, a menos que a ANDA seja para um produto na lista de escassez de medicamentos ao abrigo da secção 506E do FD&C Act (21 U.S.C. 356e), ou seja objeto de uma resposta a uma Emergência de Saúde Pública, conforme declarado pelo Secretário do Departamento de Saúde e Serviços Humanos dos US ao abrigo da secção 319 do Public Health Service Act (42 U.S.C. 247d), ou se prevê que esteja sujeita aos mesmos critérios que se aplicam a tal declaração, no momento da submissão.
- Se o requerente não conseguir resolver as discrepâncias na CRL dentro do período alargado concedido pela FDA, esta última pode considerar a retirada da ANDA.
- Se o requerente precisar de mais do que o período de extensão de trinta (30) dias, pode solicitar uma nova extensão. A alteração deve então incluir novas informações que permitam à FDA determinar se a extensão pode ser concedida ou não.
Receber um CRL da FDA pode ser bastante intimidante para os requerentes de ANDA. Desde a resolução das discrepâncias até à citação das razões/informações corretas para uma extensão, todos os requisitos relevantes devem ser cumpridos para garantir uma aprovação mais rápida do medicamento. A Freyr é um especialista comprovado em Assuntos Regulamentares com vasto conhecimento na resposta a CRLs e na garantia de conformidade com os requisitos da FDA. Contacte-nos agora para apoio estratégico End-to-End nas submissões ANDA.










