Os dispositivos médicos inovadores são essenciais para melhorar os resultados dos cuidados de saúde, abordar as necessidades médicas em evolução e fornecer soluções económicas para pacientes e prestadores de cuidados de saúde. A estratégia SAKIGAKE é um processo de revisão e aprovação acelerado para dispositivos médicos inovadores no Japão. Esta estratégia foi iniciada pelo Ministério da Saúde, Trabalho e Bem-Estar (MHLW) do Japão em 2015, com o objetivo de acelerar o desenvolvimento e a comercialização de dispositivos médicos inovadores no Japão.
No âmbito da estratégia SAKIGAKE, os dispositivos médicos que cumprem determinados critérios de inovação podem receber revisão e aprovação prioritárias pela Agência de Produtos Farmacêuticos e Dispositivos Médicos (PMDA), a Agência Regulamentar responsável pelas aprovações de dispositivos médicos no Japão. Os critérios de designação para inovação incluem o seguinte:
- Dispositivos com eficácia proeminente; espera-se que o dispositivo proporcione um benefício clínico significativo com um novo mecanismo de ação e uma melhoria radical para os doentes em comparação com os dispositivos médicos existentes.
- Em primeiro lugar, o dispositivo é aplicável para aprovações no Japão ou simultaneamente no Japão e noutros países.
- O dispositivo tem o potencial de responder a necessidades médicas não satisfeitas no Japão. A condição médica alvo deve ser grave, potencialmente fatal ou com sintomas persistentes.
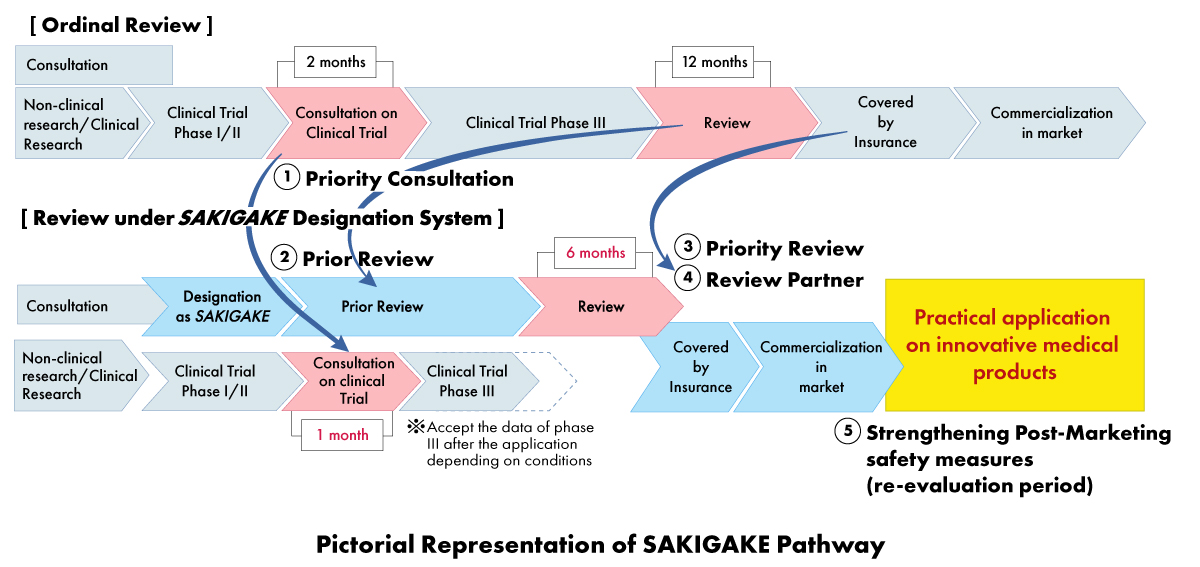
No âmbito da estratégia SAKIGAKE, os fabricantes de dispositivos médicos podem beneficiar de uma série de vantagens, incluindo:
- Consulta Prioritária: Redução do tempo de espera para a consulta de ensaios clínicos para um (01) mês.
- Revisão Prioritária: Os produtos designados SAKIGAKE recebem revisão prioritária, com o objetivo de concluir o processo de revisão no prazo de seis (06) meses em vez de 12 meses.
- Revisão Eficaz antes da Submissão: Incentivar a consulta e aceitar materiais em inglês.
- Gestor de Revisão Dedicado: A cada produto designado SAKIGAKE é atribuído um gestor de revisão dedicado para todo o processo de aprovação.
- Reforço das Medidas de Segurança Pós-comercialização: Extensão do período de reexame e facilitação da ligação com sociedades científicas.
Como Candidatar-se?
- Pelo Requerente: O requerente está a submeter a submissão à Divisão de Avaliação e Licenciamento da PMDA (ELD).
- Pela PMDA-ELD: A ELD está a contactar um potencial requerente.
Fonte: PMDA, Japão.
No geral, o sistema SAKIGAKE oferece uma via acelerada para o desenvolvimento e aprovação de dispositivos médicos inovadores no Japão. O seu objetivo é melhorar os resultados para os doentes e promover a inovação na indústria de dispositivos médicos. O fabricante deve consultar a PMDA numa fase inicial do processo de desenvolvimento para discutir os requisitos regulamentares e receber feedback sobre os seus planos de desenvolvimento de produtos.
Para saber mais sobre as vias de registo de dispositivos médicos no Japão, contacte já um especialista em regulamentação! Mantenha-se informado. Mantenha-se em conformidade.
