O principal objetivo da US FDA é escrutinar constantemente e colmatar a lacuna entre os processos regulamentares para a importação e venda ininterruptas de dispositivos médicos novos e de alta qualidade no mercado dos US. A US FDA, em 1998, lançou um programa denominado “O Novo Paradigma 510(k): Abordagens Alternativas para Demonstrar Equivalência Substancial em Notificações Pré-Comercialização.” Pretende estabelecer uma via de submissão 510(k) da FDA eficiente que contenha certas alterações na submissão 510(k) já aprovada. Esta nova notificação 510(k) oferece (03) três tipos de submissões, nomeadamente, 510(k) especial, 510(k) abreviado e 510(k) tradicional. A US FDA, em 2019, emitiu um documento de orientação 510(k) especial que descreve uma via opcional para fabricantes que realizam certas modificações bem definidas nos seus dispositivos legalmente comercializados.
Porquê um 510(k) Especial?
Quando um fabricante pretende a aprovação para as modificações que realizou num dispositivo já comercializado, ou seja, no dispositivo existente, pode solicitar um 510(k) especial. Os principais fatores a considerar ao determinar se uma alteração a um dispositivo existente pode ser apropriada para um 510(k) especial são os seguintes:
- A alteração reside no dispositivo precedente legalmente comercializado do próprio requerente.
- Não são necessários dados de desempenho, ou existem métodos bem estabelecidos, caso seja considerado necessário avaliar a alteração.
- Todos os dados de desempenho para apoiar uma determinação de equivalência substancial podem ser revistos num formato de resumo ou análise de risco.
Documentos Necessários para 510(k) Especial
- Carta de apresentação
- O nome do dispositivo legalmente comercializado (existente) do fabricante e o número 510(k).
- Uma descrição detalhada das alterações efetuadas ao dispositivo que resultaram na submissão de um novo 510(k)
- Uma comparação do dispositivo modificado com o dispositivo aprovado em formato tabular
- Outras alterações à rotulagem ou conceção
- Um resumo conciso das atividades de controlo de projeto.
- Com base na análise de risco, uma identificação das atividades de verificação e/ou validação necessárias para cumprir com a 21 CFR 820.30
- Formulário de indicações de utilização
- Uma declaração de que o requerente cumpriu e não está atualmente em violação dos requisitos do procedimento de controlo de conceção, conforme especificado em 21 CFR 820.30, e que os registos estão disponíveis para revisão mediante pedido.
Cronograma de Revisão Especial 510(k) pela FDA dos US
De acordo com as diretrizes da FDA “Refuse to Accept Policy for 510(k)s”, o prazo de análise para submissões especiais 510(k) é de trinta (30) dias após a sua receção.
Quando Solicitar um 510(k) Especial?
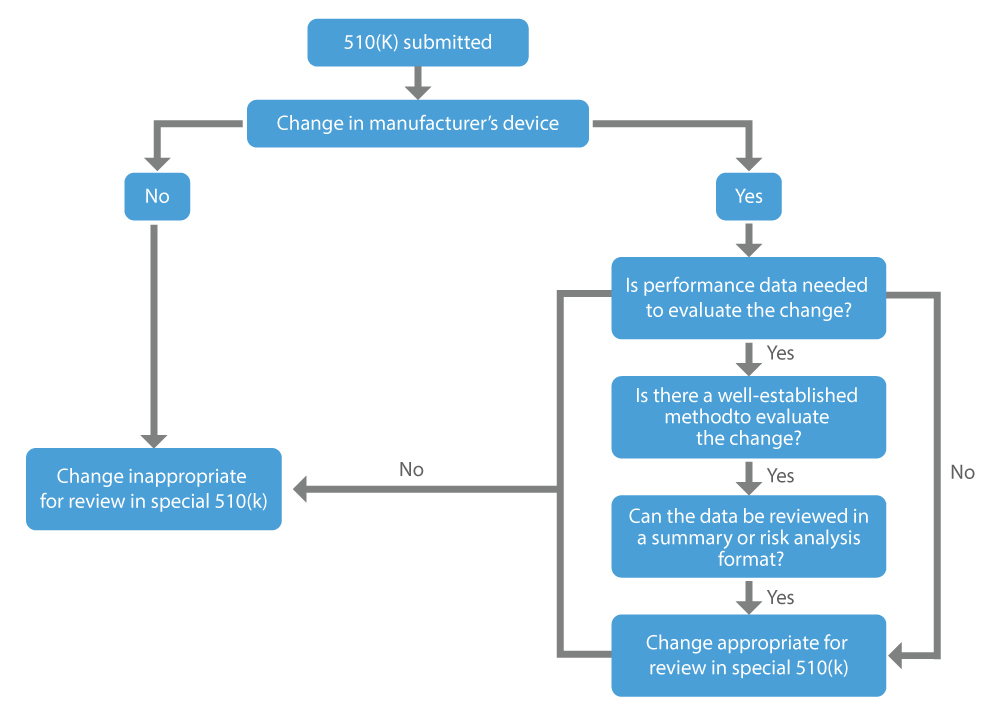
A US FDA faz esforços consistentes para fornecer dispositivos médicos seguros e eficazes para promover a saúde humana. O programa Especial 510(k) é eficiente e consistente com o procedimento de revisão menos oneroso que ajuda os fabricantes estrangeiros a vender os seus dispositivos nos EUA e permite que os pacientes tenham acesso atempado a novos dispositivos médicos.
Para qualquer esclarecimento adicional sobre o processo especial 510(k) da FDA, contacte a Freyr – um especialista em Regulamentação comprovado. Mantenha-se informado. Mantenha-se em conformidade.