
Os Assuntos Regulamentares (RA) desempenham um papel crucial para assegurar a segurança, eficácia e qualidade dos produtos farmacêuticos no dinâmico panorama farmacêutico. Os Assuntos Regulamentares de Química, Fabrico e Controlo (CMC) são essenciais para a conformidade. O seu objetivo é salvaguardar a saúde do paciente e promover a confiança pública nos produtos farmacêuticos, assegurando a consistência e a qualidade ao longo de todo o processo de fabrico do medicamento.
O CMC RA abrange os requisitos de documentação e conformidade relacionados com o fabrico, controlo de qualidade e estabilidade dos produtos farmacêuticos. Implica atenção ao detalhe e adesão às diretrizes regulamentares ao longo de todo o ciclo de vida do desenvolvimento do medicamento. Para saber mais sobre a importância do CMC RA, consulte os nossos especialistas.
Neste blog, aprofundaremos os fundamentos da CMC RA e exploraremos a sua importância para alcançar a conformidade e manter elevados padrões de qualidade.
O Papel do CMC no Desenvolvimento de Medicamentos
As considerações de CMC começam cedo no processo de desenvolvimento de medicamentos e continuam por todas as fases, desde a investigação pré-clínica até à comercialização. Os dados e a documentação de CMC são componentes críticos das submissões regulamentares, tais como submissões de Investigational New Drug (IND), submissões de New Drug (NDA) e submissões de Autorização de Introdução no Mercado (MAA). As autoridades regulamentares analisam os dados de CMC para avaliar a segurança, identidade, potência e qualidade de um medicamento, bem como a fiabilidade e consistência do processo de fabrico.
Garantir a Conformidade com CMC RA
A conformidade com os requisitos regulamentares de CMC é fundamental para uma entrada bem-sucedida no mercado. Autoridades regulamentares como a United States Food and Drug Administration (USFDA), a Agência Europeia de Medicamentos (EMA) e outras Autoridades de Saúde (HA) regionais são responsáveis por estabelecer diretrizes e padrões que devem ser seguidos. Estas diretrizes abrangem vários aspetos, incluindo práticas de fabrico, sistemas de qualidade, métodos analíticos, testes de estabilidade e validação. A conformidade envolve documentação meticulosa, adesão às Boas Práticas de Fabrico (BPF) e implementação de Sistemas de Gestão da Qualidade (SGQ) eficazes.
O Papel da Conformidade CMC no Sucesso de uma Empresa Farmacêutica
Manter altos padrões de conformidade CMC oferece várias vantagens às empresas farmacêuticas. Alguns dos principais benefícios são:
- Mitigar os riscos regulamentares.
- Apoiar aprovações regulamentares bem-sucedidas.
- Reduzir a probabilidade de recolhas de produtos.
- Fomentar uma reputação positiva de qualidade e fiabilidade.
Aspetos a Ponderar para uma Função de Assuntos Regulamentares CMC Bem-sucedida:
- Manter-se Atualizado com o Conhecimento Regulamentar: Os requisitos regulamentares em evolução das Autoridades de Saúde (HAs) exigem que se mantenha atualizado com as últimas diretrizes. A monitorização contínua das atualizações regulamentares e a sua incorporação nas práticas de CMC é crucial para manter a conformidade.
- Estabelecimento de Sistemas de Qualidade: Isto inclui o desenvolvimento e a manutenção de Procedimentos Operacionais Padrão (SOPs) abrangentes, procedimentos de controlo de documentos, processos de controlo de alterações e programas de formação para garantir que os funcionários compreendem e seguem os protocolos estabelecidos.
- Avaliação e Mitigação de Riscos: As empresas devem identificar os riscos potenciais ao longo dos processos de desenvolvimento e fabrico de medicamentos e implementar estratégias adequadas de mitigação de riscos. Isto inclui a avaliação de parâmetros críticos do processo, variabilidade da matéria-prima, potenciais impurezas e riscos da cadeia de abastecimento, o que garante a conformidade.
- Documentação e Integridade dos Dados: Manter uma documentação precisa e completa é essencial para demonstrar conformidade. As empresas devem estabelecer práticas de documentação robustas, incluindo a manutenção de registos de lotes, dados analíticos, estudos de estabilidade e relatórios de validação. Garantir a integridade, rastreabilidade e segurança dos dados é fundamental para evitar problemas de conformidade.
- Gestão Eficaz de Alterações: As empresas devem ter procedimentos de controlo de alterações bem definidos para avaliar e documentar as alterações, analisar o seu impacto na qualidade do produto e na conformidade regulamentar, e procurar as aprovações necessárias antes de implementar as alterações.
- Parcerias e Gestão Robustas de Fornecedores: Isto envolve a seleção de fornecedores qualificados, a realização de auditorias e o estabelecimento de acordos de qualidade que delineiam responsabilidades e expectativas. A realização de avaliações regulares da conformidade dos fornecedores com os requisitos das Boas Práticas de Fabrico Atuais (cGMP) é essencial.
- Preparação para Auditorias e Inspeções: As empresas devem realizar autoavaliações para identificar áreas de melhoria e garantir a preparação para auditorias regulamentares. De facto, abordar prontamente as conclusões das auditorias e implementar ações corretivas são essenciais para manter a conformidade.
- Melhoria Contínua: Isto pode ser alcançado incentivando o envolvimento dos colaboradores, fornecendo formação e educação sobre os requisitos regulamentares e promovendo uma mentalidade orientada para a qualidade em todos os níveis da organização.
- Abordagem de Ações Corretivas e Preventivas (CAPA): Ao abordar sistematicamente a não conformidade utilizando a metodologia CAPA, as empresas farmacêuticas podem demonstrar o seu compromisso com a melhoria contínua e a conformidade.
- Conhecimento das Alterações Regulamentares Pós-aprovação: Compreender os requisitos regulamentares para as alterações pós-aprovação é essencial para garantir a conformidade. A implementação de processos de gestão de alterações adequados e a comunicação eficaz com as Autoridades de Saúde (HAs) podem ajudar a gerir estas alterações, garantindo a conformidade.
O Papel de um Fornecedor Regulamentar no Processo de Conformidade CMC
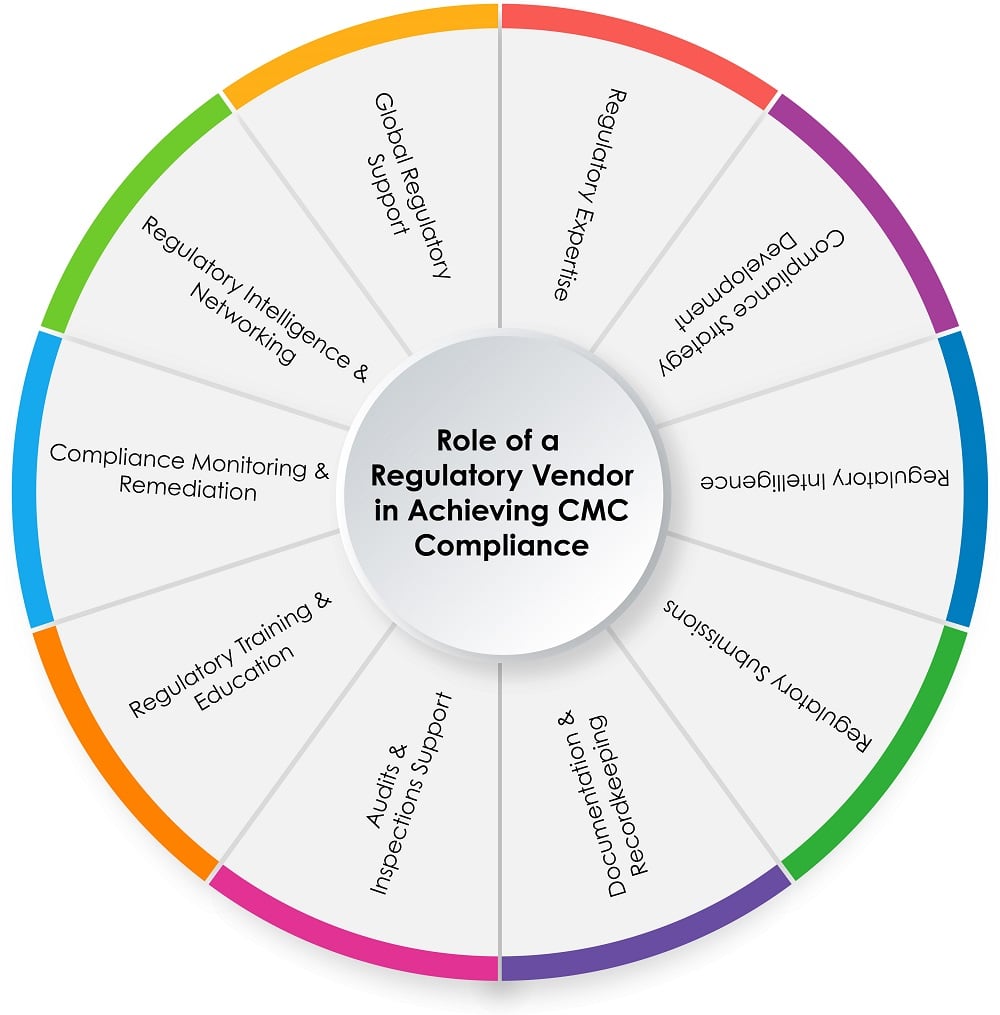
O gráfico circular abaixo (Figura 1) mostra o papel de um fornecedor regulamentar no processo de conformidade CMC:
Figura 1: O papel de um fornecedor regulamentar na obtenção da conformidade CMC
Conclusão
Alcançar e manter a conformidade com os requisitos de CMC exige uma abordagem estratégica, que envolve colaboração interfuncional, sistemas de qualidade robustos e inteligência regulamentar (RI) contínua. É também essencial para um acesso bem-sucedido ao mercado e para a disponibilidade contínua do produto. Uma compreensão aprofundada dos fundamentos da RA de CMC e a implementação de estratégias de conformidade eficazes podem ajudar as empresas farmacêuticas a navegar no panorama regulamentar, a obter aprovações e a manter os mais elevados padrões de qualidade e segurança do paciente. Parcerias regulamentares estratégicas podem otimizar estas etapas cruciais, oferecendo a melhor experiência para manter a conformidade. Fale connosco para saber mais sobre os nossos serviços!









