
A intercambialidade com um produto biológico de referência é um passo crucial no processo de aprovação para biossimilares. Garante que um biossimilar pode ser substituído pelo produto de referência sem qualquer risco significativo de eficácia reduzida ou aumento de preocupações de segurança. Este blogue tenta compreender a mais recente atualização da FDA sobre as considerações para alcançar a intercambialidade e as melhores práticas da indústria para alcançar a excelência regulamentar.
Definir a Intercambialidade
Alcançar a intercambialidade é um processo complexo e rigoroso que exige o cumprimento de requisitos regulamentares rigorosos. O desafio reside em demonstrar que o biossimilar não só corresponde ao produto de referência em termos de segurança e eficácia, mas também proporciona os mesmos resultados clínicos em qualquer paciente. O não cumprimento destes requisitos pode resultar em atrasos ou recusas na aprovação, afetando o acesso ao mercado e os cuidados ao paciente.
Requisitos Regulamentares para Intercambialidade
A FDA descreve critérios específicos para demonstrar a intercambialidade nos seus documentos de orientação. Estes critérios incluem:
- Estudos Analíticos Comparativos: São necessários estudos analíticos extensivos para demonstrar que o biossimilar é altamente semelhante ao produto de referência. Estes estudos avaliam a estrutura molecular, função e composição do biossimilar.
- Estudos Clínicos: São necessários estudos clínicos para confirmar que o biossimilar não apresenta diferenças clinicamente significativas em relação ao produto de referência em termos de segurança, pureza e potência. Isto envolve frequentemente estudos farmacocinéticos (PK) e farmacodinâmicos (PD) comparativos.
- Estudos de Troca: A FDA exige estudos de troca para avaliar o impacto da alternância entre o biossimilar e o produto de referência. Estes estudos são cruciais para garantir que a troca não afeta a eficácia ou a segurança do tratamento.
- Estratégias de Avaliação e Mitigação de Risco (REMS): Se aplicável, as REMS devem ser abordadas para garantir que o biossimilar possa ser usado de forma intercambiável sem preocupações adicionais de segurança.
Etapas para alcançar a intercambialidade estrategicamente
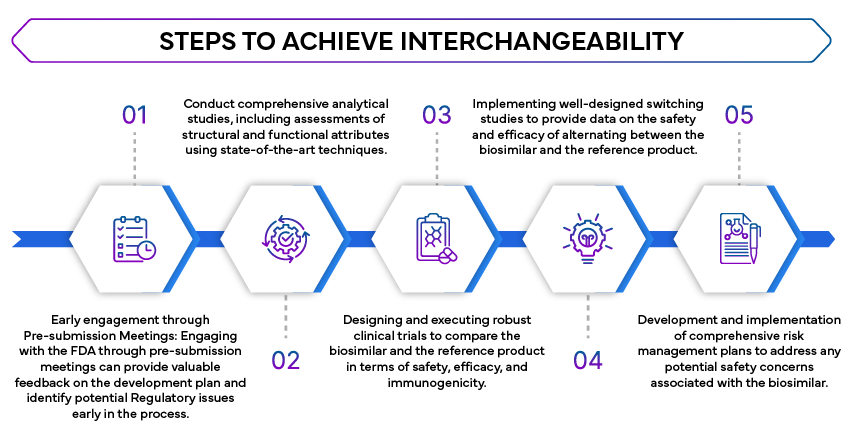
Papel de um Parceiro Regulamentar
As parcerias de regulamentação podem aumentar significativamente a probabilidade de alcançar a intercambialidade. Veja como um parceiro de regulamentação pode ajudar:
- Orientação Especializada: Fornece aconselhamento especializado sobre requisitos regulatórios e estratégias para cumprir as diretrizes da FDA.
- Apoio à Documentação: Ajuda na preparação de documentos de submissão de alta qualidade que cumprem as normas regulamentares.
- Desenho de Estudos Clínicos: Apoia o desenho e a execução de estudos clínicos e de transição robustos.
- Interações com a HA: Facilita a comunicação eficaz com a HA, garantindo feedback atempado e construtivo.
- Gestão de Risco: Desenvolver estratégias abrangentes de gestão de risco para mitigar potenciais preocupações de segurança.
Vantagens de ter um Parceiro de Regulamentação
| Vantagens | Descrição | |
| 1. | Especialização em Requisitos Regulamentares | Conhecimento aprofundado dos panoramas e requisitos regulamentares globais. |
| 2. | Documentação Otimizada | Garante a preparação de documentação precisa e em conformidade. |
| 3. | Processo de Submissão Eficiente | Reduz o tempo e o custo através de uma gestão eficiente das submissões. |
| 4. | Conformidade Melhorada | Minimiza o risco de atrasos e rejeições através de um cumprimento rigoroso. |
| 5. | Gestão Eficaz de Riscos | Identificação e mitigação proativa de potenciais riscos. |
Resumo
Alcançar a intercambialidade com um produto de referência é um processo exigente, mas essencial para a aprovação bem-sucedida de biossimilares. Exige uma compreensão abrangente dos requisitos regulamentares, planeamento meticuloso e dados clínicos robustos. A parceria com um fornecedor experiente de serviços de regulamentação pode aumentar significativamente as chances de sucesso, garantindo que o biossimilar cumpre os critérios rigorosos estabelecidos pelas autoridades regulamentares. Ao aproveitar a orientação especializada, documentação completa e gestão estratégica de riscos, os promotores podem navegar pelo complexo caminho para a intercambialidade de forma mais eficaz.










