
Nos últimos anos, o panorama dos Assuntos Regulamentares tem sofrido uma transformação significativa. No cerne desta mudança está uma crescente ênfase na centralidade nopaciente, com as autoridades de saúde (AS) em todo o mundo a reconhecerem o papel inestimável que os pacientes desempenham no desenvolvimento e aprovação de novos Medicamentos. Esta mudança não é apenas uma tendência; é uma reinterpretação fundamental de como abordamos as submissões regulamentares e, em última análise, como servimos aqueles que mais importam – os pacientes.
O Problema:
Tradicionalmente, as submissões regulamentares focavam-se principalmente no cumprimento dos requisitos técnicos e científicos, muitas vezes negligenciando o impacto direto nas experiências e resultados dos pacientes. Esta abordagem, embora exaustiva, por vezes não consegue captar as nuances das necessidades, preferências e utilização no mundo real dos medicamentos. Como resultado, existia uma desconexão entre as aprovações regulamentares e o valor real entregue aos pacientes.
Abordagens Regulamentares Centradas no Doente:
As autoridades de saúde, em particular a FDA e a EMA, deram passos significativos na incorporação das perspetivas dos pacientes nos seus quadros regulamentares.
Esta abordagem centrada no paciente é evidente em várias áreas-chave:
- Desenvolvimento de Medicamentos Focado no Paciente (PFDD):
O programa PFDD da FDA é uma iniciativa inovadora que recolhe sistematicamente o contributo dos pacientes para informar o desenvolvimento de medicamentos e a tomada de decisões regulamentares. Este programa inclui sessões de escuta aos pacientes, reuniões públicas e o desenvolvimento de documentos de orientação para melhorar o envolvimento dos pacientes ao longo de todo o ciclo de vida do produto. - Evidência do Mundo Real (RWE):
Há um reconhecimento crescente do valor dos dados do mundo real para compreender o desempenho de um produto em diversas populações de pacientes. As HAs estão agora mais abertas a considerar a RWE em submissões regulamentares, proporcionando uma visão mais abrangente dos benefícios e riscos de um produto. - Resultados Reportados pelos Pacientes (PROs):
A inclusão de PROs em ensaios clínicos e submissões Regulamentares tornou-se cada vez mais importante. Estas medidas capturam diretamente a experiência do paciente, fornecendo informações valiosas sobre sintomas, qualidade de vida e satisfação com o tratamento. - Envolvimento Precoce e Aconselhamento Científico:
As autoridades de saúde estão a encorajar os promotores a envolverem-se precocemente no processo de desenvolvimento, incluindo frequentemente representantes de pacientes nestas discussões. Este diálogo precoce ajuda a alinhar os planos de desenvolvimento com as necessidades dos pacientes e as expectativas regulamentares. - Envolvimento do Paciente nas Avaliações de Benefício-Risco:
Tanto a FDA como a EMA desenvolveram estruturas para incorporar as perspetivas dos pacientes nas avaliações de benefício-risco, garantindo que as decisões regulamentares reflitam o que é mais importante para os pacientes.
Tabela: Principais Iniciativas Centradas no Paciente por Principais Autoridades de Saúde
| Autoridade de Saúde | Iniciativa | Descrição |
|---|---|---|
| FDA | Desenvolvimento de Medicamentos Focado no Doente (PFDD) | Abordagem sistemática para recolher o contributo dos pacientes |
| EMA | Grupo de Trabalho de Doentes e Consumidores (PCWP) | Fórum de diálogo com organizações de pacientes e consumidores |
| MHRA | Envolvimento do Doente e do Público | Estratégia para envolver os pacientes nos processos Regulamentares |
| Health Canada | Estrutura de Envolvimento para Medicamentos e Produtos de Saúde Canadianos | Melhora o envolvimento do paciente em atividades Regulamentares |
Papel dos Prestadores de Serviços Regulamentares:
Neste cenário em evolução, o papel dos profissionais e parceiros de Assuntos Regulamentares tornou-se mais crucial do que nunca. Eles servem como ponte entre patrocinadores, autoridades de saúde e pacientes, garantindo que as estratégias regulamentares se alinhem com abordagens centradas no paciente.
As principais responsabilidades incluem:
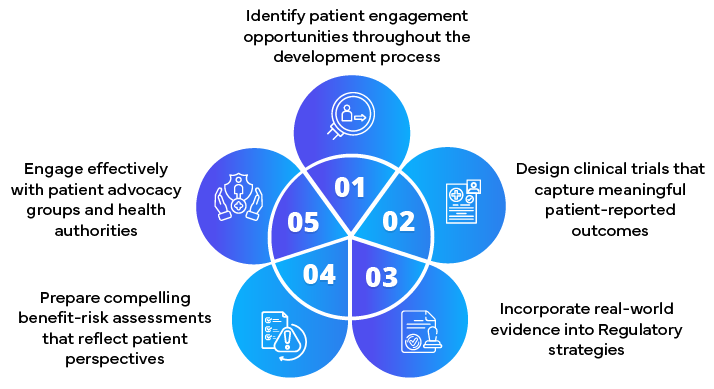
- Desenvolvimento de estratégias de envolvimento do paciente
- Incorporar o contributo do paciente nas submissões regulamentares
- Aconselhamento sobre a recolha e apresentação de dados centrados no paciente
- Facilitar o envolvimento precoce com as autoridades de saúde
- Manter-se a par dos requisitos Regulamentares centrados no paciente em evolução
Papel dos Parceiros Regulamentares na obtenção de submissões Centradas no Paciente
Resumo:
A mudança para a centralidade no paciente nos Assuntos Regulamentares representa uma oportunidade significativa para desenvolver e aprovar produtos médicos que realmente satisfaçam as necessidades dos pacientes. Ao adotar esta abordagem, os patrocinadores podem não só navegar pelas vias regulamentares de forma mais eficaz, mas também fornecer produtos que fazem uma diferença significativa na vida dos pacientes. À medida que as autoridades de saúde continuam a refinar as suas abordagens centradas no paciente, a experiência de prestadores de serviços regulamentares ou parceiros torna-se inestimável para garantir que as submissões não só cumprem os requisitos técnicos, mas também ressoam com as experiências e prioridades dos pacientes.
Nesta nova era de Assuntos Regulamentares, colocar os pacientes em primeiro lugar não é apenas uma boa prática – é a chave para o sucesso.









