
Em 9 de fevereiro de 2022, a Agência Europeia de Medicamentos (EMA) deu início à criação de um Centro de Coordenação para a Rede de Análise de Dados e Integração do Mundo Real (DARWIN EU®). Este é o primeiro passo para integrar a Evidência do Mundo Real (RWE) na avaliação de medicamentos em toda a União Europeia (UE). Garantir a segurança e a eficácia dos medicamentos é a principal atividade de qualquer Agência Reguladora, e a RWE está a revelar-se uma fonte fiável para a recolha de evidências em tempo real a partir de bases de dados globais de cuidados de saúde. Assim, esta iniciativa da EMA visa melhorar a qualidade dos medicamentos na região da UE e torná-los disponíveis mais rapidamente.
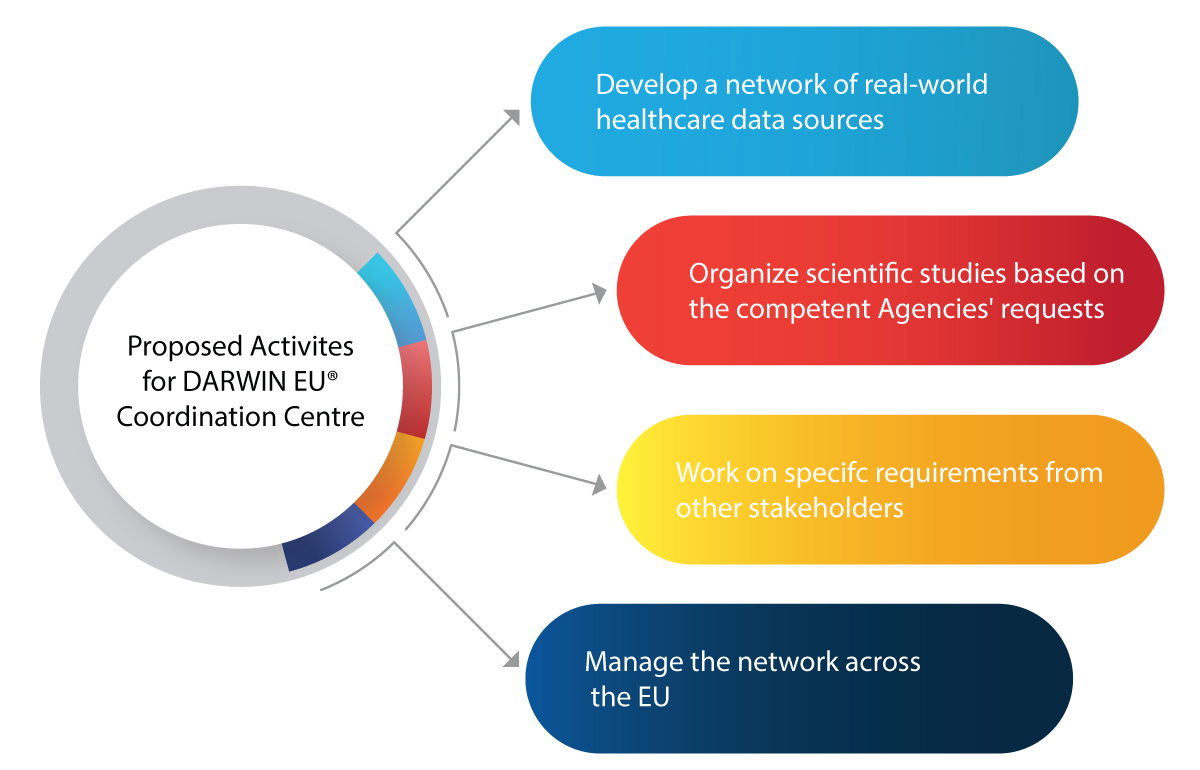
Principais Atividades Planeadas para o Centro de Coordenação da DARWIN EU®
Como é que o DARWIN EU® Vai Ajudar a EMA e as Autoridades Relevantes no Espaço Regulamentar?
Medicamentos inovadores que estejam prontamente disponíveis para os doentes são uma necessidade urgente. Os processos regulamentares para o desenvolvimento, aprovação, comercialização e Vigilância Pós-Comercialização demoram um tempo considerável, o que faz com que a procura por novos medicamentos não seja satisfeita. Reduzir o tempo de colocação no mercado, garantindo a segurança, eficácia e qualidade dos medicamentos inovadores, é o caminho a seguir. Várias Autoridades de Saúde globais estão a identificar os benefícios da integração de RWE nas suas aprovações regulamentares, e o DARWIN EU® é uma iniciativa da EMA.
A EMA planeia ligar a rede regulamentar europeia de medicamentos ao Espaço Europeu de Dados de Saúde (EHDS) para uma melhor troca de dados e acesso melhorado a vários tipos de dados de saúde no âmbito deste programa. Irá também estabelecer padrões para avaliações científicas e tomada de decisões regulamentares.
Aqui estão algumas atividades que o DARWIN EU® pretende alcançar:
- Utilização de RWE em atividades de tomada de decisão para a regulamentação de novos medicamentos, vacinas, etc.
- Integrar a RWE em todo o ciclo de vida de um medicamento, como o desenvolvimento, a autorização e a vigilância pós-comercialização
- Preparar para quaisquer emergências médicas futuras, como pandemias
- Beneficiar a indústria farmacêutica com RWE perspicazes e fiáveis sobre doentes, doenças e utilização de medicamentos
- Tomar decisões regulamentares informadas com base em RWE para a utilização segura e eficaz dos medicamentos
- Melhoria da acessibilidade de medicamentos que salvam vidas a doentes necessitados, devido à análise de dados precisa e atempada
Prazos Propostos para a DARWIN EU® se Tornar uma Rede Totalmente Funcional na UE
A EMA também especifica os prazos para a DARWIN EU® estar totalmente operacional, e são os seguintes:
- 2021 – Início do projeto
- 2022 – Criação da DARWIN EU®
- 2023 – Desenvolvimento da DARWIN EU® e definição das suas utilizações
- 2024 – Colocar a DARWIN EU® em pleno funcionamento
- 2025 – Melhorar as utilizações regulamentares dos dados de saúde, aumentando os âmbitos em termos de medicamentos, geografia, etc.
A EMA está a colaborar com o Erasmus University Medical Center Rotterdam para a criação da DARWIN EU®. O objetivo desta parceria é a criação do Centro de Coordenação para estabelecer uma rede de dados distribuída. Ambos assumiram também as tarefas de realizar estudos científicos, apoiar os processos de tomada de decisão regulamentar e gerir um catálogo de fontes de dados do mundo real.
O Que Significa a Iniciação da DARWIN EU® para o Futuro?
A EMA e os Chefes das Agências de Medicamentos (HMA) sempre trabalharam em conjunto para identificar os desafios, estabelecer metas com prazos definidos e definir prioridades nos seus documentos de estratégia de cinco (05) anos. Destina-se a fornecer uma direção estratégica às atividades realizadas pela rede regulamentar europeia de medicamentos.
A iniciação da DARWIN EU® é um passo importante para a concretização da Estratégia de Rede da EMA. A realização de estudos científicos para responder a questões de investigação, o apoio à avaliação de medicamentos na UE e a manutenção de Metadata para atividades regulamentares de medicamentos são os principais objetivos. A DARWIN EU® é vista como um interveniente importante na regulamentação de medicamentos na Europa, e os estudos-piloto deverão estar concluídos até ao final de 2022.
Se for um fabricante de medicamentos e deseja saber mais sobre RWE e como está a moldar o futuro da tomada de decisões Regulamentares, contacte os especialistas em Assuntos Regulamentares da Freyr.









