
A Therapeutic Goods Administration (TGA) na Austrália tem regras rigorosas para o registo de novos medicamentos sujeitos a receita médica com novos ingredientes ativos. Recentemente, a TGA apresentou um processo revisto para melhorar a eficácia dos medicamentos sujeitos a receita médica que salvam vidas e torná-los disponíveis aos doentes mais rapidamente. Estas alterações são pertinentes para submissões que precisam de ser apoiadas por dados não clínicos, clínicos e/ou de bioequivalência (categoria 1 e categoria 2). A TGA divulgou um documento em agosto com detalhes dos requisitos de Regulamentação para o mesmo.
Características Significativas no Novo Processo de Registo para Medicamentos Sujeitos a Receita Médica
- A TGA desenvolveu um processo de registo faseado e denominou as etapas como marcos. Cada uma delas segue um caminho separado.
- O novo processo visa melhorar a qualidade do dossiê. Os dossiês são preparados com base num formato de documento técnico comum (CTD) e seguem todos os requisitos regulamentares.
- A fase de planeamento pré-submissão é importante, pois os requerentes apresentam os detalhes da submissão prospetiva. Isso é feito pelo menos dois meses e um quarto (02 ¼) antes da submissão do dossiê completo. Esta fase visa ajudar a TGA a definir as datas dos marcos subsequentes e a preparar os recursos para gerir o CTD.
- A próxima fase é a submissão. Uma vez concluída, a TGA não permite que o requerente forneça quaisquer dados ou informações adicionais após a data de submissão. É obrigatório submeter um dossiê completo, correto e de alta qualidade.
- Ao abrigo da secção 31 da Lei dos Produtos Terapêuticos de 1989, a TGA solicita informações adicionais na fase de avaliação. Após a avaliação inicial, todos os pedidos são compilados e enviados ao requerente.
Para compreender as etapas do processo atualizado, consulte os seguintes fluxogramas.
Etapa 1
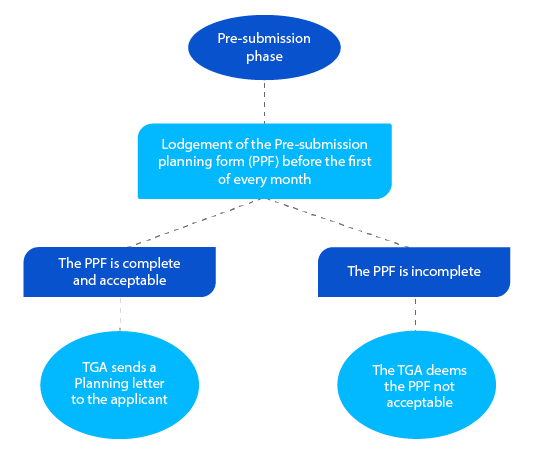
A carta de planeamento contém a data esperada em que a TGA prevê a apresentação do dossiê e outras datas-chave para a submissão de medicamentos sujeitos a receita médica.
Etapa 2
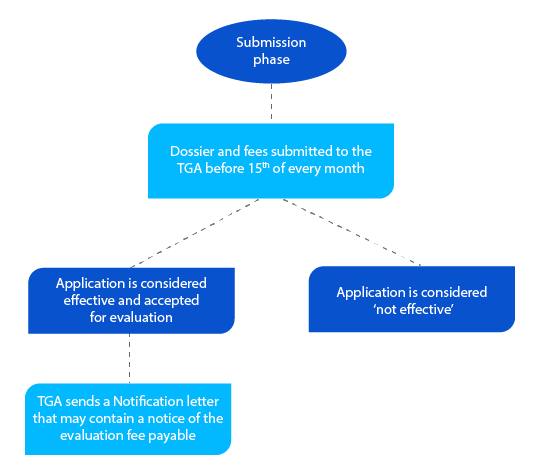
O dossiê contém informações que ajudam a TGA a avaliar a submissão e, se tudo estiver aceitável, é enviada uma carta de Notificação antes do final do mês em que o requerente submeteu o dossiê.
Etapa 3
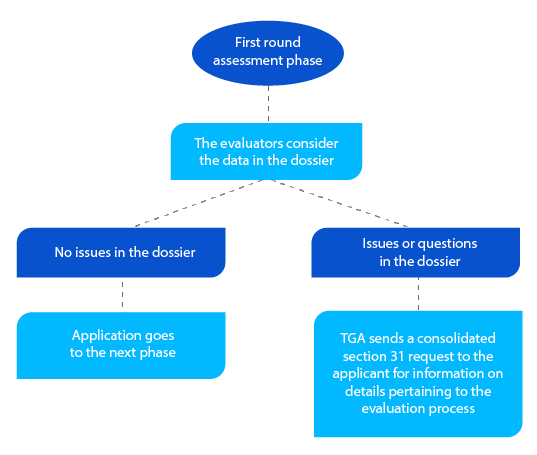
Para além da secção 31 consolidada, e sempre que aplicável, a TGA envia cópias dos relatórios de avaliação preparados pelos avaliadores de qualidade, não clínicos, clínicos e dos Planos de Gestão de Risco (RMP).
Etapa 4
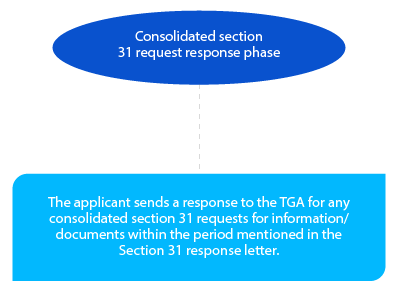
O requerente pode indicar o prazo de resposta da secção 31. Este pode ser de trinta (30) ou sessenta (60) dias e deve ser destacado no PPF. Este período deve ser confirmado pela TGA na Carta de Planeamento. O formato aceitável da resposta é CTD, e a mesma deve ser enviada em formato físico e eletrónico.
Uma vez que esta é a última oportunidade para o requerente fornecer qualquer informação em falta à TGA, deve ser feito de forma conforme.
Etapa 5
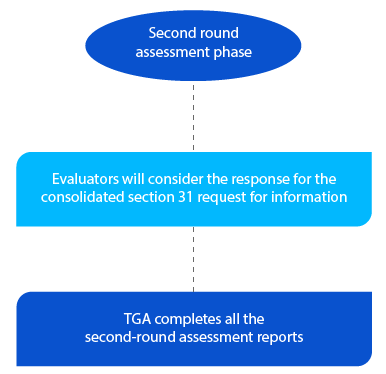
A TGA dispõe de dois (02) meses para novas submissões de medicamentos genéricos para a segunda ronda de relatórios de avaliação e um (01) mês para todos os outros tipos de submissão. Os relatórios são enviados aos respetivos requerentes após a conclusão da segunda avaliação.
Etapa 6
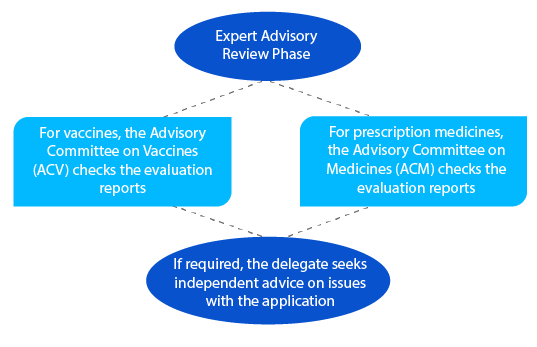
Após a análise consultiva, a TGA envia uma notificação com os detalhes do parecer que recebe do ACV ou do ACM.
Etapa 7
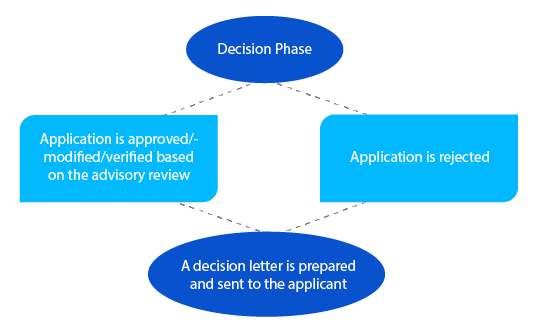
Em caso de questões pendentes, o delegado pode contactar o requerente nesta fase antes de tomar uma decisão. Para as submissões ao abrigo da secção 23 da Lei dos Produtos Terapêuticos de 1989 (medicamentos listados recentemente avaliados no Registo Australiano de Produtos Terapêuticos (ARTG)), é enviada uma notificação ao requerente no prazo de vinte e oito (28) dias após a tomada da decisão.
Etapa 8
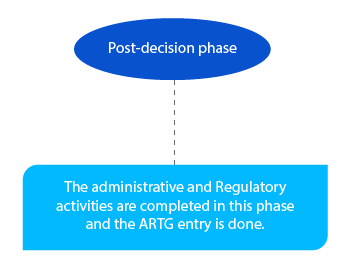
Os pagamentos pendentes são tratados nesta fase. E devem ser concluídos até ao final do mês seguinte à decisão do delegado.
Com a TGA a tomar todas as precauções para garantir a segurança, eficácia e qualidade dos medicamentos sujeitos a receita médica, enquanto reduz o seu tempo de colocação no mercado, a responsabilidade recai sobre o requerente para fazer as submissões relevantes para um processo de registo tranquilo. Seja em qualquer fase, colaborar com um fornecedor de serviços regulamentares End-to-End que seja especialista no registo de medicamentos sujeitos a receita médica é a situação ideal. Contacte uma entidade regulamentar experiente para uma via de conformidade; mantenha-se atualizado e mantenha-se em conformidade.










