
A Necessidade Médica Não Satisfeita (UMN) é uma das prioridades mais urgentes dos sistemas de saúde. A ciência e a tecnologia em constante evolução na área da saúde têm proporcionado o potencial para explorar várias opções terapêuticas. As Autoridades de Saúde incentivam terapias inovadoras que prometem benefícios significativos para a qualidade de vida dos doentes. Com base na priorização da inovação e na abordagem das necessidades não satisfeitas dos doentes para o desenvolvimento de medicamentos, a Agência Europeia de Medicamentos (EMA) introduziu a via PRIority MEdicines (PRIME) em 2016. Desde então, a via PRIME tem sido um método para conceder aprovações para terapias inovadoras num prazo acelerado. Este tipo de via facilitada pode ser explorado por qualquer empresa, desde start-ups a biotecnológicas de média dimensão e grandes organizações multinacionais. No entanto, a qualificação para a via está limitada a produtos em desenvolvimento e que ainda não solicitaram uma Autorização de Introdução no Mercado através do procedimento centralizado. Os critérios de qualificação são aplicados rigorosamente. Entre março de 2016 e abril de 2022, apenas 24% das submissões receberam o aval, enquanto 72% das submissões PRIME foram rejeitadas. Dos 24% que foram selecionados para a via PRIME, a maioria pertencia à área terapêutica da oncologia.
Os inovadores que procuram autorizações de introdução no mercado para doenças raras ou medicamentos órfãos podem frequentemente ter conjuntos de dados limitados disponíveis como prova para apoiar as suas submissões de novos medicamentos, conforme exigido pelos reguladores. As submissões para Medicamentos de Terapia Avançada (ATMPs) e medicamentos órfãos geralmente enfrentam tais desafios. Devido a dados limitados da população de doentes, é incentivada a interação constante com os reguladores para permitir melhores informações para a revisão científica e os requisitos de aprovação. O caminho PRIME pode ser útil para tais terapias devido ao envolvimento precoce dos reguladores no fornecimento de apoio proativo e orientação para a recolha de dados e avaliação benefício-risco.
Vantagens de seguir a Via PRIME
- Ajuda os inovadores a desenvolver um plano de desenvolvimento bem elaborado.
- Beneficia os inovadores ao envolver as Autoridades de Saúde na fase inicial de desenvolvimento; isto contribui para a elaboração de submissões de autorização de introdução no mercado de alta qualidade.
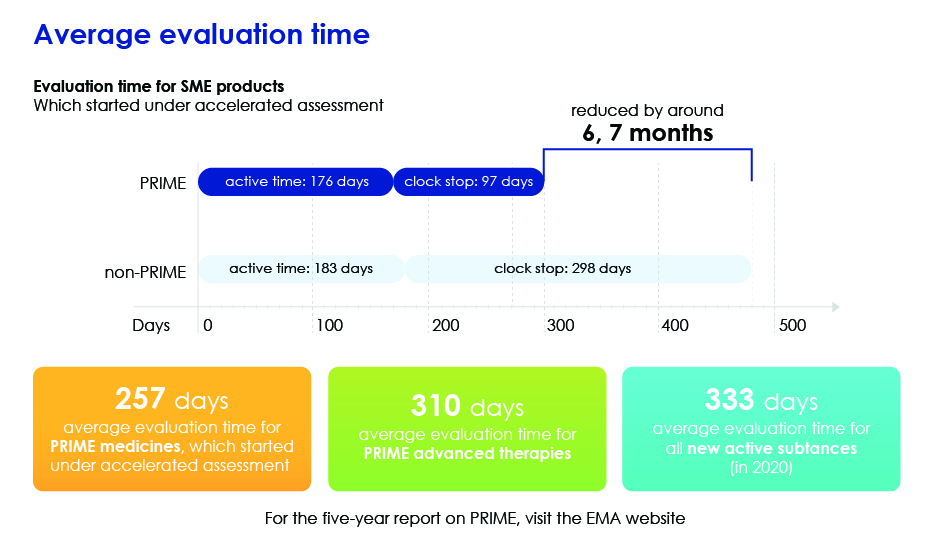
- Acelera a avaliação geral ao reduzir o tempo médio de avaliação para que os medicamentos possam chegar aos pacientes mais rapidamente.
- Apoia os inovadores a concentrarem a sua atenção no desenvolvimento de medicamentos para melhorar os resultados dos pacientes e responder às necessidades não satisfeitas dos pacientes.
Tempo de Avaliação em Detalhe
Submissões para o Percurso PRIME
A via PRIME prioriza necessidades médicas não satisfeitas. De 384 pedidos PRIME recebidos desde março de 2016, apenas 18 obtiveram Autorização de Introdução no Mercado até junho de 2021.

Está pronto para o PRIME?
A existência da via PRIME deve-se a necessidades médicas significativas não satisfeitas e ao foco em colmatar as lacunas pela Rede Regulamentar Europeia de Medicamentos (EMRN). Para avaliar a adequação de um produto à via PRIME, deve-se considerar o seguinte:
- Constatações: Os requerentes devem indicar a necessidade médica não satisfeita e apresentar um argumento convincente sobre como o seu produto irá resolver a questão.
- Potencial: Os requerentes devem demonstrar o potencial benéfico da terapia nos critérios de necessidade médica não satisfeita.
- Dados pré-clínicos: Os requerentes devem apresentar alguns dados sobre a eficácia ou o desempenho da terapia no sistema biológico humano. Os modelos não clínicos, por mais precisos que sejam, não fornecem uma visão exata do seu comportamento no sistema biológico humano.
- Fase de desenvolvimento: O requerente deve identificar a fase certa para entrar na via PRIME, a fim de obter a orientação ideal dos reguladores e prosseguir com a submissão.
Após a Concessão PRIME
Uma vez que um requerente tenha tido a oportunidade de entrar na via facilitada, a EMA irá:
- Atribuir um relator do Comité dos Medicamentos para Uso Humano (CHMP) ou do Comité das Terapias Avançadas (CAT) no caso de terapias avançadas.
- Organizar uma reunião de arranque com o relator do CHMP/CAT e um grupo multidisciplinar de especialistas para fornecer orientação sobre o plano de desenvolvimento geral e a estratégia de Regulamentação.
- Designar um único ponto de contacto para o requerente.
- Fornecer aconselhamento científico em cada etapa crucial de desenvolvimento, envolvendo um conjunto adicional de partes interessadas, como organismos de avaliação de tecnologias de saúde – para acelerar o acesso dos doentes ao novo medicamento.
- Confirmar o potencial de avaliação acelerada no momento de uma submissão, considerando a Autorização de Introdução no Mercado.
A sua submissão para o programa PRIority MEdicine (PRIME) está pronta? Contacte a Freyr hoje e avalie. Saiba mais sobre como podemos ajudar com a sua estratégia regulamentar e a designação para o programa PRIME. Mantenha-se informado. Mantenha-se em conformidade.









