
As inovações nas combinações medicamento-dispositivo levaram a avanços significativos nos cuidados ao paciente. Os medicamentos combinados com dispositivos médicos oferecem administração direcionada de medicamentos, resultados terapêuticos melhorados e maior adesão do paciente. No entanto, navegar pelo panorama regulamentar para combinações medicamento-dispositivo pode ser complexo.
Este blogue explorará as considerações e os desafios associados às operações regulamentares para produtos de combinação medicamento-dispositivo, oferecendo informações para otimizar os processos.
Visão Geral e Estrutura Regulamentar para Combinações Medicamento-Dispositivo
Os produtos de combinação medicamento-dispositivo sinergizam os efeitos terapêuticos dos medicamentos farmacêuticos com as capacidades de administração dos dispositivos médicos. As combinações medicamento-dispositivo incluem stents elutores de fármacos, inaladores e dispositivos respiratórios, adesivos transdérmicos, sistemas de administração de insulina, sistemas de infusão de fármacos e balões revestidos com fármacos. A administração direcionada, a eficácia melhorada, a maior adesão do paciente e o controlo preciso sobre o tratamento são alguns dos atributos notáveis destes produtos.
Autoridades regulamentares como a Food and Drug Administration dos Estados Unidos (US FDA), a Agência Europeia de Medicamentos (EMA) e outras estabeleceram diretrizes para combinações de medicamentos e dispositivos. Os últimos anos testemunharam desenvolvimentos notáveis no panorama regulamentar, com um foco crescente na harmonização, avaliações baseadas no risco e vigilância pós-comercialização.
Considerações Essenciais para as Operações Regulamentares
Ao navegar pelas operações regulamentares para combinações medicamento-dispositivo, algumas das considerações a ter em conta são detalhadas abaixo:
Compreender a classificação do produto e as vias regulamentares
É crucial compreender a classificação dos produtos de combinação medicamento-dispositivo e selecionar a via regulamentar apropriada. Os fabricantes devem determinar se se trata de uma combinação medicamento-dispositivo, de uma categoria de dispositivo revestido com medicamento ou de uma categoria de produto coembalado. A seleção da via correta para o tipo de produto específico é vital para um acesso bem-sucedido ao mercado.
Abordar os requisitos científicos e técnicos
Inclui garantir a compatibilidade entre os componentes do medicamento e do dispositivo, realizar estudos de estabilidade para avaliar o prazo de validade do produto, validar os processos de fabrico e implementar avaliações de risco para identificar e mitigar potenciais perigos.
Cuidados ao paciente e testes de usabilidade
Os cuidados ao paciente e a engenharia de usabilidade desempenham um papel significativo no desenvolvimento de tais produtos de combinação. Considerar fatores como a interface do utilizador, a ergonomia, o manuseamento do dispositivo e a adesão do paciente durante o desenvolvimento do produto ajuda a garantir a sua utilização segura e eficaz por pacientes e profissionais de saúde com o mínimo de erros.
Considerações pós-comercialização
As obrigações pós-comercialização são um aspeto crítico da conformidade regulamentar para combinações medicamento-dispositivo. Os fabricantes devem estabelecer processos para a notificação de eventos adversos, vigilância pós-comercialização e notificação de vigilância para monitorizar a segurança e o desempenho dos seus produtos.
Manter-se atualizado com as recentes diretrizes e atualizações regulamentares
Acompanhar as diretrizes e atualizações recentes é crucial para garantir a conformidade e alinhar as estratégias regulamentares com as expectativas atuais. O panorama regulamentar para combinações de medicamentos e dispositivos está em constante evolução. Alinhar com a FDA, o Regulamento de Dispositivos Médicos da UE (MDR) e as diretrizes do Conselho Internacional para a Harmonização dos Requisitos Técnicos para Produtos Farmacêuticos para Uso Humano (ICH) pode ajudar os fabricantes a manterem-se em conformidade.
Melhores Práticas para Otimizar as Operações Regulamentares
Para otimizar as operações regulamentares para combinações medicamento-dispositivo, as empresas farmacêuticas podem seguir as melhores práticas ilustradas no gráfico circular abaixo:
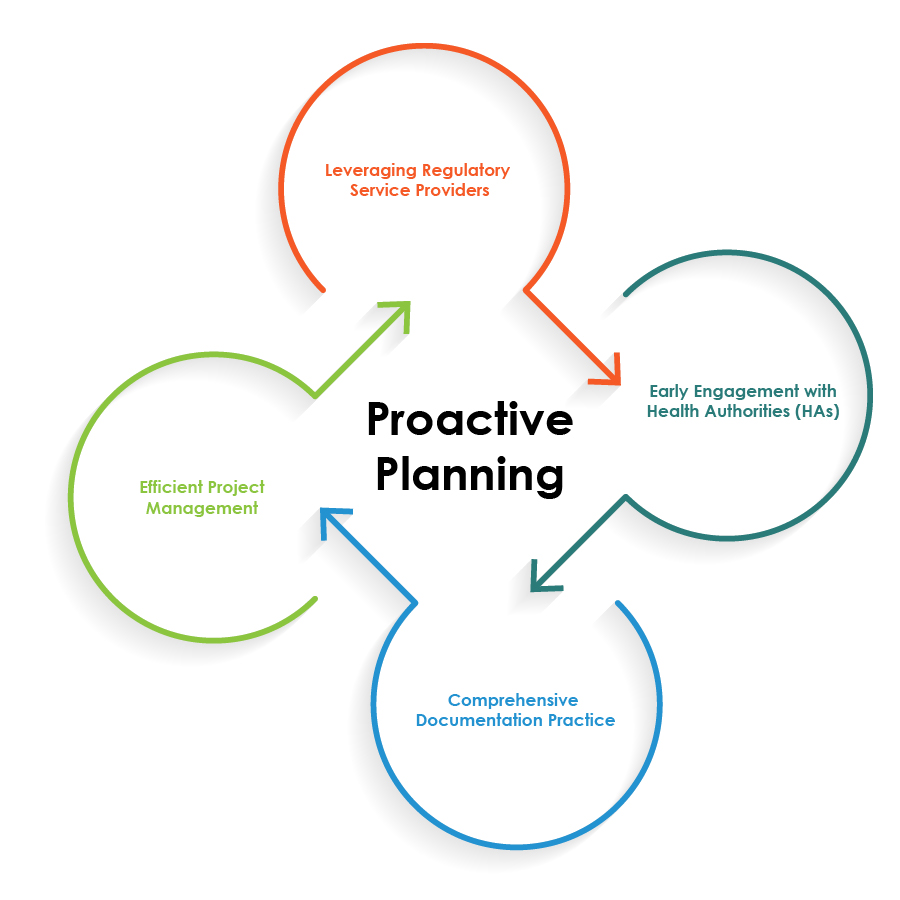
O planeamento proativo é a pedra angular para operações regulamentares de combinação medicamento-dispositivo sem falhas
Tendências e Desafios Futuros
Estar atento às tendências e deficiências futuras é crucial para as empresas farmacêuticas e para os profissionais de regulamentação envolvidos nas operações de regulamentação destes produtos. Apresentamos abaixo algumas tendências e desafios a ter em conta:
- Tecnologias emergentes: A nanotecnologia, a impressão 3D e as aplicações relacionadas influenciam o desenvolvimento de combinações inovadoras de medicamentos e dispositivos. Estas tendências tecnológicas oferecem administração direcionada de medicamentos, medicina personalizada e monitorização aprimorada do paciente. No entanto, também apresentam desafios de regulamentação únicos relacionados com a segurança, eficácia e controlo de qualidade.
- Cibersegurança: Com a crescente conectividade dos dispositivos médicos, garantir a segurança dos dados e proteger contra ameaças cibernéticas torna-se primordial. A integração de medidas robustas de cibersegurança e a atualização das melhores práticas para a segurança dos dispositivos são considerações críticas para as operações de regulamentação.
- Desafios diversos: Estes incluem as complexidades da cadeia de abastecimento global, como o aprovisionamento de matérias-primas, a disponibilidade de componentes e os processos de fabrico, que colocam desafios na manutenção da conformidade regulamentar e na garantia da qualidade do produto. Práticas robustas de gestão da cadeia de abastecimento, avaliações de risco e supervisão de fornecedores são essenciais para abordar estes desafios e mitigar os riscos associados.
Navegar no panorama regulamentar para produtos de combinação medicamento-dispositivo requer uma compreensão abrangente do quadro regulamentar, das diretrizes recentes e das melhores práticas. Abordar considerações-chave, manter-se atualizado com as mudanças e implementar as melhores práticas ajudará as empresas farmacêuticas a otimizar as suas operações regulamentares. Colaborar com fornecedores regulamentares permite que as empresas aproveitem conhecimentos e experiências especializados e otimizem as suas chances de sucesso regulamentar neste campo em evolução e exigente. Com a nossa comprovada experiência na adesão às normas regulamentares globais, a Freyr pode ajudar a alcançar um percurso de produto em conformidade. Para saber mais, contacte-nos.









