
Para melhorar a acessibilidade de medicamentos inovadores para pacientes no REINO UNIDO pós-Brexit, uma nova e acelerada via de aprovação, conhecida como Innovative Licensing and Access Pathway (ILAP), foi lançada em janeiro de 2021. O seu objetivo principal era fornecer um roteiro integrado para todas as partes interessadas que melhora o processo de desenvolvimento de produtos. O ILAP apoia ainda mais os desenvolvedores comerciais e não comerciais, facilitando o acesso de medicamentos inovadores à população de pacientes, reduzindo o tempo de colocação no mercado. As empresas farmacêuticas podem explorar o ILAP como uma via assim que os dados não clínicos estiverem consolidados. É aplicável a Novas Entidades Químicas (NCE), medicamentos biológicos, novas indicações e medicamentos reposicionados.
A ILAP é uma iniciativa desenvolvida em conjunto pela Medicines and Healthcare products Regulatory Agency (MHRA), em associação com o All-Wales Therapeutics and Toxicology Centre (AWTTC), o National Institute of Health and Care Excellence (NICE) e o Scottish Medicines Consortium (SMC) como parceiros permanentes. Os parceiros de apoio na ILAP incluem o National Health Service England (NHS), a Health Research Authority (HRA) e o National Institute for Health Research (NIHR). Juntas, as partes interessadas fornecem contributos regulamentares, científicos, éticos e comerciais aprimorados na fase inicial do desenvolvimento de medicamentos durante os ensaios clínicos.
Na opinião da Freyr, o ILAP oferece grandes oportunidades para os desenvolvedores de tratamentos inovadores, especialmente para aqueles que abordam necessidades não satisfeitas dos pacientes. Por uma taxa relativamente modesta (aproximadamente £8000), uma empresa poderia obter aconselhamento em fase inicial, conseguir uma designação para o seu produto e acordar um perfil de desenvolvimento-alvo. Isto tem o potencial de poupar uma quantidade significativa de tempo no ciclo de vida geral de desenvolvimento do produto. Existem também benefícios em olhar para além da Autorização de Introdução no Mercado e fazer preparativos antecipados para negociações de reembolso.
A ILAP compara-se favoravelmente com esquemas semelhantes oferecidos na rede europeia de medicamentos (como o PRIME). Embora diferentes em conceito e entrega, a ILAP tem critérios de aceitação mais amplos e uma taxa de aceitação mais elevada. A ILAP também oferece um caminho para a integração com o Project Orbis da Food and Drug Administration dos Estados Unidos (USFDA) para produtos oncológicos emergentes.
Como solicitar o ILAP?
Para aceder ao ILAP, os requerentes devem solicitar um Passaporte de Inovação (IP). Obter uma designação IP permite aos desenvolvedores de medicamentos aceder ao percurso com base nas evidências necessárias para que um produto cumpra os critérios de elegibilidade definidos pela NICE, SMC, AWTTC e pela MHRA.
Esta designação atua como um catalisador para produtos inovadores desde a fase pré-clínica até à fase intermédia de desenvolvimento. O IP pode levar à definição de um documento de Perfil de Desenvolvimento Alvo (TDP). O TDP é um roteiro que facilita o acesso aos parceiros do ILAP nas fases iniciais do ciclo de vida do desenvolvimento de medicamentos para acelerar e agilizar o acesso dos pacientes a tratamentos novos e inovadores. Os pacientes fazem parte de todo este processo. Várias ferramentas fornecidas pelo ILAP apoiam os requerentes em todas as fases do processo de conceção, desenvolvimento e aprovações.
Critérios de Designação de Passaporte Inovador
A orientação da MHRA esclarece os critérios para uma designação IP. Isto é particularmente relevante para produtos inovadores e também se compara favoravelmente com esquemas equivalentes oferecidos na Europa.
No futuro, a aplicabilidade específica do IP para dispositivos médicos e produtos combinados, áreas em que há sempre uma inovação significativa, pode revelar-se benéfica.
A designação IP é avaliada pelos parceiros permanentes e de apoio com base nos seguintes critérios:
- Critério 1: Detalhes da condição, paciente ou área de saúde pública
- Para condições que colocam a vida em risco e condições graves
- Num evento em que a necessidade é crucial para os pacientes
- Critério 2: O medicamento cumpre uma ou mais áreas específicas que incluem
- Medicamento inovador
- Medicamento associado a uma nova indicação
- Medicamento para doença rara
- Medicamento em desenvolvimento com o objetivo de saúde pública do REINO UNIDO
- Critério 3: O medicamento tem o potencial de oferecer
- Um breve resumo sobre como o medicamento ou indicação proposta beneficiará os pacientes.
- As opiniões de pacientes ou organizações de pacientes são encorajadas.
Ao submeter a submissão de IP, realiza-se uma reunião entre os requerentes e a MHRA para compreender se o produto cumpre os três (03) critérios.
De acordo com as últimas informações de janeiro de 2022, a MHRA recebeu setenta e uma (71) submissões, das quais quarenta e uma (41) resultaram na designação IP, vinte e duas (22) estão a ser processadas e sete (07) submissões foram recusadas.
O momento certo para entrar no ILAP é mencionado abaixo.
- Na fase inicial a intermédia de desenvolvimento do produto
- Quando dados relevantes estão disponíveis
- Quando os requerentes sentem a necessidade de obter contributos das partes interessadas
- Os requerentes aspiram a adotar novas abordagens inovadoras
- Não quando o produto está perto do fim da fase de desenvolvimento
Visão geral do Desenvolvimento de Medicamentos
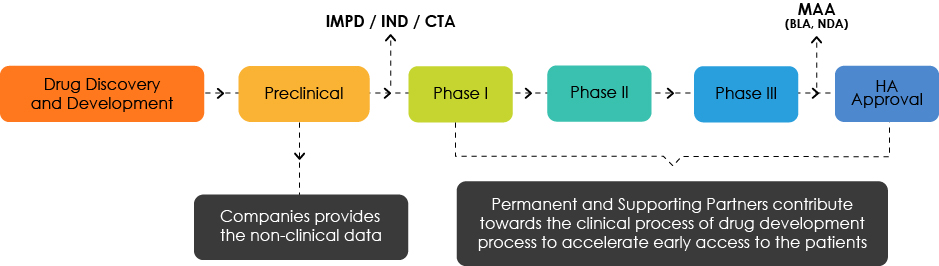
Compreender o Perfil de Desenvolvimento Alvo (TDP)
Os especialistas em TDP analisam as características do produto e destacam as deficiências de um ponto de vista regulamentar. São responsáveis por orientar os desenvolvedores de medicamentos para um roteiro que proporciona acesso precoce dos pacientes aos seus produtos.
O TDP é um documento que é atualizado em tempo real de acordo com os requisitos alinhados com o desenvolvimento do produto. Assim, um produto passa por múltiplas alterações de TDP à medida que novos dados são gerados.
A acessibilidade dos pacientes a medicamentos essenciais pode ser comprometida por atrasos no mercado. Para evitar tais cenários, as vias aceleradas funcionam como um catalisador. O ILAP é um exemplo de uma via de autorização flexível que é bem aceite em toda a indústria e pode acelerar o cronograma de desenvolvimento de medicamentos inovadores. Os critérios detalhados definidos pelo Sistema de Saúde do Reino Unido permitem que os requerentes explorem a sua elegibilidade para solicitar a designação IP. Incentivar as necessidades clínicas e dos pacientes não satisfeitas com vias aceleradas como o ILAP facilita a entrada no mercado e pode proporcionar alívio às populações de pacientes em risco. Para salvaguardar o interesse dos pacientes, as Autoridades de Saúde não comprometem a segurança, eficácia ou qualidade do produto, ao mesmo tempo que garantem um processo de aprovação expedito. Os serviços regulamentares End-to-End da Freyr facilitam o processo de documentação para apoiar a designação de Passaporte Inovador num tempo expedito, ajudando os seus produtos a chegar aos pacientes mais cedo. Contacte a Freyr.










