
Em Hong Kong, o processo de aprovação para medicamentos órfãos para doenças raras, especialmente aqueles que contêm Novas Entidades Químicas ou Biológicas (NCEs) para doenças que ameaçam a vida ou que são gravemente debilitantes, é gerido pela Pharmacy and Poisons Board of Hong Kong. Abaixo encontra-se um guia passo a passo para navegar no processo:
Guia passo a passo para a aprovação de medicamentos órfãos para doenças raras
Preparação e Submissão
Prepare a submissão os documentos essenciais:
- Relatórios de avaliação de peritos e documentos CTD sobre segurança, eficácia e qualidade
- Planos de Gestão de Risco (RMPs)
- Rótulos de produtos e folhetos informativos
- Relatórios de avaliação de riscos de impurezas elementares
- Recorde mundial de inscrições
Submeta a sua submissão para registo através do Pharmaceuticals Registration System 2.0 (PRS 2.0) no website do Drug Office. Este é um primeiro passo crítico para aqueles que registam medicamentos órfãos para doenças raras em Hong Kong.
Pagamento de taxas
Pague a taxa de submissão através de:
- PRS 2.0 (online) – via cartão de crédito ou PPS
- Presencialmente – usando dinheiro ou cheque no Drug Office
- Triagem e Avaliação
- O Drug Office examina todos os documentos submetidos antes de aceitar a submissão para avaliação.
- Se os documentos estiverem incompletos, será emitida uma carta de deficiência.
- Mecanismo de Recusa de Submissão (RTF)
- A partir de 1 de julho de 2024, o mecanismo RTF garante que apenas as candidaturas completas e devidamente documentadas passem à fase de avaliação. É concedido aos candidatos um prazo de 60 dias para corrigirem quaisquer deficiências identificadas durante a triagem inicial.
- As candidaturas incompletas serão rejeitadas na fase de pré-seleção. A falta de resposta no prazo de 60 dias implicará a rejeição automática da submissão.
Procedimentos Reforçados para Produtos NCE
No que diz respeito NCE abrangidos pelo«mecanismo 1+»(para doenças potencialmente fatais ou gravemente incapacitantes), o Conselho aprovou melhorias destinadas a facilitar e acelerar o processo de registo — o que é particularmente benéfico para os medicamentos destinados ao tratamento de doenças raras.
- Requisitos Pós-Aprovação
- Após o registo do produto:
- Cumprir os requisitos de farmacovigilância
- Comunicar reações adversas graves a medicamentos (ADRs)
- Implementar e manter planos de gestão de risco
- Após o registo do produto:
Recursos
Se for lesado por uma decisão do comité, o requerente pode recorrer ao Tribunal de Recurso da Pharmacy and Poisons.
Prazos
O Departamento de Saúde pretende concluir o processo de registo cerca de 9 meses após a submissão, desde que todos os documentos estejam completos. Isto ajuda a colocar medicamentos para doenças raras no mercado de forma eficiente.
Consulta e Feedback
O Conselho pode realizar consultas com as partes interessadas e especialistas da indústria durante as fases de avaliação e implementação de políticas.
Atualizações Contínuas
Mantenha-se informado verificando regularmente:
- O website oficial do Conselho
- Anúncios do Gabinete de Medicamentos
Fluxograma
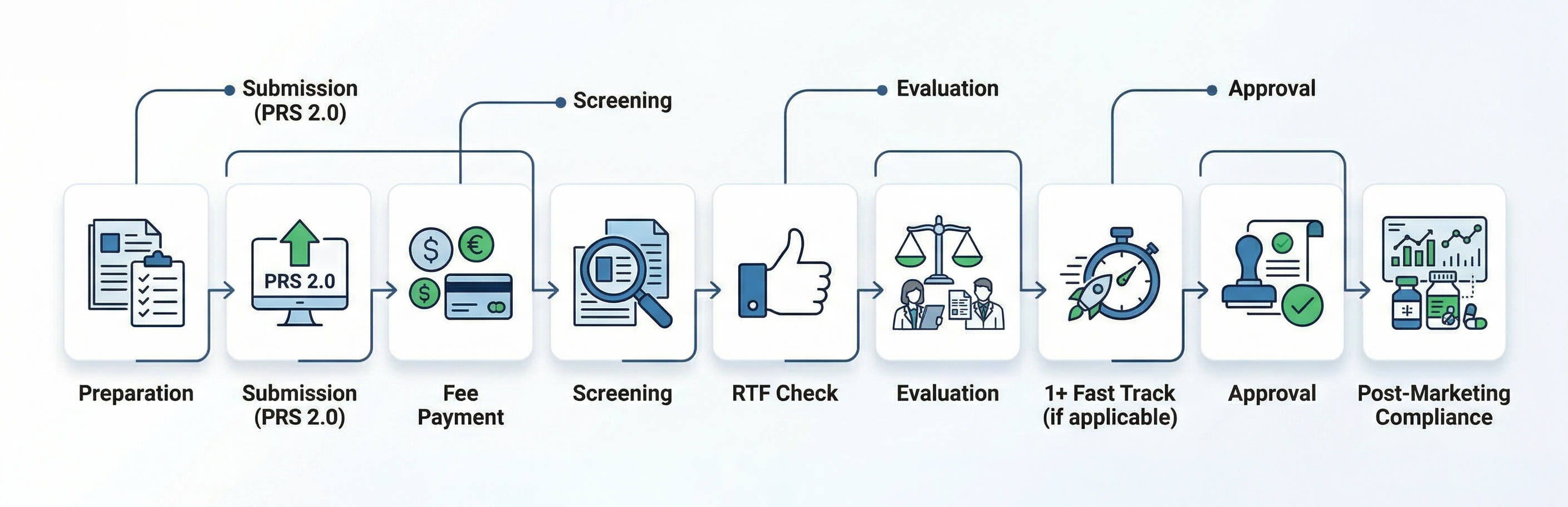
Como a Freyr Pode Ajudar
A Freyr oferece suporte End-to-End para o registo de medicamentos órfãos em Hong Kong, incluindo a preparação do dossiê, navegação no PRS 2.0 e conformidade pós-aprovação. Com experiência local e uma abordagem estratégica, ajudamos a garantir uma entrada no mercado mais rápida e em conformidade para medicamentos órfãos para doenças raras.









