
O mercado farmacêutico da Malásia é um polo em crescimento no Sudeste Asiático, oferecendo grandes oportunidades para empresas globais. Com uma procura crescente por cuidados de saúde de qualidade e um quadro regulamentar cada vez mais estruturado, o mercado farmacêutico da Malásia está a tornar-se um destino atraente tanto para fabricantes de medicamentos genéricos como para fabricantes de medicamentos inovadores.
Panorama do mercado da Malásia: Um panorama promissor no mercado farmacêutico da Malásia
Tanto os genéricos como as Novas Entidades Químicas (NCEs) apresentam fortes perspetivas no mercado farmacêutico da Malásia, um setor em rápido desenvolvimento no Sudeste Asiático. O país oferece um ambiente dinâmico para as empresas farmacêuticas, devido ao crescimento da sua população e ao aumento da procura de cuidados de saúde. O setor da saúde constitui um mercado lucrativo para os produtos farmacêuticos, uma vez que está bem estabelecido e dispõe de instalações médicas de primeira classe.
O mercado farmacêutico da Malásia caracteriza-se por uma procura crescente de novos medicamentos, especialmente em áreas terapêuticas como a diabetes, as doenças cardiovasculares e a oncologia. O ambiente regulatório tornou-se mais organizado, com regras precisas para a aprovação de produtos e a entrada no mercado, enquanto o governo continua a concentrar-se na melhoria dos cuidados de saúde públicos e no acesso aos medicamentos.
Processo de registo na Malásia:
O processo de registo de produtos farmacêuticos na Malásia é regulamentado pela Agência Nacional de Regulamentação Farmacêutica ( NPRA), que é responsável por garantir a segurança, a eficácia e a qualidade dos produtos farmacêuticos.
NPRA para o registo de produtos farmacêuticos estão em conformidade com as diretrizes e recomendações em matéria de qualidade, segurança e eficácia da Organização Mundial de Saúde (WHO) ou com outras normas internacionalmente aceites, como as da Conferência Internacional de Harmonização (ICH). As etapas principais do processo de registo são as seguintes:
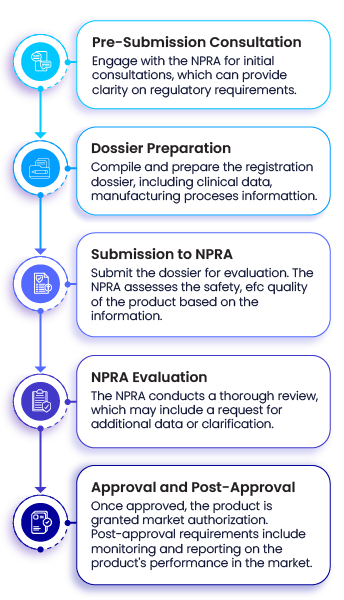
Requisitos regulamentares básicos:
Um produto farmacêutico deve cumprir várias condições regulamentares importantes para ser registado na Malásia:
- Boas Práticas de Fabrico (BPF): Para garantir que o produto cumpre os requisitos de qualidade, as instalações de fabrico têm de ser acreditadas pelas autoridades PIC/S .
- Dados clínicos: Para comprovar a segurança e a eficácia, os novos compostos farmacêuticos (NCEs) necessitam de dados de ensaios clínicos. No caso dos medicamentos genéricos, é necessário demonstrar a bioequivalência.
- Rotulagem e embalagem: É necessário respeitar a legislação local na rotulagem dos produtos, especialmente no que diz respeito ao idioma e às informações de segurança.
- Monografia do produto: É necessária uma descrição exaustiva dos ingredientes, da dosagem e das orientações de utilização do produto.
- Representação local: Normalmente, um agente ou representante local deve atuar como ponto de contacto NPRA. O requerente do registo do produto, designado por «Titular do Registo do Produto» (PRH), deve ser uma empresa constituída localmente, uma pessoa coletiva ou entidade jurídica, com endereço permanente e registada na Comissão de Empresas da Malásia (SSM) (com objeto social relacionado com produtos de saúde/farmacêuticos).
Estudo de caso da Freyr: Apoio a uma empresa farmacêutica sediada em Taiwan na sua entrada no mercado:
Visão geral do cliente: Uma empresa farmacêutica líder sediada em Taiwan procurou a Freyr para obter apoio end-to-end com vista ao lançamentoMedicamentos genéricos e NCE Medicamentos mercado farmacêutico da Malásia. O seu objetivo era garantir uma entrada atempada no mercado, superando simultaneamente as complexidades regulatórias.
Detalhes do projeto: O âmbito do trabalho da Freyr inclui uma gama completa de serviços de conformidade regulamentar:
- Estratégia e abordagem regulamentar: Foi desenvolvida uma estratégia que cumpre NPRA e é adaptada às necessidades do cliente para o lançamento do produto na Malásia.
- Análise técnica e análise de lacunas: Foi realizada uma análise exaustiva dos documentos de registo, com o objetivo de identificar eventuais lacunas e garantir a sua conformidade com os requisitos NPRA.
- Compilação e apresentação: Assegurei-me de que toda a documentação necessária estava completa e em conformidade com as normas regulamentares antes de compilar e apresentar o dossiê de registo à NPRA.
- Acompanhamento junto NPRA: Supervisionei a correspondência contínua com NPRA resolver quaisquer dúvidas ou pedidos adicionais, acelerando o processo de aprovação.
Resultado: Com a assistência da Freyr, o cliente conseguiu concluir com sucesso o processo de registo na Malásia. Os produtos foram aprovados rapidamente, permitindo uma entrada no mercado sem complicações, colmatando quaisquer lacunas técnicas e garantindo a apresentação da documentação adequada. Este caso destacou a competência da Freyr em Assuntos Regulamentares o seu papel na orientação eficaz no mercado farmacêutico da Malásia.
O cliente pôde concentrar-se nas suas principais atividades comerciais graças ao end-to-end da Freyr, que garantiu que todo o processo regulatório — desde a preparação do dossiê até à aprovação final — decorresse sem problemas.
Pronto para entrar no próspero mercado farmacêutico da Malásia?
O mercado farmacêutico da Malásia oferece um enorme potencial de crescimento. No entanto, lidar com o quadro regulamentar exige uma estratégia bem estruturada, documentação precisa e conhecimento do contexto local.
Ao estabelecer parcerias com prestadores de serviços regulatórios experientes, como a Freyr, as empresas farmacêuticas podem agilizar a sua entrada no mercado farmacêutico da Malásia, colmatar lacunas técnicas e obter aprovações mais rapidamente — abrindo caminho para novas oportunidades nesta região dinâmica.










