
Na indústria farmacêutica, a segurança do doente depende de um fator crucial: a consistência na qualidade do produto. Cada comprimido, frasco ou injeção que chega ao doente deve funcionar exatamente como previsto. Essa consistência é o resultado de uma rigorosa validação de processos (PV), regida por um sólido quadro de Garantia da Qualidade (QA).
A validação de processos é uma filosofia de qualidade que garante que os processos de fabrico sejam bem compreendidos, controlados e capazes de fornecer, de forma consistente, produtos que cumpram as especificações predefinidas. Do QA , a validação de processos passa de um mero exercício de conformidade para uma medida proativa de salvaguarda, tanto da integridade do produto como da saúde do doente.
O que é a validação de processos?
De acordo com as diretrizes FDA ICH , a validação de processos consiste na «recolha e avaliação de dados, desde a fase de conceção do processo até à produção comercial, que estabelece provas científicas de que um processo é capaz de fornecer produtos de qualidade de forma consistente».
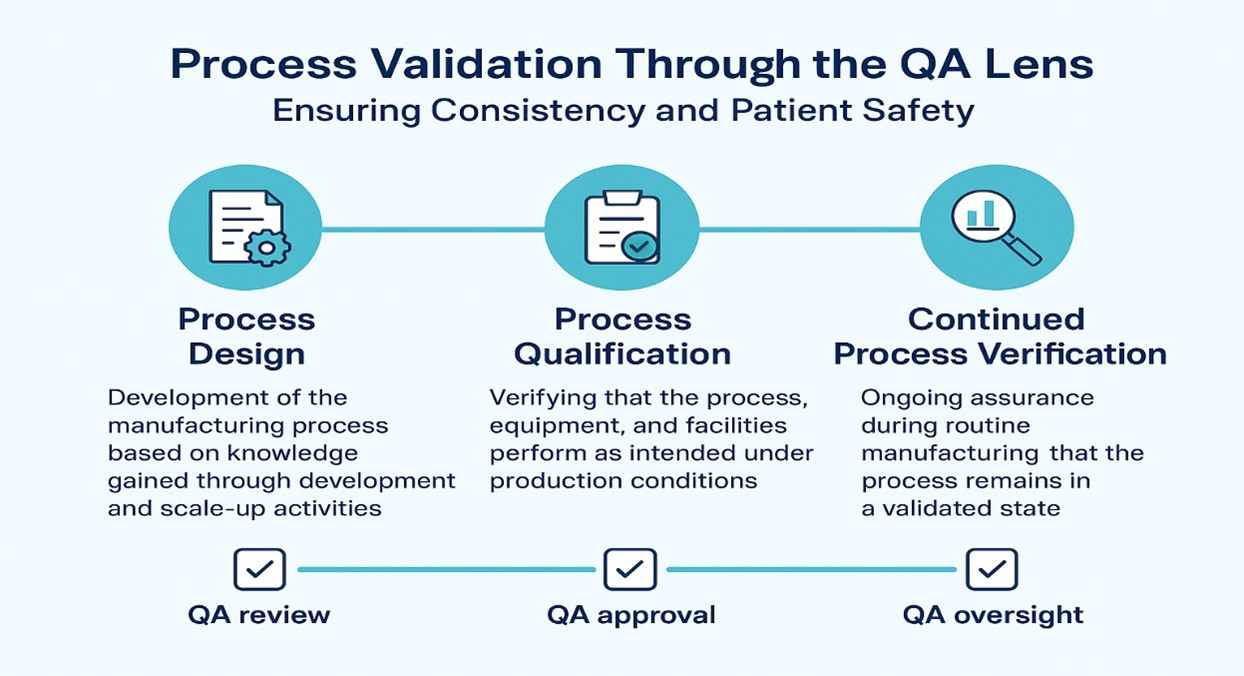
O ciclo de vida da validação inclui normalmente três (3) fases críticas:
- Fase 1 – Conceção do Processo:
Desenvolvimento do processo de fabrico com base nos conhecimentos adquiridos através de atividades de desenvolvimento e ampliação.
QAPapelQA: Assegurar a aplicação das avaliações de risco, dos controlos de conceção e dos princípios da qualidade por conceção (QbD). - Fase 2 – Qualificação do processo:
Verificar se o processo, o equipamento e as instalações funcionam conforme previsto em condições de produção.
QAFunçãoQA: Aprovar protocolos de qualificação, analisar desvios e garantir a integridade dos dados durante a execução. - Fase 3 – Verificação Contínua do Processo (CPV):
Garantia contínua, durante a produção de rotina, de que o processo se mantém num estado validado.
QAPapelQA: Implementação de análises de tendências, métricas de qualidade e sistemas CAPA para manter o controlo.
QA : Para além da documentação
Embora a validação de processos envolva avaliações técnicas e estatísticas, a QA garante que esta seja executada com rigor científico e em conformidade com os requisitos regulamentares. A responsabilidade QAabrange todas as fases, desde o planeamento e a aprovação do protocolo até à gestão de alterações e à verificação contínua.
- Abordagem baseada no risco
QA um papel fundamental na adoção de uma abordagem baseada no risco, tal como definida pela ICH . Os Parâmetros Críticos do Processo (CPPs) e os Atributos Críticos de Qualidade (CQAs) são identificados, avaliados e monitorizados para minimizar os riscos. QA que os protocolos de validação sejam estatisticamente sólidos e que os planos de mitigação de riscos sejam integrados na conceção.
- Integridade e rastreabilidade dos dados
Numa era transformação digital, a integridade dos dados continua a ser um dos principais focos do QA. Os princípios ALCOA+ (Atribuível, Legível, Contemporâneo, Original, Preciso, além de Completo, Consistente, Duradouro e Disponível) orientam todas as entradas e revisões de dados. QA que os dados de validação — desde a qualificação de equipamentos até aos registos de lotes — sejam rastreáveis, verificados e estejam em conformidade com 21 CFR Part 11 .
- Melhoria contínua através do CPV
Após a validação, QA o desempenho do processo utilizando o controlo estatístico de processos (SPC) e ferramentas de análise de tendências. Os desvios ou resultados fora da tendência desencadeiam ações corretivas e preventivas (CAPA) para melhorar continuamente a capacidade do processo. Este sistema de ciclo fechado reforça a conformidade a longo prazo e reduz a variabilidade do produto.
Expectativas regulatórias e normas internacionais
As entidades reguladoras de todo o mundo, incluindo aFDA US , EMA, MHRA e WHO, esperam que as empresas farmacêuticas demonstrem a validação dos processos através de uma abordagem centrada no ciclo de vida. QA o alinhamento com estas diretrizes em constante evolução, nomeadamente:
- FDA para a Indústria – Validação de Processos: Princípios e Práticas Gerais
- ICH (Desenvolvimento Farmacêutico), Q9 (Gestão de Riscos de Qualidade) e Q10 (Sistema de Qualidade Farmacêutica)
- Anexo 15 da UE – Qualificação e validação
Ao manter uma documentação harmonizada e a rastreabilidade, QA a preparação para as inspeções e a conformidade regulamentar a nível global, independentemente das variações regionais.
Desafios na validação de processos e QA
Desafio | Solução QA |
|---|---|
Dados inconsistentes entre lotes | Implementar registos eletrónicos de lotes (EBR) e pontos de verificação para a revisão QA |
Falta de fundamentação estatística na amostragem | QA o protocolo esteja em conformidade com os níveis de confiança estatística (por exemplo, intervalos de confiança de 95 %) |
Documentação insuficiente | QA sistemas de controlo de documentos e rastreabilidade SOP |
Desvios durante a validação | QA o tratamento de desvios, a análise das causas profundas e a implementação de CAPA |
Gestão do ciclo de vida | QA os programas de CPV e os critérios de revalidação estejam claramente definidos |
Transformação digital no QA a validação de processos
QA modernas QA estão a recorrer à automatização e a plataformas de validação digital para aumentar a eficiência e a precisão. Ferramentas como os Sistemas de Gestão do Ciclo de Vida da Validação (VLMS) permitem a colaboração em tempo real entre as equipas QA, produção e validação.
A experiência da Freyr em Validação de Sistemas Informáticos (CSV) e Garantia de Software Informático (CSA) ajuda os clientes a adotar estratégias de validação digital em conformidade com as normas, escaláveis e preparadas para inspeção. Isto garante não só a conformidade, mas também a excelência operacional e prazos mais curtos para o lançamento de produtos.
Construir confiança através da qualidade
A validação de processos é um compromisso contínuo com a qualidade, a segurança e a confiança dos doentes. Através QA , as empresas farmacêuticas podem garantir que os seus processos não só são validados, como também são continuamente melhorados para cumprir os mais elevados padrões globais.
Ao integrar QA todas as fases da validação de processos, as organizações reforçam o seu Sistema de Gestão da Qualidade (SGQ), reduzem o risco regulamentar e cumprem a sua promessa fundamental: produtos seguros e eficazes para os doentes em todo o mundo.
Na Freyr, a nossa equipa de especialistas QA validação colabora com empresas farmacêuticas globais para estabelecer estruturas de validação robustas, em conformidade com as normas e preparadas para inspeções. Desde a correção do Sistema de Gestão da Qualidade (SGQ) e o desenvolvimento de estratégias de validação de processos até QA digital QA , a Freyr garante um alinhamento regulamentar perfeito e excelência operacional.
Descubra como a Freyr pode ajudá-lo a alcançar a excelência em validação.










