
No cenário altamente regulamentado da indústria das Ciências da Vida, a adesão às Diretrizes Específicas do Produto (PSGs) é primordial para o desenvolvimento e aprovação bem-sucedidos de medicamentos. As PSGs são documentos abrangentes emitidos por Autoridades de Saúde (HAs) globais para fornecer orientação para as aprovações de produtos farmacêuticos dentro de categorias terapêuticas específicas.
Este blog detalha o propósito, a relevância e a perspetiva da HA sobre a emissão de PSGs. A compreensão da lógica e das expectativas estabelecidas nos PSGs, que permitem o sucesso estratégico das empresas de ciências da vida, é detalhada neste artigo.
Compreender as Orientações Específicas do Produto e os seus Tipos
As Orientações Específicas do Produto desempenham um papel fundamental na definição do percurso regulamentar para produtos farmacêuticos. Ao fornecer orientação direcionada, as Autoridades de Saúde garantem a consistência e avaliações robustas das submissões de produtos dentro de categorias terapêuticas específicas. Ao aderir às Orientações Específicas do Produto, as empresas farmacêuticas podem navegar no complexo panorama regulamentar, garantindo que os seus produtos cumprem os padrões de segurança e eficácia exigidos.
As Orientações Específicas do Produto não se limitam ao desenvolvimento de medicamentos genéricos. Abrangem também uma vasta gama de produtos farmacêuticos, tais como os seguintes:
- Para Medicamentos Inovadores: Os PSGs fornecem orientações específicas sobre estudos pré-clínicos, desenho de ensaios clínicos, avaliação de segurança, farmacocinética e parâmetros de eficácia. Eles orientam as empresas sobre o tipo e a quantidade de dados necessários para demonstrar a segurança e a eficácia dos seus medicamentos inovadores.
- Para Biossimilares: Os PSGs (Princípios de Orientação Específicos) descrevem os requisitos de dados, métodos analíticos e considerações de desenho de estudos clínicos para produtos biossimilares. Ao segui-los, as empresas de biossimilares podem demonstrar a semelhança dos seus produtos com o medicamento biológico de referência, abrindo caminho para a aprovação e o acesso ao mercado.
- Para Produtos Biológicos: Estas diretrizes abordam aspetos críticos, como o fabrico, a caracterização e os estudos de comparabilidade, garantindo que os produtos biológicos cumprem os padrões aprovados.
Desenvolvimento de Diretrizes e Processos Específicos do Produto
O desenvolvimento de PSGs é um esforço colaborativo que envolve Autoridades de Saúde (HAs), especialistas científicos e partes interessadas da indústria. As seguintes são as fases de desenvolvimento dos PSGs:
Etapa 1 - Avaliação abrangente da área terapêutica: As Autoridades de Saúde (AS) identificam lacunas nas diretrizes existentes e iniciam o desenvolvimento de PSGs para abordar essas lacunas. Especialistas científicos e partes interessadas da indústria são então envolvidos para contribuir com a sua experiência, garantindo que as diretrizes preliminares sejam baseadas em evidências e práticas de implementar.
Etapa 2 - Consulta Pública: Os PSGs preliminares estão agora disponíveis para revisão pública e feedback. Esta abordagem aberta e transparente permite que as partes interessadas, incluindo Profissionais de Saúde (HCPs), grupos de pacientes e representantes da indústria, forneçam contributos valiosos e melhorem a qualidade e relevância gerais das diretrizes.
Etapa 3: Fase de Revisão Interna: Enquanto os PSGs preliminares estão em consulta pública, a equipa de desenvolvimento de PSGs dentro das Autoridades de Saúde (AS) realiza uma revisão interna rigorosa, garantindo que as diretrizes cumprem os requisitos de Regulamentação necessários e se alinham com o quadro de Regulamentação mais amplo.
Etapa 4 - Finalização: Uma vez finalizados, os PSGs são publicados e tornados acessíveis à indústria, fornecendo orientação clara e acionável para o desenvolvimento e submissão de produtos.
Componentes dos PSGs
As empresas de ciências da vida devem ter uma compreensão clara dos componentes dos PSGs. O gráfico circular seguinte ilustra-os em detalhe:
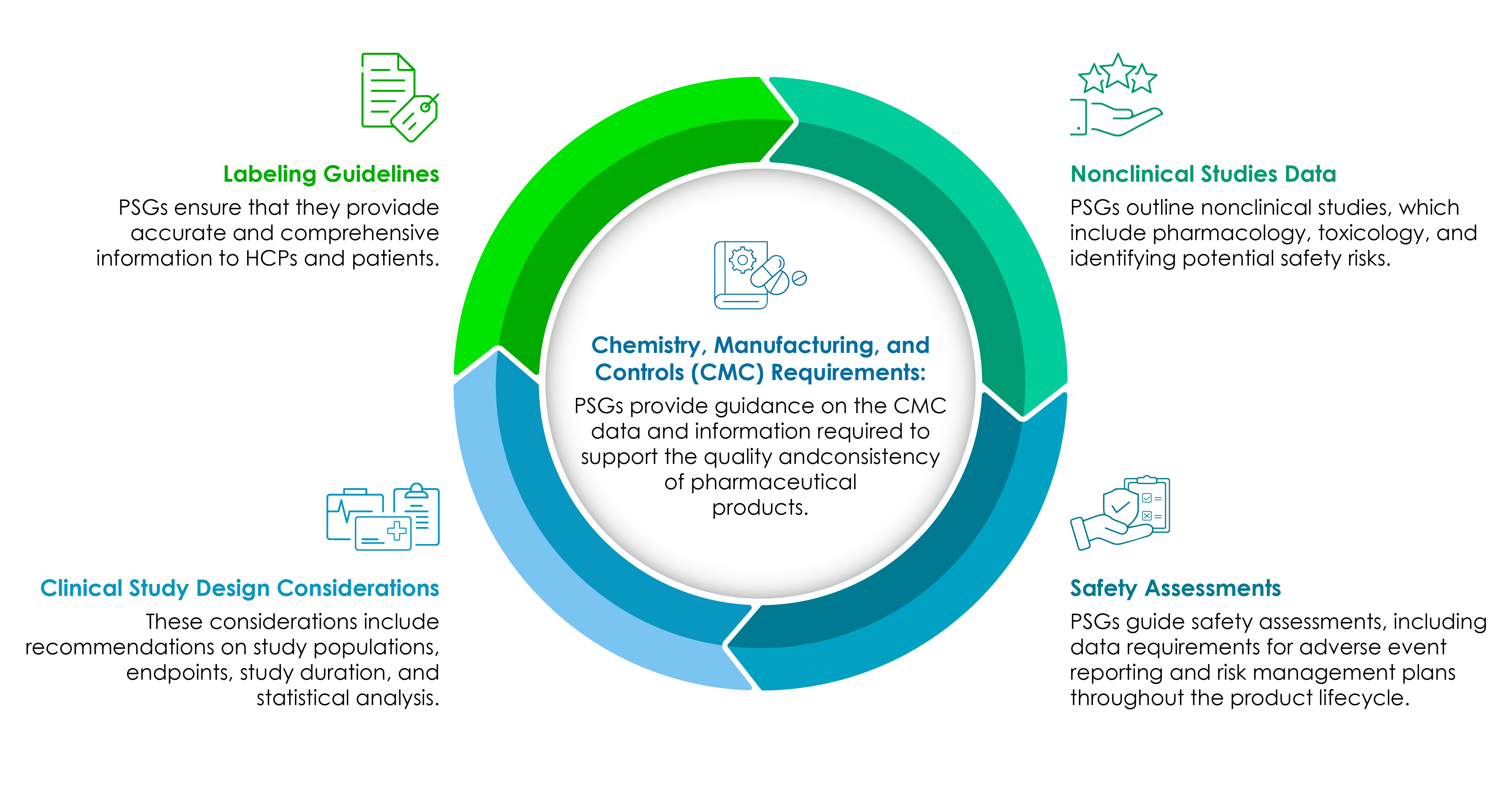
A CMC continua a ser o ponto central de cada desenvolvimento de produto farmacêutico com enfoque regulamentar.
Gerir os PSGs
Gerir os PSGs em conformidade regulamentar pode ser alcançado através dos seguintes pontos/estratégias listados:
- Envolvimento Precoce com as Autoridades de Saúde: Este envolvimento promove uma abordagem colaborativa e ajuda a abordar proativamente os desafios potenciais.
- Experiência Científica: A utilização de conhecimentos especializados garante que os desenhos de estudo, os métodos analíticos e as avaliações de segurança estejam alinhados com os mais elevados padrões científicos.
- Consultores de Regulamentação: Os consultores fornecem orientação especializada, garantindo que os planos de desenvolvimento e as submissões regulamentares sejam bem-sucedidos.
- Revisão Abrangente de PSG: As empresas devem identificar as secções específicas do PSG aplicáveis ao seu produto e alinhar os seus planos de desenvolvimento em conformidade.
- Monitorização Contínua: Os PSGs são documentos dinâmicos que podem ser atualizados ou revistos frequentemente. As empresas devem monitorizar as alterações nos PSGs para garantir a conformidade regulamentar com os requisitos mais recentes dos PSGs.
A orientação regulamentar especializada facilita a navegação no PSG. Consulte agora!
Conclusão
As Diretrizes Específicas do Produto (PSGs) constituem a base das submissões regulamentares para produtos farmacêuticos em categorias terapêuticas específicas. Compreender as perspetivas da HA por trás da emissão das PSGs é fundamental para empresas de ciências da vida que procuram acelerar as aprovações, garantir a qualidade do produto e navegar pelo panorama regulamentar global sem problemas.
Como fornecedor líder de serviços regulamentares, a Freyr reconhece a importância de aderir às melhores práticas e de alavancar a experiência que irá guiar as empresas de ciências da vida a alinhar as suas estratégias de desenvolvimento de produtos de acordo com os requisitos do PSG. Contacte-nos hoje para saber mais sobre os nossos serviços e como o podemos ajudar a alcançar os seus objetivos.









