
Os produtos combinados, que integram medicamentos, dispositivos e/ou produtos biológicos, revolucionaram os cuidados de saúde ao oferecer soluções terapêuticas inovadoras. No entanto, a sua natureza única apresenta desafios regulamentares significativos. Este guia abrangente explora o intrincado panorama da regulamentação de produtos combinados e fornece estratégias para navegar com sucesso nestes percursos complexos.
Compreensão dos Produtos Combinados e do Seu Quadro Regulamentar
Os produtos combinados são produtos médicos que combinam dois (2) ou mais componentes regulamentados – medicamentos, dispositivos ou produtos biológicos – numa única entidade. Estes produtos inovadores podem assumir várias formas, como stents farmacológicos, seringas pré-cheias ou adesivos transdérmicos. O quadro de regulamentação para produtos combinados é principalmente regido pela U.S. Food and Drug Administration (FDA) nos Estados Unidos, com abordagens semelhantes adotadas por organismos de regulamentação em todo o mundo.
O Gabinete de Produtos Combinados (OCP) da FDA desempenha um papel crucial na determinação do modo de ação primário (PMOA) de um produto combinado, que determina o processo regulamentar e o centro principal da FDA responsável pela revisão. O Centro de Avaliação e Investigação de Medicamentos (CDER), o Centro de Dispositivos e Saúde Radiológica (CDRH) e o Centro de Avaliação e Investigação de Produtos Biológicos (CBER) colaboram no processo de revisão, enfatizando a necessidade de uma abordagem integrada para garantir a segurança e eficácia dos produtos combinados.
Determinação do Percurso Regulamentar
Um (1) dos passos mais críticos no desenvolvimento de uma estratégia regulamentar para produtos combinados é determinar o percurso regulamentar adequado. Esta decisão baseia-se principalmente no PMOA do produto. Aqui estão as principais considerações:
- Modo de Ação Primário (PMOA): Identificar o modo de ação único que proporciona a ação terapêutica mais importante do produto combinado.
- Atribuição ao Centro Principal: Com base no PMOA, o produto será atribuído ao CDER, CDRH ou CBER para revisão primária.
- Tipo de Submissão Regulamentar: Dependendo do centro principal, a submissão pode assumir a forma de uma submissão de Novo Medicamento (NDA), submissão de Licença para Produtos Biológicos (BLA) ou Aprovação Pré-Comercialização (PMA).
- Pedido de Designação (RFD): Se o PMOA não for claro, os promotores podem submeter um RFD ao OCP para uma determinação formal.
- Pré-Pedido de Designação (Pre-RFD): O OCP pode receber um Pré-RFD para feedback informal e não vinculativo sobre questões de classificação e jurisdição.
Compreender estes fatores é crucial para desenvolver uma estratégia regulamentar eficaz adaptada ao seu produto combinado específico.
Navegação nos Processos de Revisão Pré-Comercialização
O processo de revisão pré-comercialização para produtos combinados pode ser complexo, exigindo um planeamento e execução cuidadosos. Aqui estão as principais estratégias para navegar neste processo de forma eficaz:
- Envolvimento Precoce com os Reguladores: Inicie discussões com a FDA no início do processo de desenvolvimento através de reuniões de pré-submissão. Estas interações podem fornecer orientações valiosas sobre os requisitos regulamentares, desenhos de estudo e potenciais desafios.
- Plano de Desenvolvimento Abrangente: Desenvolver um plano robusto que aborde os aspetos únicos do seu produto combinado, incluindo como as partes constituintes interagem e os seus efeitos combinados na segurança e eficácia.
- Abordagem de Testes Integrada: Conceber estudos pré-clínicos e clínicos que avaliem os componentes individuais e o produto combinado completo. Esta abordagem deve avaliar potenciais interações e efeitos cumulativos.
- Considerações sobre o Sistema de Qualidade: Implementar um sistema de qualidade que esteja em conformidade com os regulamentos de medicamentos (21 CFR 210/211) e dispositivos (21 CFR 820), conforme apropriado para o seu produto.
- Engenharia de Fatores Humanos: Incorporar estudos de fatores humanos para avaliar as interações do utilizador com o produto combinado, garantindo uma utilização segura e eficaz.
- Gestão de Risco: Desenvolver um plano de gestão de risco abrangente que aborde os riscos potenciais associados a cada componente e à sua combinação.
Ao adotar estas estratégias, os promotores podem otimizar o processo de revisão pré-comercialização e aumentar a probabilidade de sucesso regulamentar.
Abordagem dos Desafios Pós-Comercialização
As responsabilidades regulamentares para produtos de combinação estendem-se para além da aprovação de mercado. Uma vigilância pós-comercialização e conformidade eficazes são cruciais para o sucesso a longo prazo. Considere as seguintes estratégias:
- Farmacovigilância Integrada: Implementar um sistema de farmacovigilância robusto que capte eventos adversos relacionados com os componentes de medicamento e dispositivo do produto combinado.
- Estudos Pós-Comercialização: Planear e conduzir estudos pós-comercialização para recolher dados adicionais de segurança e eficácia, especialmente para produtos combinados inovadores.
- Manutenção do Sistema de Qualidade: Atualize e mantenha continuamente o seu sistema de qualidade para garantir a conformidade com as regulamentações relevantes para componentes de medicamentos e dispositivos.
- Gestão de Alterações: Estabeleça um processo simples para gerir alterações pós-aprovação, considerando o impacto potencial nos aspetos de medicamento e dispositivo do produto.
- Inteligência Regulatória: Mantenha-se informado sobre a evolução das regulamentações e documentos de orientação relacionados com produtos de combinação para garantir a conformidade contínua.
Ao abordar proativamente estes desafios pós-comercialização, os fabricantes podem manter a conformidade Regulatória e a segurança do produto ao longo de todo o ciclo de vida do produto.
Considerações Regulatórias Globais
À medida que o mercado de produtos de combinação se expande globalmente, a compreensão dos requisitos Regulatórios internacionais torna-se cada vez mais importante. Considere estas estratégias para o sucesso Regulatório global:
- Harmonização Regulatória: Aproveite os esforços de harmonização internacional, como os do Fórum Internacional de Reguladores de Dispositivos Médicos (IMDRF), para otimizar as submissões Regulatórias globais.
- Requisitos Específicos do Mercado: Pesquise e compreenda os requisitos específicos para produtos de combinação nos mercados-alvo, uma vez que as regulamentações variam significativamente entre os países.
- Submissões Simultâneas: Considere submissões simultâneas a múltiplas agências Regulatórias para acelerar o acesso ao mercado global, quando apropriado.
- Ensaios Clínicos Globais: Desenhe ensaios clínicos que cumpram os requisitos de múltiplas agências Regulatórias para apoiar as submissões de comercialização global.
- Parcerias Internacionais: Colabore com especialistas Regulatórios locais ou parceiros nos mercados-alvo para navegar pelas regulamentações específicas de cada país e considerações culturais.
Ao adotar uma perspetiva global no desenvolvimento de estratégias de regulamentação, os fabricantes podem expandir o seu alcance de mercado para produtos combinados de forma mais eficaz.
Conclusão
Navegar pelos percursos Regulatórios para produtos de combinação requer uma compreensão abrangente de estruturas Regulatórias complexas e planeamento estratégico.
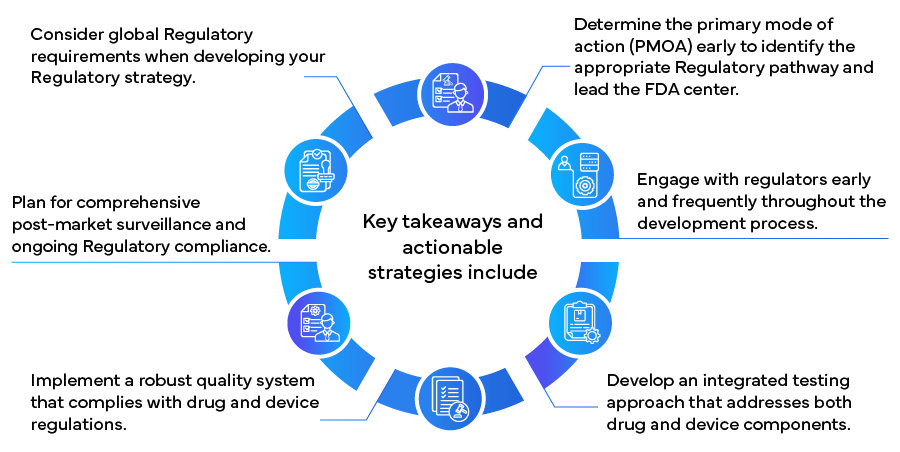
Ao implementar estas estratégias, os fabricantes podem navegar de forma mais eficaz no complexo panorama Regulatório para produtos de combinação, potencialmente acelerando o tempo de chegada ao mercado e garantindo a conformidade e o sucesso a longo prazo. À medida que o campo dos produtos de combinação continua a evoluir, manter-se informado sobre as alterações Regulatórias e manter a flexibilidade nas abordagens Regulatórias será crucial para o sucesso contínuo neste setor de saúde inovador e em rápido crescimento.









