Enquanto os produtos farmacêuticos inovadores ou de marca acarretam custos adicionais associados à investigação e desenvolvimento do produto, desde a fase de identificação da molécula até à autorização pós-comercialização, os produtos farmacêuticos genéricos são relativamente económicos. Estas terapias não só reduzem o custo global do tratamento, como também melhoram significativamente o acesso dos pacientes a medicamentos que salvam vidas. Uma vez que a dependência da importação de antibióticos genéricos e da terapia medicamentosa para doenças raras afetou a disponibilidade destes produtos farmacêuticos a nível global durante a pandemia, as agências de saúde estão a introduzir novas diretrizes para apoiar os fabricantes locais de medicamentos.
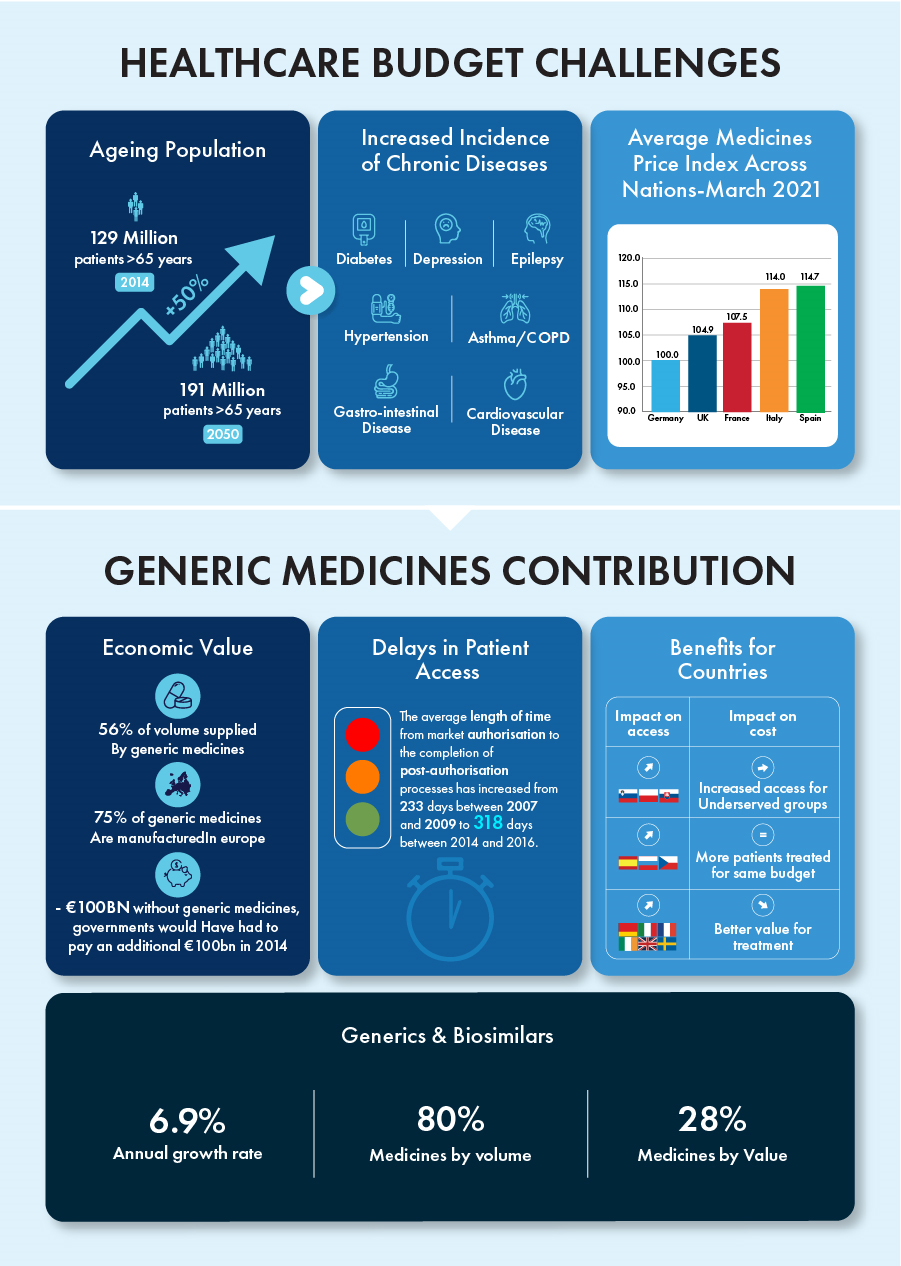
Desde 1993, a organização comercial Medicines for Europe, anteriormente conhecida como European Generics Medicine Association (EGA), tem sido consistente com o seu objetivo de familiarizar a população de pacientes europeus com terapias económicas. Na última década, forneceram com sucesso 67% de todos os medicamentos à Europa, ampliando o acesso dos pacientes a 100% em sete (07) áreas terapêuticas chave. No âmbito das autoridades de saúde europeias, uma “autonomia estratégica” pós-Brexit desencadeou a necessidade imediata de remediar eficazmente a desvantagem competitiva enfrentada pelos fabricantes europeus de genéricos e biossimilares. Com o advento da pandemia de COVID-19, as capacidades da cadeia de abastecimento global sucumbiram sob a pressão da procura de medicamentos. Medicamentos que salvam vidas e que proporcionavam alívio para doenças crónicas desapareceram das prateleiras das farmácias locais. Para superar os obstáculos relacionados com produtos farmacêuticos protegidos por patente e construir capacidade de fabrico local de medicamentos para melhorar o acesso dos pacientes, o Conselho da UE adotou um regulamento que prevê uma exceção a uma molécula original, concedendo um Certificado Complementar de Proteção (SPC). Esta disposição facilita o fabrico de genéricos e biossimilares antes da expiração da patente para fins de armazenamento ou exportação. No entanto, a exceção será aplicável apenas nas seguintes circunstâncias.
- Os genéricos ou biossimilares produzidos destinam-se exclusivamente à exportação para outro país onde a patente da molécula do medicamento não existe ou expirou, ou para fins de armazenamento dentro do prazo remanescente da patente de seis (06) meses.
- Conforme o requisito, o fabricante transmitiu a informação à Autoridade de Saúde local e ao titular do SPC antes de três (03) meses.
- O fabricante informou todas as partes interessadas na comercialização do produto.
- O fabricante garantiu que os requisitos de rotulagem indicam que o produto farmacêutico se destina apenas a fins de exportação.
De Facto
Desde a concessão da Autorização de Introdução no Mercado condicional para produtos de vacinas COVID-19 na UE, o Comité de Medicamentos para Uso Humano (CHMP) da Agência Europeia de Medicamentos autorizou quatro (04) locais para a produção de vacinas num ano; dois (02) na Suíça e dois (02) nos EUA. Tais decisões a favor da expansão dos locais de produção irão melhorar as capacidades de fabrico de vacinas, tornando-as mais acessíveis à população europeia.
Os genéricos e biossimilares contribuíram, por si só, para uma taxa de crescimento anual de 6,9%, representando 80% de todos os medicamentos em volume e 28% em valor na última década. O prazo de patente para certos produtos biológicos avaliados em cerca de 90 mil milhões de euros terminará até 2023, criando um ambiente competitivo para estes produtos com um enorme potencial de crescimento.
A implementação de uma derrogação do SPC beneficiaria a União Europeia ao:
- Adicionar aproximadamente 90,5 mil milhões de euros adicionais por ano.
- Gerar vinte e cinco mil (25.000) novas oportunidades de emprego com dois mil (2.000) empregos diretos para a indústria de API da UE. A iniciativa ajudará os estados membros da UE a poupar 3,1 mil milhões de euros em despesas de saúde.
- Armazenar alternativas mais baratas de medicamentos inovadores patenteados para permitir a sua entrada no mercado imediatamente após a expiração da Propriedade Intelectual (PI), melhorando o acesso dos pacientes.
Para um fabricante de medicamentos sediado na União Europeia, a implementação da isenção do SPC é uma das iniciativas mais gratificantes a favor dos genéricos. Uma vez que a Autoridade de Saúde da UE regulamenta medicamentos para uso humano e veterinário através de um procedimento centralizado ou descentralizado, navegar pelos requisitos locais específicos pode ser avassalador. Um especialista, ciente dos requisitos locais relativos a várias submissões e documentos de licença, pode ajudá-lo a focar os seus esforços em protocolos de produção essenciais, em vez de se fixar em complexos obstáculos regulamentares. Reimagine o seu potencial de negócio ao experienciar conformidade e qualidade. Contacte a Freyr.









