
Na indústria farmacêutica, a conformidade com as normas regulamentares não é apenas um requisito legal; é um componente crítico da segurança do paciente e da qualidade do produto. Um dos aspetos mais significativos para manter a conformidade é a gestão eficaz dos desvios. Os desvios, que podem ocorrer em qualquer fase do negócio farmacêutico, desde o fabrico à distribuição, são desvios dos procedimentos ou normas estabelecidos. Uma gestão adequada dos desvios é essencial para garantir que os produtos farmacêuticos são seguros, eficazes e de alta qualidade.
Compreender a Gestão de Desvios
A gestão de desvios é uma abordagem sistemática para lidar com eventos inesperados que podem, potencialmente, impactar a qualidade do produto ou a segurança do paciente. Envolve a documentação, investigação e correção destes eventos, bem como a implementação de medidas para prevenir a sua recorrência. Este processo é parte integrante do Sistema de Gestão da Qualidade (QMS) de uma empresa farmacêutica e é escrutinado durante auditorias e inspeções.
Etapas na Gestão de Desvios
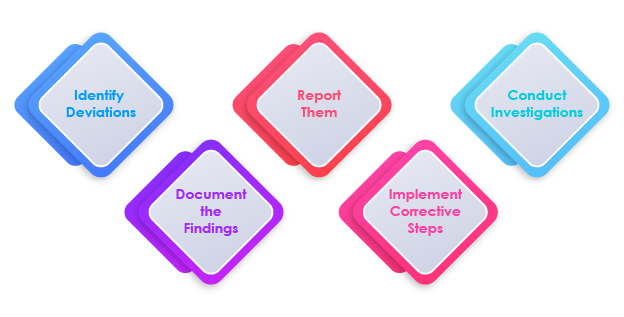
O Papel da Gestão de Desvios na Conformidade
As diretrizes de organismos reguladores como a FDA e a EMA enfatizam a importância de uma abordagem de gestão da qualidade baseada no risco. Esta abordagem foca-se em processos críticos que protegem os participantes humanos e garantem a integridade dos dados do estudo. A gestão de desvios desempenha um papel crucial nisto, identificando, avaliando e mitigando riscos potenciais para a qualidade do estudo.
Impacto nas Auditorias e Inspeções
Durante auditorias e inspeções, a gestão de desvios é uma área fundamental de foco. Os auditores examinam como os desvios são documentados, investigados e resolvidos. Avaliam também a eficácia das ações corretivas e preventivas (CAPAs). Um sistema robusto de gestão de desvios demonstra o compromisso de uma empresa com a conformidade e a melhoria contínua, o que pode influenciar positivamente os resultados das auditorias.
Validação de Serviços e Gestão de Desvios
A validação é o processo de garantir que os sistemas e processos de fabrico produzem consistentemente resultados que cumprem as especificações predeterminadas. Os desvios observados durante a validação devem ser minuciosamente investigados para determinar o seu impacto no resultado da validação. A gestão adequada destes desvios é crucial para que o processo de validação seja considerado fiável e para que os sistemas e processos sejam aprovados para utilização.
Acelerar o Desenvolvimento e a Aprovação
Ao seguir as recomendações regulamentares sobre a gestão de desvios, as empresas farmacêuticas podem acelerar o desenvolvimento e a aprovação de novos medicamentos e produtos biológicos. Isto porque um sistema de gestão de desvios bem gerido pode identificar e retificar rapidamente os problemas, reduzindo assim os atrasos no cronograma de desenvolvimento e garantindo que as inovações chegam mais rapidamente aos pacientes.
Aprendizagem e Melhoria Contínuas
A gestão de desvios não se trata apenas de resolver problemas imediatos; trata-se também de aprender com eles. A aprendizagem contínua através da recolha e análise de dados é vital para melhorar os sistemas de qualidade da indústria farmacêutica. Ao compreender as causas-raiz dos desvios, as empresas podem implementar medidas preventivas mais eficazes, melhorando a qualidade e a segurança gerais dos produtos.
Conclusão
A gestão adequada dos desvios é um pilar fundamental dos serviços de conformidade, auditoria e validação farmacêutica. Garante que as empresas farmacêuticas podem manter os mais elevados padrões de qualidade do produto e segurança do paciente. Ao gerir eficazmente os desvios, as empresas cumprem os requisitos regulamentares e contribuem para a confiança dos prestadores de cuidados de saúde, pacientes e autoridades reguladoras. À medida que a indústria farmacêutica continua a evoluir, a importância de sistemas robustos de gestão de desvios só aumentará, sublinhando ainda mais o seu papel crítico no ciclo de vida dos produtos farmacêuticos.










