
As Autorizações de Uso de Emergência (EUAs) são importantes para disponibilizar Medicamentos que salvam vidas aos pacientes mais rapidamente. Têm sido úteis no combate a pandemias como a COVID-19. Uma iniciativa da United States Food and Drug Administration (USFDA) iniciada no ano de 2004, a EUA entrou em vigor quando a Secção 564 do Federal Food, Drug, and Cosmetic Act foi alterada pelo Project BioShield Act. Este programa é um passo dado pela FDA para proteger a saúde pública, garantindo a segurança, eficácia e qualidade dos produtos médicos, ao mesmo tempo que aborda emergências médicas e ameaças emergentes à saúde pública.
Vamos entender melhor nas linhas seguintes.
Descodificar a EUA
A via da EUA é um meio para facilitar a acessibilidade de contramedidas médicas em tempos de emergências declaradas. O Comissário da FDA pode autorizar o seguinte em tais situações:
- O uso autorizado de produtos médicos não aprovados.
- O uso não autorizado de produtos médicos aprovados.
Os produtos abrangidos pela EUA incluem vacinas, fluidos IV, medicamentos, dispositivos, testes, etc., e podem ser utilizados para diagnosticar, tratar ou prevenir condições que ponham a vida em risco. Os produtos recebem a EUA se os seguintes critérios forem cumpridos:
- Prova de uma condição/doença que ponha a vida em risco.
- Os dados científicos fornecem provas suficientes de que o produto é eficaz para o uso a que se destina.
- Os benefícios do produto superam os riscos (ou seja, evidência de segurança).
- Falta de produtos alternativos.
Aconselha-se os patrocinadores a compreenderem os requisitos da FDA com antecedência para que sigam o melhor processo regulamentar e garantam uma submissão EUA sem erros. A seguir, encontra-se a informação obrigatória que deve ser partilhada pelo patrocinador na submissão.
Dados a Serem Submetidos pelo Patrocinador à FDA para uma Aprovação EUA
- Descrição do produto e o seu uso pretendido.
- O estado de aprovação do produto junto da FDA.
- Informações de segurança e eficácia, como dados clínicos e não clínicos, etc.
- Relatório de análise risco-benefício.
- Dados de Química, Fabrico e Controlo (CMC).
- Informações sobre a dosagem, contraindicações, advertências e eventos adversos para a distribuição do produto médico em questão.
Como são Emitidas as EUAs pela FDA?
Abaixo encontra-se uma interpretação diagramática do ciclo de vida da EUA, em resumo:
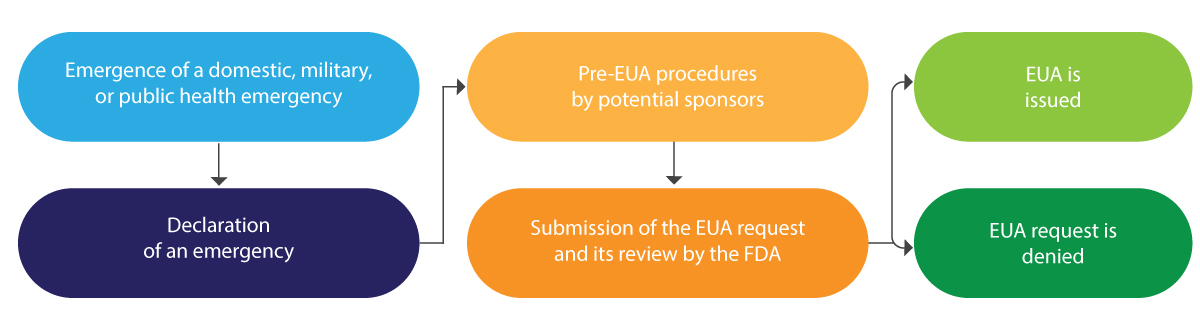
A EUA é tipicamente emitida por um período limitado e, no final da referida emergência, é terminada pela FDA.
EUA e COVID-19
O Secretário de Saúde e Ciências Humanas (HHS) declarou a COVID-19 como uma pandemia em 31 de janeiro de 2020. Desde então, a FDA tem sido fundamental na aprovação de algumas vacinas e kits de teste domésticos sob a via EUA para lidar com o surto global em curso.
Com o surgimento de novas variantes da COVID-19, toda a indústria farmacêutica está a trabalhar arduamente para conter a propagação e reduzir as taxas de mortalidade. Há uma necessidade de novos Medicamentos e aprovações mais rápidas pelas Autoridades Regulamentares globais, para que o seu tempo de colocação no mercado seja reduzido. A via EUA para o registo de novos Medicamentos/fármacos é o caminho a seguir, de acordo com os especialistas. Várias outras Autoridades de Saúde, como a Agência Europeia de Medicamentos (EMA), a Central Drugs Standard Control Organization (CDSCO), a Saudi Food and Drug Authority (SFDA), etc., também implementaram a via EUA para aprovações mais rápidas.
Se for um fabricante de medicamentos e procura uma EUA para o seu produto que salva vidas, precisará de um fornecedor de soluções Regulamentares experiente. Contacte a Freyr para um tempo de colocação no mercado mais rápido e um caminho em conformidade.










