
O Programa de Auditoria Única de Dispositivos Médicos (MDSAP) permite que uma Organização de Auditoria (OA) reconhecida realize uma única auditoria ao Sistema de Gestão da Qualidade (SGQ) de um fabricante de dispositivos médicos. Fornece requisitos regulamentares relevantes para cinco países, ou seja, Brasil (ANVISA), EUA (FDA), Japão (PMDA), Canadá (Health Canada) e Austrália (TGA). Além das autoridades regulamentares participantes, vários outros parceiros internacionais (os observadores oficiais e membros afiliados) estão envolvidos no MDSAP.
A certificação MDSAP é obrigatória pela Health Canada para dispositivos de Classe II, III e IV, mas é voluntária para os outros quatro países. Promoveu a transparência e o alinhamento regulamentar entre as autoridades participantes e minimizou a necessidade de múltiplas auditorias, poupando assim tempo e recursos aos fabricantes de dispositivos médicos. Para lhe dar uma melhor perspetiva sobre o programa MDSAP, tentámos aqui abordar as quinze (15) perguntas mais frequentes.
- Por que foi o Programa MDSAP desenvolvido quando existe uma certificação ISO 13485 globalmente aceite?
O MDSAP foi desenvolvido para reduzir o ónus das auditorias regulamentares para os fabricantes de dispositivos médicos e para promover um maior alinhamento das abordagens regulamentares e dos requisitos técnicos com base em normas internacionais e melhores práticas. Foca-se em trazer consistência, previsibilidade e transparência aos programas regulamentares, padronizando os procedimentos e as práticas dos reguladores e das organizações de auditoria de terceiros.
A auditoria baseia-se nos requisitos do Sistema de Gestão da Qualidade (SGQ) ao abrigo da ISO 13485 e nos requisitos regulamentares do país participante onde os dispositivos médicos serão comercializados.
- Quais são os critérios de elegibilidade para ser submetido a uma auditoria MDSAP?
Qualquer fabricante de dispositivos médicos que pretenda comercializar o seu dispositivo nos países participantes pode submeter-se a uma auditoria MDSAP. No entanto, cada Autoridade Regulamentar pode estabelecer critérios de exclusão para determinadas condições, se necessário.
Por exemplo, no Japão, as exceções para elegibilidade são:
- Um Local de Fabrico Registado (RMS) que fabrica dispositivos médicos feitos de tecidos humanos/animais
- Um RMS que fabrica IVDs radioativos, e
- A designação de um Autorização de Introdução no Mercado (MAH)
- A auditoria MDSAP inclui produtos combinados?
Dispositivos médicos que incluem medicamentos (substâncias medicinais) ou produtos biológicos (por exemplo, materiais de origem animal que foram tornados não viáveis, ou tecidos, células, ou substâncias de origem microbiana ou recombinante, sangue humano ou extratos de sangue humano ou produtos sanguíneos, etc.) são considerados produtos combinados e podem ser incluídos no âmbito de uma auditoria MDSAP.
No entanto, devido a diferenças na forma como estes produtos são regulamentados nas jurisdições das Autoridades Regulamentares participantes, os relatórios de auditoria MDSAP e os documentos de certificação podem não ser considerados uma alternativa aos requisitos de inspeção e avaliação em algumas jurisdições.
Austrália- Os produtos combinados estão sujeitos a um exame externo da TGA ao abrigo da Avaliação de Conformidade Australiana. Mas uma auditoria MDSAP eficaz pode reduzir as inspeções para estes dispositivos.
Brasil, Japão- Produtos combinados considerados dispositivos médicos estão incluídos no MDSAP, uma vez que não existem requisitos específicos relativos ao QMS.
Canadá- O modelo MDSAP abrange os requisitos de QMS para produtos combinados considerados dispositivos médicos.
EUA- As auditorias MDSAP não são consideradas alternativas às inspeções da FDA para produtos combinados.
- Posso selecionar o país abrangido pela auditoria MDSAP?
Sim, a auditoria é realizada de acordo com o âmbito declarado na submissão de serviços de certificação. Espera-se que os fabricantes de dispositivos médicos estejam em conformidade com os regulamentos apenas nas jurisdições onde os seus produtos serão comercializados.
- Sou um fabricante de dispositivos médicos dos US, com a intenção de comercializar o meu dispositivo apenas no Japão. Estou prestes a ser submetido a uma auditoria MDSAP. Preciso de cumprir os requisitos de outros países também?
Não, os fabricantes de dispositivos médicos só devem estar em conformidade com os requisitos e regulamentos da ISO 13485 nas jurisdições onde os seus produtos serão comercializados.
- A minha Organização de Auditoria (AO) e o Organismo Notificado Europeu são os mesmos. Posso ser auditado para ambos ao mesmo tempo?
Se o seu AO e o Organismo Notificado Europeu forem os mesmos, a avaliação da conformidade pode ser realizada após a auditoria MDSAP, e não simultaneamente. Os Organismos Notificados Europeus são observadores para o MDSAP, e a avaliação da conformidade é realizada de acordo com o EU MDR 2017/745. Para o MDSAP, a avaliação é realizada de acordo com os requisitos da ISO 13485 e os requisitos regulamentares dos países participantes abrangidos.
- Qual é a diferença entre as avaliações de Fase I e II?
O MDSAP inicial processo de auditoria envolve duas fases. A auditoria inicial, também designada por auditoria de Certificação Inicial, consiste em auditorias de Fase I e Fase II.
A auditoria da Fase I inclui a revisão da documentação e a avaliação da prontidão do fabricante de dispositivos médicos para ser submetido a uma auditoria da Fase II.
A auditoria de Fase II é realizada para verificar se todos os requisitos aplicáveis da ISO 13485 e outros requisitos regulamentares da autoridade regulamentar em questão são implementados.
- Quantos auditores posso esperar para uma auditoria MDSAP?
A Determinação do Tempo de Auditoria especifica como determinar a duração da auditoria no local em dias-homem. O AO decide quantos auditores irão compor a equipa de auditoria. Por exemplo, uma auditoria de (06) dias-homem pode ser concluída em três (03) dias por uma equipa de dois (02) auditores.
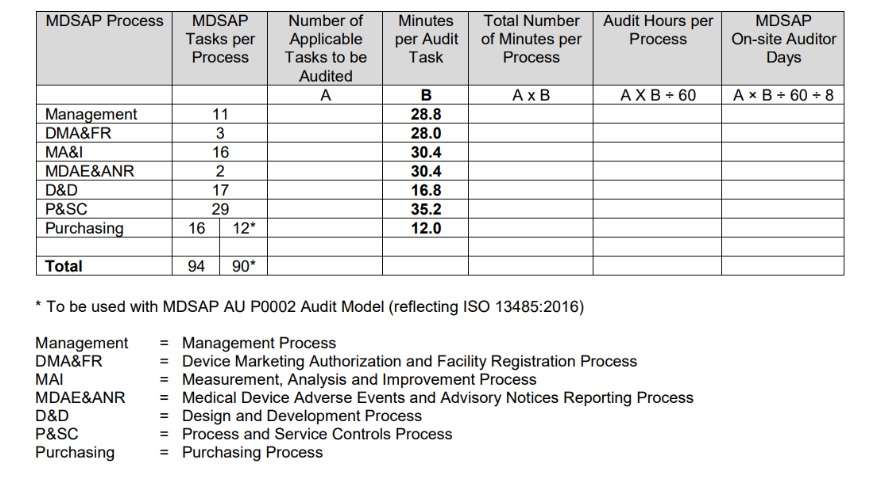
- Como é programada a auditoria MDSAP?
O Procedimento de Determinação do Tempo de Auditoria, emitido pela FDA, resume o processo para determinar a duração do cálculo da auditoria na tabela seguinte.
O cálculo da duração da auditoria baseia-se principalmente no número de tarefas de auditoria aplicáveis associadas ao tipo de auditoria a ser realizada e às atividades específicas da organização a serem auditadas.
Para informações detalhadas sobre o mesmo, pode consultar MDSAP P0008007.
- Existe um guia ou uma lista de verificação a que possa aceder para garantir a conformidade com uma auditoria MDSAP?
Sim, pode aceder ao documento MDSAP Audit Approach. É um guia bem organizado emitido pela USFDA que faz referência cruzada a secções específicas da ISO 13485:2016 e a regulamentos relevantes emitidos pela TGA da Austrália, ANVISA do Brasil, Health Canada do Canadá, MHLW/PMDA do Japão e US FDA.
- Qual é o papel de um observador numa auditoria MDSAP?
Um observador MDSAP é uma Autoridade Regulamentar que está autorizada a participar em reuniões, avaliações e outras atividades, mas não utiliza os resultados do MDSAP. Os observadores são representados no Conselho de Autoridades Regulamentares do MDSAP (RAC) por um gestor de nível superior.
- Quais são os próximos passos a seguir se recebi uma pontuação de 4 ou superior?
O sistema de classificação é atribuído às não conformidades observadas durante a auditoria pela AO. Uma pontuação de 4 ou 5 indica um alto risco de intervenção. Deve fornecer um plano de remediação para cada não conformidade registada no prazo de 15 dias de calendário a contar da data de emissão do relatório de não conformidade. O plano de remediação deve incluir os resultados da investigação da não conformidade, as suas causas e as ações corretivas planeadas para evitar qualquer recorrência. A evidência da implementação do plano/ação de remediação deve ser fornecida no prazo de trinta (30) dias de calendário a contar da data de conclusão da auditoria.
- Existe uma diferença no processo de abordagem da auditoria por um auditor interno vs. AO?
O MDSAP segue uma abordagem por processos. É provável que o AO analise as ligações e os pontos em comum, enquanto um auditor interno poderá focar-se mais num aspeto funcional de cada vez. Assim, o AO poderá encontrar uma não conformidade numa área funcional e procurar respostas noutra área funcional. No entanto, seguir a abordagem por processos poderá ser disruptivo durante uma auditoria interna.
- Posso recorrer à AO se puder provar que uma não conformidade registada não é válida?
A AO tem um processo de recurso ou disputa, que pode utilizar se conseguir demonstrar que uma não conformidade registada é inválida. No entanto, as classificações atribuídas às não conformidades não podem ser alteradas devido a ações corretivas. Só podem ser alteradas com base em evidências que demonstrem que não eram válidas.
- Qual é a validade do certificado MDSAP?
Os fabricantes de dispositivos médicos certificados ao abrigo do programa MDSAP serão auditados anualmente, de acordo com um ciclo de certificação de três anos. A auditoria inicial é uma auditoria completa ao QMS do fabricante de dispositivos médicos. É seguida por auditorias de vigilância realizadas anualmente durante dois (02) anos consecutivos. O ciclo recomeça com uma auditoria de recertificação no terceiro ano.
Para saber mais sobre os nossos serviços MDSAP, contacte a Freyr hoje para agendar uma chamada com os nossos Especialistas.









