
ALCANÇAR O PRAZO DE CONFORMIDADE IDMP ATÉ JULHO DE 2016: NÃO É UMA TAREFA TRIVIAL
Existem muitas questões sobre o IDMP, por exemplo: onde estão os dados numa organização? É necessária a limpeza e alinhamento dos dados atuais? Como é que as empresas organizam estes dados para fácil recuperação e submissão? A organização tem processos que podem beneficiar de um repositório central?
Alcançar a conformidade com a Identificação de Medicamentos (IDMP) não é uma tarefa trivial, a atividade deve ter em consideração várias pressões regulamentares e operacionais. As organizações devem esperar até que as autoridades emitam a orientação final e aprovem as especificações. Ao mesmo tempo, esperar por estas orientações pode não lhes deixar tempo suficiente para organizar os seus assuntos.
IDMP é uma norma complexa com implicações abrangentes de dados que exige colaboração e cooperação entre muitas unidades multifuncionais. A transição oferece uma oportunidade para uma análise End-to-End dos processos de negócio e das capacidades de TI de uma organização em várias unidades funcionais. Ajuda também a estabelecer um sistema robusto de gestão de mudanças.
As organizações devem compreender que uma boa arquitetura de informação requer esforço e tempo para ser alcançada e devem também reconhecer que o IDMP não é apenas um XEVMPD maior. É também importante notar que a orientação do ICH é apenas parte da história, e a disponibilidade de orientações regionais é crítica. Deve-se também ter em perspetiva que as implementações regionais paralelas terão âmbitos e prazos diferentes, com uma vasta gama de contribuidores de dados.
Além disso, as empresas farmacêuticas que pretendem comercializar em regiões regulamentadas devem tornar-se conformes com o IDMP a partir de 2016. Recentemente, a EMA organizou um dia de informação sobre o IDMP e partilhou o seu estado de implementação de alto nível e os prazos. Após discussão com a indústria farmacêutica, fornecedores de software e análise da disponibilidade dos seus próprios sistemas e recursos, a EMA planeou dividir a implementação geral do EU-IDMP em várias iterações. Este plano será proposto à Comissão Europeia (CE) para aprovação e, se conseguirem convencer a CE, a implementação do IDMP na UE será distribuída entre 2016 e 2018. No pior cenário, se a CE não concordar, não há plano B. As multas por não conformidade podem ascender a 5% da receita de uma organização; não ter uma boa solução para a conformidade inicial e contínua com o IDMP é um risco que nenhuma empresa farmacêutica pode dar-se ao luxo de correr.
IDMP: DESENVOLVIDO COMO UM CONJUNTO GLOBAL DE NORMAS NO ÂMBITO DA ISO
No caso de qualquer legislação que deva ser introduzida sobre a identificação de Medicamentos em qualquer um dos países ISO, esta será feita com base nas normas ISO IDMP. Uma vez que diferentes regiões adotem as normas IDMP, a entrada de dados será consistente e, por sua vez, as empresas globais e os reguladores terão acesso para verificar a consistência dos dados entre as regiões. Além disso, vocabulários controlados comuns facilitarão fortemente este processo.
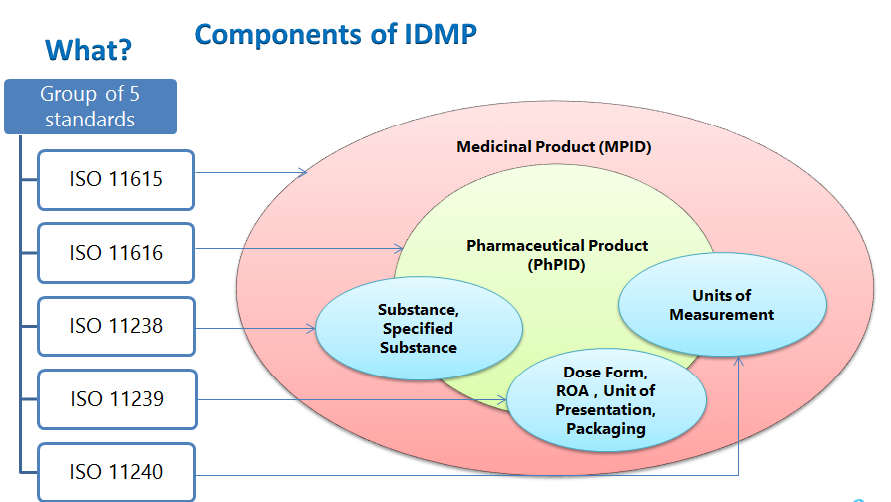
Os elementos estruturais da IDMP incluem o ID do medicamento, o ID do produto farmacêutico, o ID da substância, vocabulários controlados – forma farmacêutica, via de administração, componentes da embalagem, unidades de apresentação, unidades de medida e a descrição do processo de fabrico a ser submetida.
NORMAS IDMP
- ISO 11615 – Informação sobre produtos medicinais
- ISO 11616 – Informação sobre produtos farmacêuticos
- ISO 11238 – Substâncias
- ISO 11239 – Formas farmacêuticas, Unidades de apresentação, Vias de administração e Embalagem
- ISO 11240 – Unidades de medida
ESTADO ATUAL
O ICH está a preparar guias de implementação e a rever as normas ISO
Reguladores da UE preparam-se para o IDMP
- A EMA iniciou trabalhos para estabelecer ligação com a rede regulamentar da UE para definir os casos de negócio para os dados IDMP.
- A EMA está a criar um “Força-tarefa da UE para ISO IDMP recrutar especialistas dos Comités da EMA e do EU Network Data Board para alcançar este objetivo. Especificamente, irá:
- Definir os elementos de dados obrigatórios e opcionais da ISO IDMP
- Definir regras de negócio para elementos de dados opcionais
- Definir conformidade e tipos de dados
- Definir os modelos de governação da UE
POSIÇÃO DOS REGULADORES DOS US
- Liderança ativa no avanço do IDMP com os reguladores globais (antigo ICH) e com a ISO.
OUTROS REGULADORES
- Suíça – Pretende implementar após a UE (seguidor rápido)
- O Japão e o Canadá nomearam reguladores para serem especialistas no grupo IG de Substâncias.
CRONOLOGIAS
GUIAS EUROPEUS DE IMPLEMENTAÇÃO
- Rascunho dos guias de implementação iniciado e os guias estarão disponíveis a partir do 1.º trimestre de 2016
OUTROS
- A FDA ainda sem data, mas pretende desenvolver o SPL conforme necessário
- Japão – Incerto no ICH, mas agora a trabalhar no grupo do Regulador e na ISO
- Canadá – Espera-se que implemente, mas ainda sem detalhes específicos
- Suíça – Sem atualizações ainda
COMPREENDER OS REQUISITOS DE CONFORMIDADE IDMP
IDMP exige informação sobre Medicamentos em termos de um conjunto de identificadores padrão, que são construídos com base numa hierarquia de identificação criada durante a construção do Dicionário de Medicamentos EudraVigilance (EVMPD) ou na sua forma estendida (xEVMPD). Haverá uma sobreposição de informação com a que é submetida nas submissões de Structured Product Labeling (SPL) nos US e noutros registos de produtos a nível global.
No entanto, o IDMP possui novos identificadores, novas categorias e novas formas de expressar as relações entre os elementos no modelo de dados. O IDMP deve ser integrado no ADN da organização, pois precisa de impulsionar a construção de modelos de dados em toda a sua empresa. A infraestrutura de TI de uma organização pode então reconhecê-lo em vários sistemas, processos de negócio e unidades funcionais como RA, Segurança, I&D, documentação e processos de fabrico.
DESAFIOS DE CONFORMIDADE COM O IDMP
Organizacional
- Dados distribuídos entre vários departamentos
- Patrocínio sénior necessário para incentivar a participação
Técnico
- Descobrir, recolher e consolidar, limpar dados
- 250 a 300 campos por produto
Coordenação
- Gestão de mudanças contínuas
- Coordenação entre várias equipas
- Manter a conformidade dos dados com os processos internos
EM CONCLUSÃO:
IDMP: IMPACTO NA INDÚSTRIA FARMACÊUTICA
A implementação das normas IDMP deverá ter impacto na preparação e planeamento das submissões e na manutenção de dados a nível da empresa, incluindo dados de fabrico e informações estruturadas sobre substâncias para as informações de registo.
NORMA IDMP: GANHOS DE EFICIÊNCIA ASSEGURADOS APÓS A IMPLEMENTAÇÃO
Garantir que a sua organização está preparada para enfrentar o desafio IDMP exigirá uma estreita cooperação entre vários departamentos da sua organização. Um prestador de serviços competente, com um portefólio exclusivo de competências regulamentares, pode ajudar a avançar para a conformidade com o IDMP, o que pode ajudar uma organização a responder a novas oportunidades em evolução no mercado.










