
As submissões regulamentares e as tarefas de publicação têm sido tradicionalmente laboriosas, envolvendo horas de esforços manuais para formatar documentos, gerar PDFs em conformidade com a agência, realizar verificações de qualidade, compilar documentos para submissões, etc. Com os prazos exigentes, as empresas de ciências da vida apressam-se sempre para submissões atempadas. Em todo o mundo, os organismos de regulamentação estão a preparar-se para adotar desenvolvimentos recentes como o eCTD v4.0 para submissões de dossiês, alterações e outros relatórios. O eCTD v4.0 é uma mudança incremental que provavelmente irá impactar o futuro das submissões regulamentares, com todos os países a prepararem-se para o aceitar e implementar.
Considerando todos os desafios relacionados com as submissões regulamentares, a necessidade atual é uma solução tecnologicamente avançada para impulsionar o processo de submissão e revisão de medicamentos. Uma vez que as organizações já estão a considerar a automação como parte integrante do processo de submissão regulamentar, é crucial considerar como esta pode aumentar a produtividade durante a transição para o eCTD 4.0.
Como a Automação Ajuda na Transição para o eCTD 4.0?
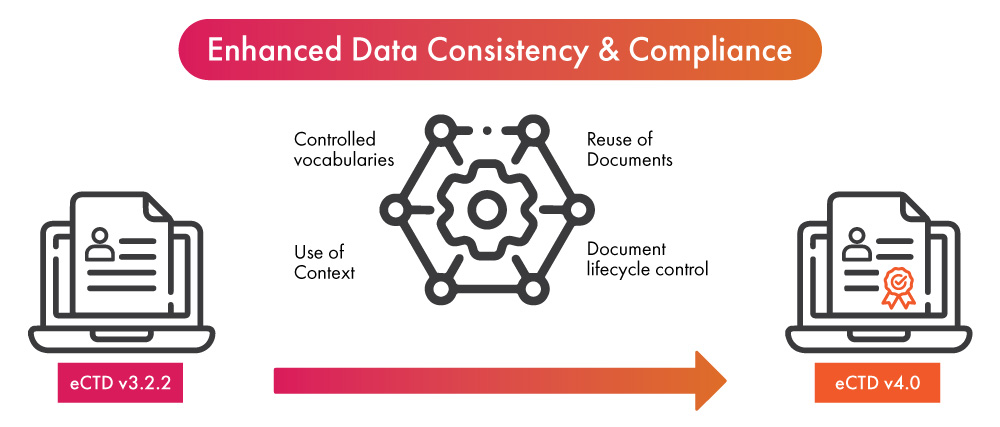
- No limiar da adoção da versão mais recente do eCTD, a implementação da automação no processo de submissão regulamentar pode trazer benefícios duplos para as empresas de ciências da vida, que incluem garantir a conformidade com o eCTD v4.0 num tempo mais rápido, por um lado, e melhorar a consistência dos dados e otimizar o processo de submissão, por outro.
- Uma vez que os dados tenham sido finalizados para utilização num (01) processo de regulamentação, a automação permite que os dados preencham outras submissões ou atualizações. Aproveita a nova funcionalidade do eCTD v4.0, que agora permite substituições de dados de muitos para um e de muitos para muitos, permitindo assim a reutilização dos dados de forma simplificada.
- As notificações automatizadas eliminam a necessidade de entregar mensagens ou fazer chamadas telefónicas quando a atividade é necessária. Isto permite uma comunicação mais rápida e clara, levando a vocabulários controlados, um componente essencial do eCTD v4.0.
- A automação na submissão de documentos ajudará a facilitar ainda mais o processo de atualização de conteúdo já submetido. Isto melhorará o controlo do ciclo de vida dos documentos submetidos.
- A automação em grupos de contexto pode acelerar o processo de organização de múltiplos ficheiros destinados a ser utilizados para submissões regulamentares.
No meio da transição para o eCTD v4.0, é crucial que as organizações de ciências da vida estabeleçam parcerias com fornecedores que estejam preparados para o novo padrão e compreendam como automatizar e otimizar o processo de publicação regulamentar. As empresas precisam de se preparar para adotar as mais recentes tecnologias impulsionadas pela automação para obter benefícios significativos e uma vantagem competitiva no mercado. O eCTD v4.0 é uma mudança importante que surgiu após muito tempo. As organizações precisam de iniciar a sua prova de conceito para testar o terreno, uma vez que será em breve aceite em muitos países em todo o mundo, dependendo dos prazos de cada país.
Nós, na Freyr, estamos na vanguarda da inovação através da tecnologia e estamos preparados para apoiar os nossos clientes ao tornar o nosso software de submissão regulamentar e publicação - Freyr SUBMIT PRO pronto para eCTD v4.0.
Para saber mais sobre a prontidão da Freyr para o eCTD 4.0, por favor, clique aqui para descarregar a sessão arquivada do webinar.









