
Além de completarem as submissões de dados xEVMPD necessárias, as organizações das ciências da vida terão agora de utilizar um formulário de submissão online chamado Digital Application Dataset Integration (DADI). A Agência Europeia de Medicamentos (EMA) concebeu o DADI como um substituto a longo prazo para o Formulário de Submissão Eletrónica (eAF) baseado em PDF, que foi criado para apoiar as submissões eCTD.
Os prazos para esta transição foram divulgados recentemente pela EMA. O DADI substituirá o formulário para variações de Medicamentos no ano de 2022. Outros formulários de submissão para Produtos Autorizados Centralmente (CAP) e Produtos Autorizados Nacionalmente (NAP) serão seguidos em breve até 2023. O projeto também substituirá os formulários utilizados para os principais procedimentos da UE, incluindo o Procedimento Centralizado (CP), o Procedimento de Reconhecimento Mútuo (MRP), o Procedimento Descentralizado (DCP) e o Procedimento Nacional (NP).
Os formulários web (incluindo o Formulário de Variações Humanas (HVF) para medicamentos destinados a humanos) irão uniformizar as entradas para os eAFs, a fim de fornecer dados mestre de produto padrão para medicamentos. Irão permitir tanto a saída existente legível por humanos como a nova saída legível por máquina para processamento digital, com base no padrão de troca de dados Fast Healthcare Interoperability Resources (FHIR) para medicamentos. Irão também utilizar os dados mestre de produto existentes dos Serviços de Gestão de Produtos (PMS) para preencher automaticamente os campos do formulário sempre que aplicável.
Os formulários DADI baseados na web destinam-se a permitir um processamento mais metódico de uma submissão, reduzindo assim a carga de trabalho da organização. Por exemplo, erros e discrepâncias serão reduzidos devido aos formulários que apoiam o escrutínio das submissões apresentadas pelas Autoridades de Saúde. Os formulários também abrirão caminho para dados "corretos à primeira" a serem introduzidos em bases de dados, tornando assim a integração de sistemas e a partilha de dados entre as Autoridades de Saúde sem esforço. Além disso, os novos formulários substituirão a tecnologia arcaica.
Benefícios do DADI
O objetivo do DADI e desta transformação dos processos regulamentares impulsionada por dados pode ser resumido da seguinte forma:
- Para melhorar a eficiência nas funções regulamentares, de R&D e de fabrico
- Para comunicar com as Autoridades de Saúde de forma mais rápida.
- Para permitir a tomada de decisão baseada em dados, tanto para as empresas como para as Autoridades
- Para ter melhores perceções e antevisão dos resultados de negócio e do desempenho geral
De forma holística, isto visa ser benéfico para os pacientes, reguladores, bem como para a indústria.
Últimas Alterações de Prazos pela EMA
- A data de entrada em vigor para os HVF foi adiada para outubro de 2022, da data inicialmente prevista de abril de 2022.
- Atualmente, o HVF está a ser submetido a Testes de Aceitação do Utilizador (UAT) fechados por um grupo composto por Especialistas na Matéria em DADI.
- Posteriormente, será realizada uma UAT integrada com um grupo maior de várias partes interessadas no segundo trimestre de 2022.
- Assim que for implementado, haverá uma fase de transição de seis (06) meses na qual tanto os eAFs (versão PDF antiga) como os formulários baseados na web serão aceites em paralelo. Após este período, apenas o HVF será aceite.
Consulte o seguinte infográfico para consultar os prazos para a implementação do HVF (Atualizado em fevereiro de 2022, sujeito a alterações pela EMA):
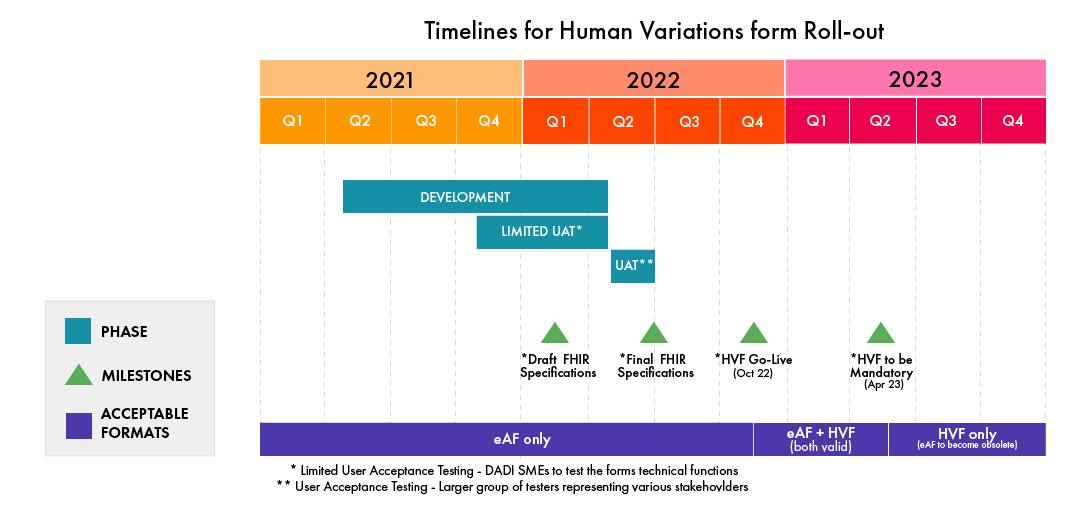
(fonte: EMA)
Garantir a Adaptabilidade ao Ambiente Regulamentar Dinâmico.
Todas as principais Autoridades de Saúde estão agora a avançar para a submissão de conjuntos de dados e documentos de alta qualidade. É importante que as organizações mantenham os mesmos num sistema unificado.
É também crucial ter uma compreensão clara de todo o ciclo de vida da submissão – os seus requisitos, as pessoas e os processos a ela associados, e o local atual dos dados de origem através de uma avaliação aprofundada das necessidades. A limpeza e o enriquecimento de dados devem ser priorizados se a avaliação indicar essa necessidade.
É imperativo ter um Sistema de Gestão de Informação Regulamentar (RIMS) em vigor que se adapte a regulamentos e diretrizes em evolução e que seja também flexível para redefinir as necessidades atuais da organização e cumprir com o ambiente regulamentar dinâmico. Para saber mais sobre o conjunto de soluções regulamentares da Freyr, que prepararão a sua organização para DADI e outras alterações de processo semelhantes, visite-nos em Freyr Digital.









