
A adoção do eCTD 4.0 representa um passo crucial para modernizar as submissões regulamentares em todo o mundo. Com benefícios como o rastreamento aprimorado de documentos e eficiências impulsionadas por Metadata, não é surpresa que as agências globais estejam a abraçar esta mudança.
Mas qual é a posição da EMA? Ao contrário da FDA, que delineou fases claras de implementação, a EMA está a adotar uma abordagem mais ponderada, começando com programas-piloto e avaliações técnicas. Neste blogue, detalhamos os planos da EMA para o eCTD 4.0, o seu potencial impacto nos processos regulamentares e como a sua empresa pode manter-se à frente.
Mais importante ainda, a EMA já tornou obrigatório o eCTD 4.0? Vamos aprofundar.
O que é o eCTD 4.0 e em que difere do eCTD 3.2.2?
O Documento Técnico Comum Eletrónico (eCTD) é o formato internacionalmente aceite para as submissões regulamentares. Este padroniza a forma como as empresas farmacêuticas submetem as submissões de medicamentos e gerem as atualizações do ciclo de vida em diferentes mercados.
A versão atual, eCTD 3.2.2, tem sido utilizada há anos. No entanto, as entidades reguladoras, incluindo a EMA, têm trabalhado no sentido do eCTD 4.0, que se baseia na norma Health Level 7 (HL7) Regulated Product Submission (RPS). Esta atualização melhora a eficiência das submissões e a gestão do ciclo de vida regulamentar.
Principais diferenças entre o eCTD 3.2.2 e o eCTD 4.0:
- Melhor Gestão do Ciclo de Vida: Rastreamento melhorado das versões dos documentos, reduzindo a duplicação.
- Granularidade Mais Flexível: Permite a reutilização estruturada de documentos em diferentes submissões.
- Melhor Manuseamento de Metadata: Metadata mais estruturada, tornando as interações regulamentares mais fluidas.
- Maior Interoperabilidade: Concebido para funcionar melhor com os sistemas regulamentares digitais em evolução a nível global.
- Embora estas mudanças ofereçam inúmeros benefícios, a transição para o eCTD 4.0 exige preparação, investimento e uma compreensão das expectativas regulamentares.
A Posição da EMA sobre a Adoção do eCTD 4.0
A grande questão na mente de todos é: A EMA tornou obrigatório o eCTD 4.0? A resposta é ainda não, mas a transição está em curso.
Estado Atual do eCTD 4.0 na UE:
- Atualmente, o eCTD 3.2.2 continua a ser o padrão obrigatório para as submissões na UE.
- A EMA tem avaliado ativamente o eCTD 4.0, mas ainda não tornou o seu uso obrigatório.
- A agência está a trabalhar em conjunto com outros organismos reguladores, como a FDA e a PMDA do Japão, para alinhar os padrões globais.
- Não foram estabelecidos prazos oficiais de transição, mas a EMA indicou que o eCTD 4.0 se tornará eventualmente obrigatório.
Abordagem da EMA: Implementação Faseada com um Programa Piloto
Ao contrário da USFDA, que delineou um plano de implementação faseado, a EMA está a adotar uma abordagem estruturada. A agência lançou um Programa Piloto Técnico para testar a implementação do eCTD 4.0 com as partes interessadas da indústria.
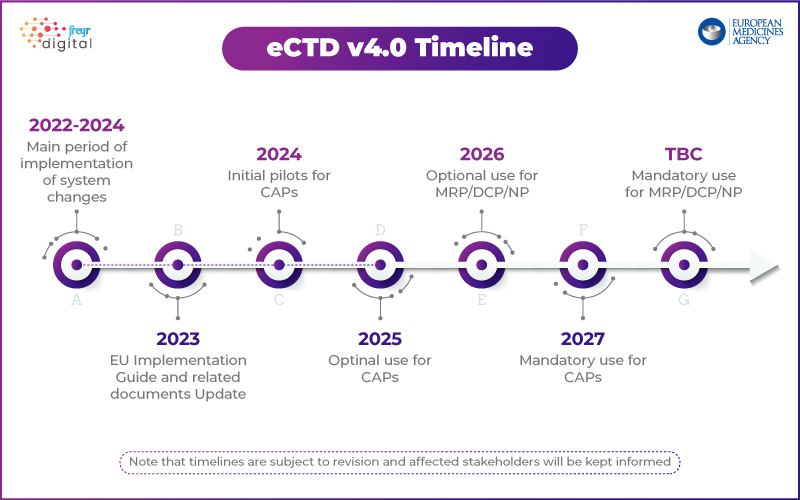
Principais destaques da estratégia eCTD 4.0 da EMA:
- Passo 1: Foco na interoperabilidade técnica com ferramentas regulamentares.
- Fases Futuras: Submissões de teste, gestão do ciclo de vida e submissões agrupadas.
- Pacote de implementação preliminar disponível com vocabulários controlados e critérios de validação.
A EMA está empenhada em assegurar uma transição tranquila, e as empresas de ciências da vida devem acompanhar as atualizações na página oficial da EMA sobre eCTD.
Desafios e Considerações para Empresas de Ciências da Vida
Embora o eCTD 4.0 ofereça benefícios claros, a sua adoção não está isenta de desafios. Aqui estão algumas considerações importantes para as empresas farmacêuticas e de biotecnologia:
- Complexidades Regulamentares
- A transição gradual da EMA significa que as empresas devem estar preparadas para processos de submissão duplos (eCTD 3.2.2 e eCTD 4.0).
- Diferentes regiões terão diferentes prazos de adoção, exigindo que as empresas se mantenham ágeis.
- Desafios Técnicos
- A migração de dados do eCTD 3.2.2 para o 4.0 exige um planeamento cuidadoso.
- As regras de validação mudarão significativamente, exigindo software e ferramentas atualizados.
- As empresas precisam de investir em automação e soluções impulsionadas por IA para garantir a conformidade.
- Riscos de Conformidade
- Mapeamento de metadata incorreto ou o incumprimento dos novos requisitos de granularidade de documentos poderá levar à rejeição da submissão.
- As equipas de regulamentação precisam de formação adequada para compreender as novas regras de validação.
- Impacto nos Fluxos de Trabalho Existentes
- As empresas terão de adaptar os processos internos para acomodar o eCTD 4.0.
- Será necessária uma maior colaboração entre as equipas de regulamentação, de TI e de submissão.
A principal conclusão? As empresas precisam de começar a preparar-se agora, mesmo que a EMA ainda não tenha tornado obrigatório o eCTD 4.0.
Como as empresas podem preparar-se para a transição para o eCTD 4.0 da EMA
Embora a EMA não tenha estabelecido um prazo oficial, as empresas proativas beneficiarão de uma preparação antecipada. Veja como:
- Avaliar os Processos de Submissão Atuais
- Identificar lacunas nos fluxos de trabalho eCTD 3.2.2 existentes.
- Avaliar como as novas regras de gestão do ciclo de vida irão impactar as submissões em curso.
- Investir nas Ferramentas eCTD 4.0 Certas
- Selecionar software de submissão regulamentar que seja compatível com o eCTD 4.0.
- Garantir que o software suporta as normas HL7 RPS e a automação de Metadata.
- Formar Equipas de Regulamentação e de TI
- Realizar workshops e sessões de formação sobre as alterações do eCTD 4.0.
- Fornecer orientações para a etiquetagem de Metadata e o acompanhamento do ciclo de vida.
- Interaja com a EMA e Pares da Indústria
- Participe nos programas-piloto da EMA e nas consultas regulamentares.
- Mantenha-se atualizado sobre as últimas orientações da EMA e as atualizações regulatórias.
- Realizar Testes e Validação
- Executar submissões de teste internas utilizando estruturas eCTD 4.0.
- Identifique potenciais problemas na granularidade de documentos e no mapeamento de Metadata antes do mandato final da EMA.
Ao começar agora, as empresas podem garantir uma transição suave sem interrupções nos registos regulamentares.
O Que Se Segue? O Futuro do eCTD 4.0 na Europa
Embora o cronograma completo de transição permaneça incerto, a estratégia de longo prazo da EMA envolve:
- Padronizar as submissões em todos os mercados globais, melhorando a consistência e a eficiência.
- Reduzir os prazos de aprovação através de um melhor acompanhamento do ciclo de vida das submissões.
- Integrar a IA e a automação nos fluxos de trabalho regulamentares para melhorar a conformidade.
Nos próximos anos, podemos esperar mais clareza da EMA, incluindo prazos de transição oficiais e novos critérios de validação.
Conclusão
Embora a EMA ainda não tenha tornado obrigatório o eCTD 4.0, é apenas uma questão de tempo até que se torne o padrão para as submissões regulamentares na UE. As empresas que se prepararem proativamente obterão uma vantagem competitiva, garantindo a conformidade e evitando obstáculos regulamentares de última hora.
Principais Conclusões
- O eCTD 3.2.2 continua a ser o padrão atual, mas o eCTD 4.0 está no horizonte.
- A EMA está a adotar uma abordagem gradual, sem um mandato oficial ainda.
- As empresas devem começar a preparar-se agora para garantir uma transição suave.
- Investir em novas tecnologias, formar equipas e testar as submissões será fundamental.
Apelo à Ação
Mantenha-se atualizado com os anúncios regulamentares da EMA e comece a avaliar a sua preparação para o eCTD 4.0. Quanto mais cedo se preparar, mais fácil será a transição quando a obrigatoriedade for implementada.
Gostaria de assistência na escolha de um software compatível com eCTD 4.0 ou de compreender como esta transição afeta o seu negócio? Sinta-se à vontade para nos contactar.









