
O mundo da regulamentação farmacêutica está prestes a receber uma grande atualização com a implementação do eCTD 4.0. Este formato padronizado promete um percurso mais fluido para as submissões de novos medicamentos às entidades reguladoras. Mas para as empresas que visam uma fatia do mercado farmacêutico japonês de 141,5 mil milhões de dólares, há uma reviravolta crucial – o Japão está a acelerar o cronograma de adoção!
Apresenta-se abaixo uma análise destes destaques:
- Adoção Obrigatória: Ao contrário de outras regiões que têm fases voluntárias antes da adoção obrigatória, até 2026, o Japão pretende tornar obrigatório o uso do eCTD 4.0.
- A Preparação é Fundamental: A preparação é fundamental devido às restrições de tempo e à ausência de um caminho de migração direto do formato PMDA JP1.0 do Japão para o eCTD 4.0, e focar-se num sistema melhor ajudará as empresas farmacêuticas no Japão durante o processo de transição. Estes passos incluem a atualização de software, a formação de pessoal e a preparação de PDFs para o novo formato.
- Recursos Disponíveis: A Agência de Produtos Farmacêuticos e Dispositivos Médicos (PMDA) do Japão publicou recursos que podem orientar as empresas nesta mudança, como o “ICH Electronic Common Technical Document eCTD 4.0 Implementation Guide”, com explicações sobre as alterações efetuadas e as melhores práticas disponíveis.
Seguem-se algumas razões pelas quais não deve perder este jogo de números:
- Via Rápida para eCTD 4.0: Ao contrário de outras regiões onde o processo é faseado, o Japão visa uma adoção obrigatória do eCTD 4.0 já em 2026. Isso é três anos antes do prazo estabelecido pela US FDA para 2029! Com um cronograma tão ambicioso, significa que o Japão assumiu a liderança em termos de incorporação global do eCTD.
- Sem Margem para Erro: O JP não pode ser diretamente convertido para eCTD 4.0, ao contrário das suas versões anteriores. Isto significa que as empresas farmacêuticas têm de estar extremamente preparadas para tal, a fim de evitar quaisquer atrasos na submissão, o que lhes poderá custar milhões em receita.
- Uma Ajuda Para Uma Entrada Suave: A Agência Japonesa de Produtos Farmacêuticos e Dispositivos Médicos (PMDA) compreende os desafios. Desenvolveram recursos, como guias de implementação, concebidos para orientar as empresas através destas modificações com facilidade e para uma boa entrada no mercado japonês. (https://www.pmda.go.jp/english/).
Se está a desenvolver medicamentos para o vasto mercado japonês, é hora de apertar o cinto! Aqui está a sua lista de verificação pré-voo:
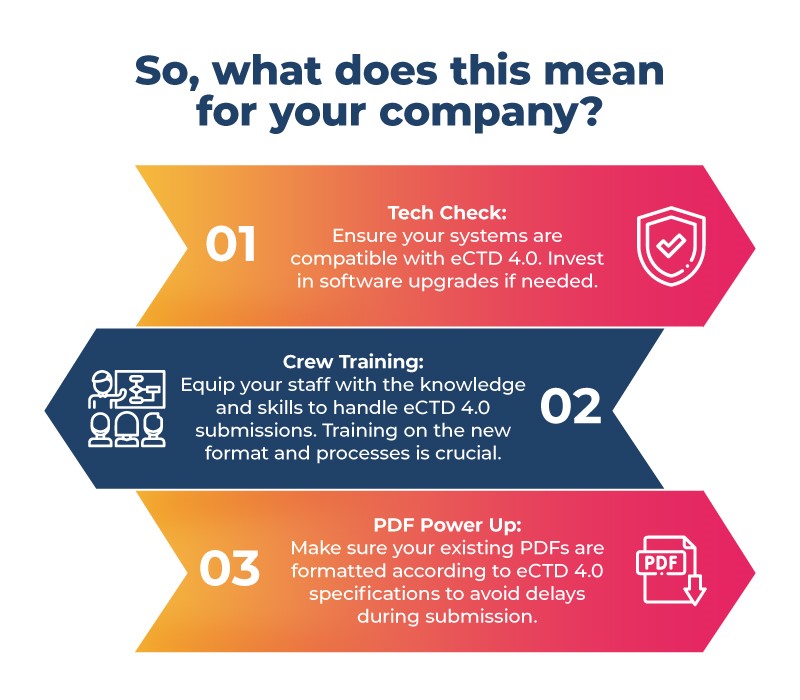
A transição para o eCTD 4.0 promete maior eficiência e padronização global em todo o processo de aprovação de medicamentos. A sua empresa pode antecipar esta mudança no Japão para uma transição suave e aproveitar as inúmeras oportunidades oferecidas por esta nova era. Lembre-se que não se preparar é preparar-se para falhar – por isso, esteja pronto para prosperar com o eCTD 4.0 no Japão.
Os benefícios e as oportunidades adquiridas são atrativos para a indústria farmacêutica. No entanto, apresenta a sua quota-parte de dificuldades ao longo do caminho que devem ser resolvidas. Para navegar sem problemas num ambiente regulamentar em constante mudança, as empresas podem procurar parcerias com consultores fiáveis como a Freyr. Abrace o futuro das submissões regulamentares no Japão com o nosso software eCTD incomparável, Freyr SUBMIT PRO, que está em conformidade com as normas 21 CFR Part 11 e possui um modelo de implementação flexível. Contacte-nos hoje para saber mais e embarcar numa jornada rumo a uma maior eficiência e sucesso. Solicite uma demonstração hoje.









